Axit nitric có rất nhiều ứng dụng quan trọng. Phần lớn dùng để sản xuất phân đạm, ngoài ra còn được dùng để sản xuất thuốc nổ, thuốc nhuộm, dược phẩm,… Bài viết dưới đây sẽ giúp các em nhận biết axit này nhanh nhất.
Cách nhận biết axit nitric (HNO3)
I. Cách nhận biết axit nitric (HNO3)
- Axit nitric là một axit mạnh và có tính oxi hóa rất mạnh.
- Cách nhận biết dung dịch axit HNO3 loãng:
+ Dùng quỳ tím: quỳ tím chuyển sang màu đỏ.
+ Dùng kim loại Cu: Đồng tan ra, dung dịch thu được có màu xanh, thoát ra khí màu nâu (thực tế là thoát ra khí không màu hóa nâu ngoài không khí).
3Cu + 8HNO3 loãng → 3Cu(NO3)2 + 2NO↑ + 4H2O
2NO(không màu) + O2 → 2NO2 (nâu đỏ)
II. Mở rộng
- Axit nitric tinh khiết là chất lỏng, không màu, bốc khói mạnh trong không khí ẩm.
- Axit nitric kém bền. Ngay ở điều kiện thường, khi có ánh sáng, dung dịch axit nitric đặc bị phân hủy một phần giải phóng khí NO2. Khí này tan trong dung dịch axit, làm cho dung dịch có màu vàng.
4HNO3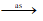 4NO2 + 2H2O + O2
4NO2 + 2H2O + O2
- Trong phòng thí nghiệm, thường có loại HNO3 đặc có nồng độ 68%.
- Axit nitric bốc khói chứa 98% HNO3 thường được sử dụng trong ngành công nghiệp thuốc nổ.
III. Bài tập nhận biết axit nitric (HNO3)
Bài 1: Cho các hóa chất sau: quỳ tím, Cu, NaOH, phenolphtalein, BaCl2, AgNO3. Số chất có thể phân biệt hai dung dịch loãng: HNO3 và HCl đựng trong lọ bị mất nhãn?
A. 1
B. 2
C. 3
D. 4
Hướng dẫn giải:
- Quỳ tím, phenolphtalein, BaCl2, NaOH không phân biệt được.
- Cho Cu vào, hiện tượng thu được:
+ Đồng tan ra, dung dịch có màu xanh, có khí thoát ra: HNO3.
3Cu + 8HNO3 loãng → 3Cu(NO3)2 + 2NO↑ + 4H2O
2NO + O2 → 2NO2
+ Không hiện tượng: HCl
- Cho AgNO3 vào, hiện tượng thu được:
+ Xuất hiện kết tủa trắng: HCl.
AgNO3 + HCl → AgCl↓ + HNO3
+ Không hiện tượng: HNO3.
Đáp án B
Bài 2: Chỉ dùng một hóa chất, hãy phân biệt các dung dịch sau: HNO3, NaNO3, H2SO4, Ba(OH)2 chứa trong các lọ mất nhãn.
Hướng dẫn giải:
- Đánh số thứ tự từng lọ mất nhãn, trích mỗi lọ một ít sang ống nghiệm đánh số tương ứng (trích mẫu thử).
- Cho các mẩu quỳ tím vào các mẫu thử, hiện tượng:
+ Quỳ tím chuyển sang màu đỏ: HNO3 và H2SO4 (nhóm I)
+ Quỳ tím chuyển sang màu xanh: Ba(OH)2.
+ Quỳ tím không đổi màu: NaNO3.
- Cho vài giọt dung dịch Ba(OH)2 vừa nhận biết ở trên vào các mẫu thử nhóm I, hiện tượng:
+ Xuất hiện kết tủa trắng: H2SO4.
H2SO4 + Ba(OH)2 → BaSO4↓ + 2H2O
+ Không hiện tượng: HNO3.
Ba(OH)2 + 2HNO3 → Ba(NO3)2 + 2H2O
Xem thêm cách nhận biết các chất hóa học nhanh, chi tiết khác:
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.