Ở điều kiện thường, clo là chất khí màu vàng lục, mùi xốc, rất độc, nó phá hoại niêm mạc của đường hô hấp. Clo tan trong nước gọi là nước clo có màu vàng nhạt. Khí clo tan nhiều trong các dung môi hữu cơ như benzen, etanol, hexan cacbon tetraclorua,…Nhận biết khí clo bằng phương pháp hóa học như thế nào? Ứng dụng của clo là gì? Bài viết sau đây, sẽ cung cấp các kiến thức này cho các em.
Cách nhận biết khí Cl2
I. Cách nhận biết khí Cl2
Một số cách nhận biết khí clo:
* Cách 1: Sục khí vào dung dịch AgNO3
- Hiện tượng: Xuất hiện kết tủa màu trắng.
- Phương trình hóa học:
Cl2 + H2O ⇄ HCl + HClO
HCl + AgNO3 → AgCl↓ + HNO3
* Cách 2: Sục khí Cl2 vào dung dịch KI cho thêm ít hồ tinh bột.
- Hiện tượng: Dung dịch hóa xanh đậm
- Phương trình hóa học:
Cl2 + 2KI → I2 + 2KCl
- Giải thích: Iot sinh ra tác dụng với hồ tinh bột tạo ra chất có màu xanh.
* Cách 3: Dùng quỳ tím ẩm
- Hiện tượng: giấy quỳ tím chuyển sang màu đỏ nhưng ngay sau đó bị mất màu.
- Giải thích: Do clo tác dụng với nước sinh ra HCl và HClO làm quỳ tím chuyển đỏ. Tuy nhiên, HClO có tính tẩy màu làm quỳ tím mất màu.
- Phương trình hóa học:
Cl2 + H2O ⇄ HCl + HClO
II. Mở rộng
Clo có rất nhiều ứng dụng trong sản xuất công nghiệp:
+ Điều chế nước Ja-ven.
+ Tẩy trắng vải, sợi, bột giấy.
+ Khử trùng nước sinh hoạt.
+ Điều chế nhựa PVC, chất dẻo, chất màu, cao su.
III. Bài tập nhận biết khí Cl2
Bài 1: Dùng thuốc thử nào để phân biệt ba khí sau: Cl2, SO2, CO2.
Hướng dẫn giải:
- Dẫn các khí qua dung dịch nước Br2, hiện tượng thu được:
+ Dung dịch Br2 mất màu: SO2
Phương trình hóa học:
SO2 + Br2 + 2H2O → 2HBr + H2SO4
+ Không hiện tượng: Cl2 và CO2.
- Dẫn hai khí còn lại lần lượt qua dung dịch nước vôi trong dư, hiện tượng:
+ Dung dịch vẩn đục: CO2
Phương trình hóa học:
CO2 + Ca(OH)2 → CaCO3↓ + H2O
+ Dung dịch không có hiện tượng: Cl2
Phương trình hóa học:
2Cl2 + 2Ca(OH)2 → CaCl2 + Ca(ClO)2 + 2H2O
Chú ý: Cl2 có phản ứng với Ca(OH)2 nhưng không cho hiện tượng có thể quan sát được.
Bài 2: Bằng phương pháp hóa học hãy nhận biết các chất khí sau: H2, HCl, Cl2, O2.
Hướng dẫn giải:
- Cho mẩu quỳ tím ẩm vào các lọ chứa các khí trên:
+ Quỳ tím chuyển sang màu đỏ: HCl
+ Quỳ tím chuyển sang màu đỏ, sau đó bị mất màu: Cl2
Cl2 + H2O ⇄ HCl + HClO
(HClO có tính tẩy màu nên làm mất màu quỳ tím)
+ Không hiện tượng: H2, O2.
- Dẫn lần lượt 2 khí qua ống nghiệm đựng CuO đun nóng, hiện tượng:
+ Chất rắn màu đen chuyển dần sang màu đỏ: H2
CuO + H2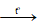 Cu↓ + H2O
Cu↓ + H2O
+ Không hiện tượng: O2.
Xem thêm cách nhận biết các chất hóa học nhanh, chi tiết khác:
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.