Bài tập nhận biết, phân biệt anken là bài tập khá phổ biến trong chương trình hóa học phổ thông. Bài tập thường hỏi về cách nhận biết, phân biệt anken với các hiđrocacbon khác hoặc các dẫn xuất của hiđrocacbon. Bài viết dưới đây sẽ hướng dẫn bạn cách nhận biết, phân biệt anken chính xác và nhanh nhất.
Cách nhận biết anken
I. Cách nhận biết anken
- Để nhận biếtanken ta sử dụng dung dịch brom (Br2) hoặc dung dịch thuốc tím (KMnO4). Anken sẽ làm mất màu nâu đỏ của dung dịch Br2 hoặc làm mất màu màu tím của dung dịch KMnO4.
- Nhận biết anken bằng dung dịch brom
+ Tổng quát: CnH2n + Br2 → CnH2nBr2
+ Hiện tượng: Khi anken phản ứng với dung dịch brom ở nhiệt độ thường thấy màu nâu đỏ của dung dịch brom nhạt dần, nếu anken dư dung dịch mất màu.
+ Phương trình hóa học minh họa:
CH2=CH2 + Br2(màu nâu đỏ) → CH2Br-CH2Br (không màu)
CH3-CH=CH-CH3 + Br2 (màu nâu đỏ) → CH3-CHBr-CHBr-CH3 (không màu)
+ Giải thích: Phản ứng xảy ra do dung dịch brom tham gia phản ứng cộng ̣̣(phá vỡ liên kết π trong anken).
- Nhận biết anken bằng dung dịch KMnO4
+ Tổng quát: 3CnH2n+2KMnO4+ 4H2O → 3CnH2n(OH)2+2MnO2↓+2KOH
+ Hiện tượng: Khi anken phản ứng với dung dịch KMnO4 ở nhiệt độ thường thấy màu của dung dịch KMnO4 nhạt dần và có kết tủa đen MnO2.
+ Phương trình hóa học minh họa:
3CH2=CH2 + 4H2O + 2KMnO4 → 3HO-CH2-CH2-OH + 2MnO2↓ + 2KOH
+ Giải thích: Do xảy ra phản ứng oxi hóa không hoàn toàn giữa anken và dung dịch KMnO4
Chú ý:
- Những phương pháp trên có thể dùng để nhận biết anken và ankan.
- Xicloankan vòng ba cạnh cũng có khả năng làm mất màu dung dịch brom (phản ứng cộng mở vòng)
- Những phương pháp trên không dùng để nhận biết anken với các hợp chất không no có liên kết C=C, C ≡ C.
II. Mở rộng
- Nhận biết anken với ank-1-in bằng dung dịch AgNO3/NH3.
Các ank-1-in phản ứng sẽ tạo kết tủa màu vàng. Anken không có phản ứng này.
+ Phương trình hóa học:
CH ≡ C-CH3 + AgNO3 + NH3 → CAg ≡ C-CH3↓vàng + NH4NO3
III. Bài tập nhận biết anken
Bài 1:Có hai bình mất nhãn đựng hai khí không màu là metan và etilen. Trình bày phương pháp hóa học phân biệt hai bình khí.
Huướng dẫn giải:
Dẫn lần lượt từng khí qua ống nghiệm đựng dung dịch brom, khí nào làm brom nhạt màu là etilen:
CH2=CH2 + Br2(màu nâu đỏ) → CH2Br-CH2Br (không màu)
Khí không làm brom nhạt màu là metan
Bài 2: Phân biệt các khí sau: N2, H2, CH4, C2H2, C2H4, chứa trong các bình mất nhãn.
Hướng dẫn giải:
Nhận xét:
- N2: không cho phản ứng cháy.
- H2: đốt cháy, sản phẩm cháy không làm đục nước vôi trong.
- CH4: đốt cháy, sản phẩm cháy làm đục nước vôi trong.
- Các khí còn lại dùng các phản ứng đặc trưng để nhận biết.
Cách nhận biết:
- Cho các khí tác dụng với dung dịch AgNO3/NH3. Khí nào tạo được kết tủa vàng là C2H2.
CH ≡ CH + 2AgNO3 + 2NH3 → CAg ≡ CAg↓ + 2NH4NO3
- Dẫn các khí còn lại qua dung dịch nước brom (màu nâu đỏ). Khí nào làm nhạt màu nước brom là C2H4.
H2C=CH2 + Br2 → BrH2C-CH2Br
- Lần lượt đốt cháy 3 khí còn lại, sau đó dẫn sản phẩm cháy qua bình đựng nước vôi trong.
+ Khí không cháy là N2.
+ Khí cháy, cho sản phẩm cháy nào làm đục nước vôi trong là CH4.
CH4 + 2O2 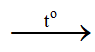 CO2 + 2H2O
CO2 + 2H2O
CO2 + Ca(OH)2 → CaCO3↓ +H2O
+Khí cháy, sản phẩm cháy không làm đục nước vôi trong là H2.
2H2 + O2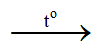 2H2O
2H2O
Xem thêm cách nhận biết các chất hóa học nhanh, chi tiết khác:
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.