Khi xăng cháy trong động cơ ô tô sẽ tạo ra nhiệt độ cao, lúc đó N2 phản ứng với O2 tạo thành NO:
N2( g)+O2( g)⇌2NO(g)NO khi được giải phóng ra không khí nhanh chóng kết hợp với O2 tạo thành NO2 là một khí gây ô nhiễm môi trường. Ở 2000oC, hằng số cân bằng Kc của phản ứng (1) là 0,01.
Nếu trong bình kín dung tích 1 lít có 4 mol N2 và 0,1 mol O2 thì ở 2000oC lượng khí NO tạo thành là bao nhiêu (giả thiết NO chưa phản ứng với O2 )?
 Giải bởi Vietjack
Giải bởi Vietjack
Phương trình phản ứng: N2(g) + O2(g) ⇌ 2NO(g)
Ban đầu: 4 0,1 0 (mol/L)
Cân bằng: 4−x1 0,1−x1 2x (mol/L)
Hằng số cân bằng Kc=4x2(0,1−x).(4−x)=0,01⇒ x≈0,027
Vậy số mol khí NO tạo thành là: 2x.1 = 0,054 (mol) ⇒ x≈0,027
Cho phản ứng hoá học sau: Br2( g)+H2( g)⇌2HBr(g)
Biểu thức hằng số cân bằng (Kc) của phản ứng trên là
A. KC=2[HBr][Br2][H2].
B. KC=[HBr]2[H2][Br2].
C. KC=[H2][Br2][HBr]2.
D. KC=[H2][Br2]2[HBr].
Phosphorus trichloride (PCl3) phản ứng với chlorine (Cl2) tạo thành phosphorus pentachloride (PCl5) theo phản ứng:
PCl3( g)+Cl2( g)⇌PCl5( g)
Cho 0,75 mol PCl3 và 0,75 mol Cl2 vào bình kín dung tích 8 lít ở 227oC. Tính nồng độ các chất ở trạng thái cân bằng, biết giá trị hằng số cân bằng Kc ở 227oC là 49.
Trong dung dịch muối CoCl2 (màu hồng) tồn tại cân bằng hoá học sau:
[Co(H2O)6]2+ + 4Cl−⇌[CoCl4]2−+6H2O ΔrH0298<0
màu hồng màu xanh
Dự đoán sự biến đổi màu sắc của ống nghiệm đựng dung dịch CoCl2 trong các trường hợp sau:
a) Thêm từ từ HCl đặc.
Polystyrene là một loại nhựa thông dụng được dùng để làm đường ống nước. Nguyên liệu để sản xuất polystyrene là styrene (C6H5CH2CH3). Styrene được điều chế từ phản ứng sau:
C6H5CH2CH3( g)⇌C6H5CH=CH2( g)+H2( g) ΔrHo298=123 kJ
Cân bằng hoá học của phản ứng trên sẽ chuyển dịch theo chiều nào nếu:
a) Tăng áp suất của bình phản ứng.
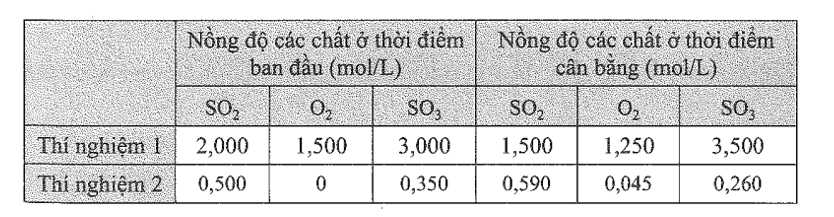
Các kết quả trong bảng sau đây được ghi lại từ hai thí nghiệm giữa khí sulfur dioxide và khí oxygen để tạo thành khí sulfur trioxide ở 600oC. Tính giá trị Kc ở hai thí nghiệm và nhận xét kết quả thu được.
c) Khi tăng áp suất, các cân bằng hoá học chuyển dịch theo chiều thuận là
A. (1); (2) và (3).
B. (1); (3) và (5).
C. (2); (3) và (4).
D. (3); (4) và (5).
Cho 5 mol H2 và 5 mol I2 vào bình kín dung tích 1 lít và nung nóng đến 227oC. Đồ thị biểu diễn sự thay đổi nồng độ các chất theo thời gian được cho trong hình sau:
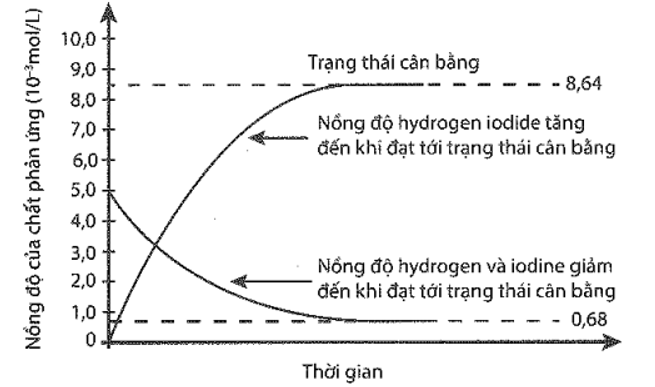
Nồng độ của HI ở trạng thái cân bằng là
A. 0,68 M.
B. 5,00 M.
C. 3,38 M.
D. 8,64 M.
Cho cân bằng hoá học sau:
4NH3( g)+5O2( g)⇌4NO(g)+6H2O(g) ΔrHo298=−905 kJ
Yếu tố nào sau đây cần tác động để cân bằng trên chuyển dịch sang phải?
A. Giảm nhiệt độ.
B. Tăng áp suất.
C. Giảm nồng độ của O2.
D. Thêm xúc tác Pt.
b) Khi tăng nhiệt độ, các cân bằng hoá học chuyển dịch theo chiều thuận là
A. (1); (2) và (3).
B. (1); (2) và (5).
C. (4) và (5).
D. (3) và (5).
Cho phản ứng hoá học sau: N2O4( g)⇌2NO2( g) KC=4,84⋅10−3 Phương án nào sau đây là nồng độ của các chất tại thời điểm cân bằng?
A. [N2O4( g)]=4,84⋅10−1M;[NO2( g)]=1,0⋅10−4M.
B. [N2O4( g)]=1,0⋅10−1M;[NO2( g)]=4,84⋅10−4M.
C. [N2O4( g)]=1,0⋅10−1M;[NO2( g)]=2,20⋅10−2M.
D. [N2O4( g)]=5,0⋅10−2M;[NO2( g)]=1,10⋅10−2M..






Cho dãy các chất sau: KOH, NaCl, H2SO3, CuO, C6H12O6 (glucose). Số chất không điện li có trong dãy là?




CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.