Với Giải SBT Hóa học 10 trang 13 trong Bài 3: Nguyên tố hóa học Sách bài tập Hóa học lớp 10 Chân trời sáng tạo hay nhất, chi tiết sẽ giúp học sinh dễ dàng làm bài tập trong SBT Hóa học 10 trang 13.
SBT Hóa học 10 trang 13
Bài 3.10 trang 13 sách bài tập Hóa học 10: Hoàn thành những thông tin còn thiếu trong bảng trang 13 sách bài tập Hóa học lớp 10 sau:
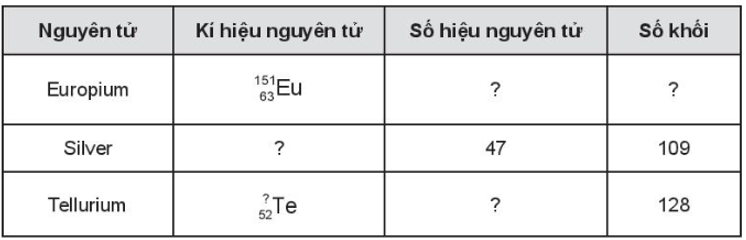
Lời giải:
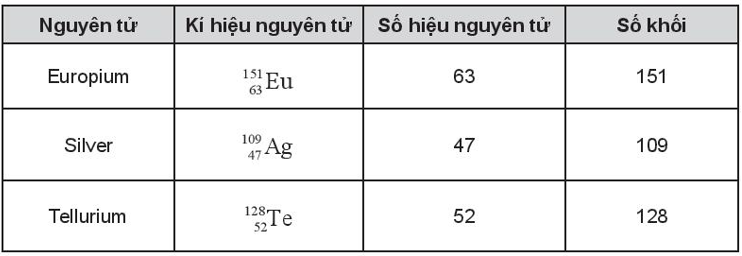
Bài 3.11 trang 13 sách bài tập Hóa học 10: Cho biết số proton, neutron và electron của nguyên tử
Lời giải:
Số proton = số electron = Z = 30.
Số neutron = số khối (A) – số hiệu nguyên tử (Z) = 65 – 30 = 35.
Bài 3.12 trang 13 sách bài tập Hóa học 10: Nguyên tử Mg có ba đồng vị ứng với thành phần phần trăm về số nguyên tử như sau:

Lời giải:
Giả sử trong hỗn hợp nói trên có 50 nguyên tử 25Mg, số nguyên tử tương ứng của hai đồng vị 24Mg và 26Mg lần lượt là:
A. 389 và 56.
B. 56 và 389.
C. 495 và 46.
D. 56 và 495.
Lời giải:
Đáp án đúng là: A
Giả sử trong hỗn hợp nói trên có 50 nguyên tử 25Mg, số nguyên tử tương ứng của hai đồng vị còn lại là:
+ Số nguyên tử 24Mg: nguyên tử.
+ Số nguyên tử 26Mg: nguyên tử.
Bài 3.13 trang 13 sách bài tập Hóa học 10: Hãy so sánh:
a. Số lượng hợp chất và số lượng nguyên tố.
b. Số lượng nguyên tố và số lượng đồng vị.
Lời giải:
a) Số lượng hợp chất lớn hơn số lượng nguyên tố vì hợp chất là sự kết hợp của 2 hay nhiều nguyên tố.
b) Số lượng nguyên tố ít hơn số lượng đồng vị vì hầu hết các nguyên tố hóa học đều có nhiều đồng vị.
Bài 3.14 trang 13 sách bài tập Hóa học 10: Oxide của kim loại M (M2O) được ứng dụng rất nhiều trong ngành hóa chất như sản xuất xi măng, sản xuất phân bón, … Trong sản xuất phân bón, chúng ta thường thấy M2O có màu trắng, tan nhiều trong nước và là thành phần không thể thiếu cho mọi loại cây trồng. Tổng số hạt cơ bản trong phân tử X có công thức M2O là 140, trong phân tử X có tổng số hạt mang điện nhiều hơn số hạt không mang điện là 44. Xác định công thức phân tử của M2O.
Lời giải:
Trong X có 2 nguyên tử M và 1 nguyên tử O.
Nguyên tử O có pO = 8 và nO = 8
Tổng số hạt cơ bản trong phân tử X có công thức M2O là 140 nên:
4pM + 2nM + 2pO + nO = 140 hay 4pM + 2nM = 116 (1)
Trong phân tử X có tổng số hạt mang điện nhiều hơn số hạt không mang điện là 44 nên:
(4pM + 2pO) – ( 2nM + nO) = 44 hay 4pM – 2nM = 36 (2)
Từ (1) và (2) có pM = 19 và nM = 20.
Vậy M là K (potassium); X là K2O.
Bài 3.15 trang 13 sách bài tập Hóa học 10: Hợp chất XY2 phổ biến trong sử dụng để làm cơ chế đánh lửa bằng bánh xe trong các dạng súng cổ. Mỗi phân tử XY2 có tổng các hạt proton, neutron, electron bằng 178; trong đó, số hạt mang điện nhiều hơn số hạt không mang điện là 54, số hạt mang điện của X ít hơn số hạt mang điện của Y là 12. Hãy xác định kí hiệu hóa học của X, Y.
Lời giải:
Kí hiệu số đơn vị điện tích hạt nhân X, Y lần lượt là ZX; ZY; số neutron (hạt không mang điện) của X và Y lần lượt là NX và NY.
Mỗi phân tử XY2 có tổng các hạt proton, neutron, electron bằng 178 nên:
2ZX + 4ZY + NX + 2NY = 178 (1)
Trong XY2, số hạt mang điện nhiều hơn số hạt không mang điện là 54 nên:
2ZX + 4ZY – (NX + 2NY) = 54 (2)
Từ (1) và (2) ta có: 2ZX + 4ZY = 116 (3)
Lại có trong XY2 số hạt mang điện của X ít hơn số hạt mang điện của Y là 12, nên:
2ZX + 12 = 4ZY (4)
Từ (3) và (4) ta có: ZX = 26; ZY = 16.
Vậy X là sắt (iron, Fe); Y là lưu huỳnh (sulfur, S).
Xem thêm lời giải vở bài tập Hóa học lớp 10 Chân trời sáng tạo với cuộc sống hay, chi tiết khác:
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.