Với Giải SBT Hóa học 10 trang 37 trong Bài 10: Liên kết cộng hóa trị Sách bài tập Hóa học lớp 10 Chân trời sáng tạo hay nhất, chi tiết sẽ giúp học sinh dễ dàng làm bài tập trong SBT Hóa học 10 trang 37.
Nội dung bài viết
SBT Hóa học 10 trang 37
Bài 10.21 trang 37 sách bài tập Hóa học 10: Giải thích vì sao độ âm điện của nitrogen là 3,04 xấp xỉ với độ âm điện của chlorine là 3,16 nhưng ở điều kiện thường, nitrogen kém hoạt động hơn nhiều so với chlorine.
Lời giải:
Tuy có độ âm điện xấp xỉ nhau nhưng phân tử nitrogen có liên kết ba (N ≡ N), còn phân tử chlorine chỉ có liên kết đơn (Cl – Cl) nên phân tử nitrogen có năng lượng liên kết (945 kJ/ mol) lớn hơn nhiều so với phân tử chlorine (243 kJ/ mol), dẫn đến phải tiêu tốn năng lượng nhiều hơn để phá vỡ liên kết trong phân tử nitrogen so với trong phân tử chlorine. Vì vậy ở điều kiện thường, nitrogen kém hoạt động hơn nhiều so với chlorine.
Bài 10.22 trang 37 sách bài tập Hóa học 10: Dưới đây là biểu đồ tương tác của hai nguyên tử hydrogen ở thể khí so với khoảng cách hạt nhân giữa chúng:
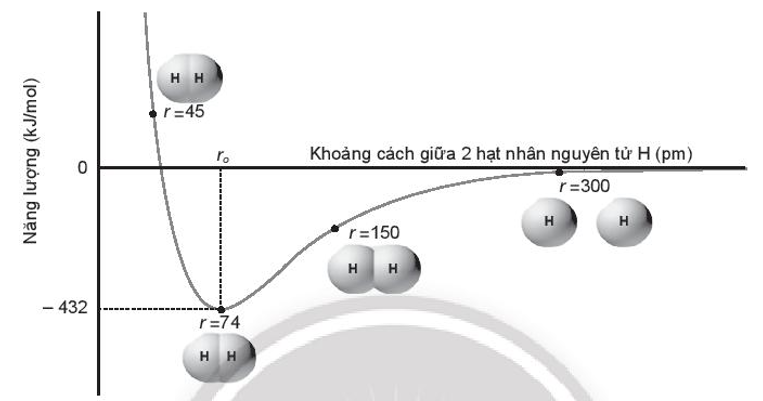
Cho biết năng lượng liên kết của phân tử hydrogen (H2) và độ dài liên kết H – H là bao nhiêu? Giải thích.
Lời giải:
Trên biểu đồ, năng lượng tối thiểu đại diện cho độ bền liên kết và khoảng cách ro tại mức năng lượng tối thiểu gọi là độ dài liên kết. Do đó phân tử H2 có năng lượng liên kết là 432 kJ/mol và có độ dài liên kết H – H là 74 pm.
Bài 10.23 trang 37 sách bài tập Hóa học 10: Sodium chloride tan được trong nước hay trong dầu hỏa? Giải thích.
Lời giải:
Sodium chloride là hợp chất ion nên chỉ tan trong dung môi phân cực là nước, không tan trong dung môi không phân cực là dầu hỏa.
Bài 10.24 trang 37 sách bài tập Hóa học 10: Vì sao benzene (C6H6) không tan trong nước nhưng tan tốt trong các dung môi hữu cơ như tetrachloromethane (CCl4), hexane (C6H14), …?
Lời giải:
Benzene (C6H6) là hợp chất không phân cực nên benzene không tan trong dung môi phân cực (nước) mà tan tốt trong các dung môi không phân cực như tetrachloromethane (CCl4), hexane (C6H14), …
Bài 10.25 trang 37 sách bài tập Hóa học 10: Biết phân tử BF3 có cấu trúc phẳng, phân tử CCl4 có cấu trúc hình tứ diện đều. Hãy cho biết có bao nhiêu phân tử phân cực và không phân cực trong hình dưới đây? Giải thích.
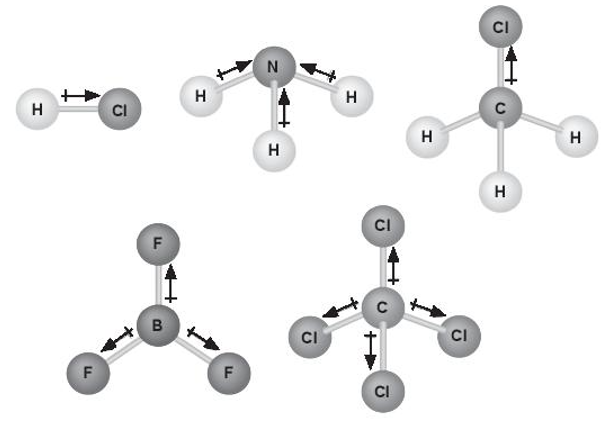
Lời giải:
- Ba phân tử đầu: HCl, NH3, CH3Cl đều là các phân tử phân cực, do tổng moment lưỡng cực không triệt tiêu.
- Hai phân tử sau: BF3, CCl4 đều là các phân tử không phân cực do tổng moment lưỡng cực triệt tiêu.
Xem thêm lời giải vở bài tập Hóa học lớp 10 Chân trời sáng tạo với cuộc sống hay, chi tiết khác:
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.