Với Giải SBT Hóa học 10 trang 29 trong Bài 10: Quy tắc octet Sách bài tập Hóa học lớp 10 Kết nối tri thức hay nhất, chi tiết sẽ giúp học sinh dễ dàng làm bài tập trong SBT Hóa học 10 trang 29.
SBT Hóa học 10 trang 29
Bài 10.8 trang 29 SBT Hóa học 10: Trong tự nhiên, các khí hiếm tồn tại dưới dạng nguyên tử tự do. Các nguyên tử của khí hiếm không liên kết với nhau tạo thành phân tử và rất khó liên kết với các nguyên tử của các nguyên tố khác. Ngược lại nguyên tử các nguyên tố khác lại liên kết với nhau tạo thành phân tử hay tinh thể. Giải thích.
Phương pháp giải:
Dựa vào
- Quy tắc octet: Trong quá trình hình thành liên kết hóa học, nguyên tử của các nguyên tố nhóm A có xu hướng tạo thành lớp vỏ ngoài cùng có 8 electron tương ứng với khí hiếm gần nhất (hoặc 2 electron với khí hiếm Helium)
Lời giải:
- Các nguyên tử khí hiếm đều có cấu hình electron bão hòa (đã tuân theo quy tắc octet) => Nguyên tử khí hiếm rất bền vững nên khó tham gia phản ứng hóa học.
- Các nguyên tử của các nguyên tố khác có xu hướng liên kết với nhau để đạt được cấu hình electron bền vững của khí hiếm do chưa có cấu hình electron bão hòa
Bài 10.9 trang 29 SBT Hóa học 10: Cấu hình electron lớp ngoài cùng của nguyên tử potassium (kali) là 4s1, cấu hình electron lớp ngoài cùng của nguyên tử bromine là 4s24p5. Làm thể nào các nguyên tử potassium và bromine có được cấu hình electron của nguyên tử khí hiếm theo quy tắc octet.
Phương pháp giải:
Để có được cấu hình electron của nguyên tử khí hiếm theo quy tắc octet
- Nguyên tố kim loại nhóm A có x electron ở lớp ngoài cùng sẽ nhường đi x electron
- Nguyên tố phi kim có x electron ở lớp ngoài cùng sẽ nhận thêm (8-x) electron
Lời giải:
- Nguyên tử potassium sẽ nhường 1 electron: K => K+ + 1e để có cấu hình electron giống với khí hiếm argon (3s23p6)
- Nguyên tử bromine sẽ nhận 1 electron: Br + 1e => Br- để có cấu hình electron giống với khí hiếm krypton (4s24p6)
Bài 10.10 trang 29 SBT Hóa học 10: Khi hình thành liên kết H + Cl → HCl và khi phá vỡ liên kết HCl → H + Cl thì hệ thu năng lượng hay toả năng lượng. Năng lượng phân tử HCl lớn hơn hay nhỏ hơn năng lượng hệ hai nguyên tử H và Cl riêng rẽ? Trong hai hệ đó thì hệ nào bền hơn?
Phương pháp giải:
Dựa vào
- Khi tạo thành 1 liên kết thì hệ tỏa năng lượng
- Khi phá vỡ 1 liên kết thì hệ thu năng lượng
Lời giải:
- Khi hình thành liên kết H + Cl → HCl thì hệ tỏa năng lượng và khi phá vỡ liên kết HCl → H + Cl thì hệ thu năng lượng
- Năng lượng phân tử HCl nhỏ hơn năng lượng hệ hai nguyên tử H và Cl riêng rẽ
=> Vậy nên hệ HCl bền hơn hệ H và Cl
Bài 10.11 trang 29 SBT Hóa học 10: Trong phân tử Na2S, cấu hình electron của các nguyên tử có tuân theo quy tắc octet không?
Phương pháp giải:
Dựa vào
- Quy tắc octet: Trong quá trình hình thành liên kết hóa học, nguyên tử của các nguyên tố nhóm A có xu hướng tạo thành lớp vỏ ngoài cùng có 8 electron tương ứng với khí hiếm gần nhất (hoặc 2 electron với khí hiếm Helium)
- Các bước thực hiện:
+ Bước 1: Viết cấu hình electron của các nguyên tử
+ Bước 2: Xác định số electron lớp ngoài cùng của các nguyên tử
+ Bước 3: Viết sự hình thành liên kết trong các phân tử
+ Bước 4: Xác định sự thỏa mãn quy tắc octet
Lời giải:
|
|
Phân tử Na2S |
|
- Bước 1: Viết cấu hình electron của các nguyên tử |
- Cấu hình electron của Na: 1s22s22p63s1 - Cấu hình electron của S: 1s22s22p63s23p4 |
|
- Bước 2: Xác định số electron lớp ngoài cùng của các nguyên tử |
- Na có 1 electron lớp ngoài cùng - S có 6 electron lớp ngoài cùng |
|
- Bước 3: Viết sự hình thành liên kết trong các phân tử |
2Na -> 2Na+ + 2.1e S + 2e -> S2- 2Na+ + S2- -> Na2S |
|
- Bước 4: Xác định sự thỏa mãn quy tắc octet |
- Nguyên tử Na sau khi nhường 1 electron và nguyên tử S sau khi nhận 2 electron đều có cấu hình electron lớp ngoài cùng có 8 electron -> Phù hợp với quy tắc octet |
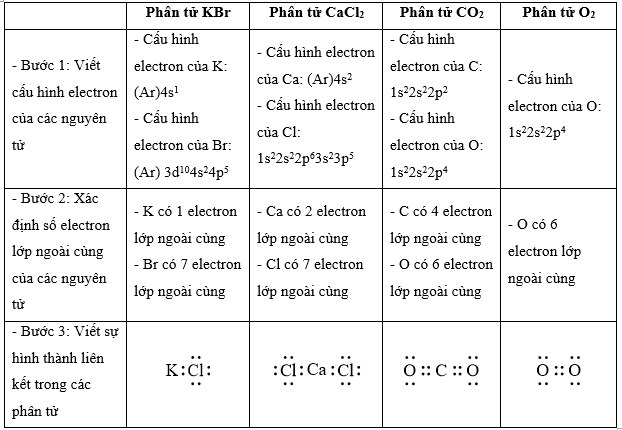
Bài 10.12 trang 29 SBT Hóa học 10: Vận dụng quy tắc octet để giải thích sự hình thành liên kết trong các phân tử O2, CO2, CaCl2, KBr.
Phương pháp giải:
Dựa vào
- Quy tắc octet: Trong quá trình hình thành liên kết hóa học, nguyên tử của các nguyên tố nhóm A có xu hướng tạo thành lớp vỏ ngoài cùng có 8 electron tương ứng với khí hiếm gần nhất (hoặc 2 electron với khí hiếm Helium)
- Các bước thực hiện:
+ Bước 1: Viết cấu hình electron của các nguyên tử
+ Bước 2: Xác định số electron lớp ngoài cùng của các nguyên tử
+ Bước 3: Viết sự hình thành liên kết trong các phân tử
Lời giải:
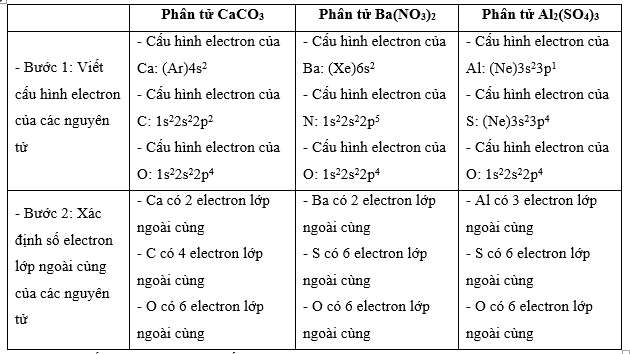
Bài 10.13 trang 29 SBT Hóa học 10: Đá vôi (thành phần chính là CaCO3) được dùng để sản xuất vôi, trong lĩnh vực xây dựng... Barium nitrate Ba(NO3)2 có trong thành phần của kính quang học, gốm, men,… Phèn đơn aluminium sulfate (thành phần chính là Al2(SO4)3) được sử dụng rộng rãi trong xử lí nước thải, trong công nghệ sản xuất giấy, công nghệ nhuộm vải và công nghệ lọc nước và nuôi trồng thuỷ sản,... Dựa vào tắc octet, đề xuất công thức cấu tạo của các chất trên.
Phương pháp giải:
Dựa vào
- Quy tắc octet: Trong quá trình hình thành liên kết hóa học, nguyên tử của các nguyên tố nhóm A có xu hướng tạo thành lớp vỏ ngoài cùng có 8 electron tương ứng với khí hiếm gần nhất (hoặc 2 electron với khí hiếm Helium)
- Các bước thực hiện:
+ Bước 1: Viết cấu hình electron của các nguyên tử
+ Bước 2: Xác định số electron lớp ngoài cùng của các nguyên tử
+ Bước 3: Viết sự hình thành liên kết trong các phân tử
Lời giải:
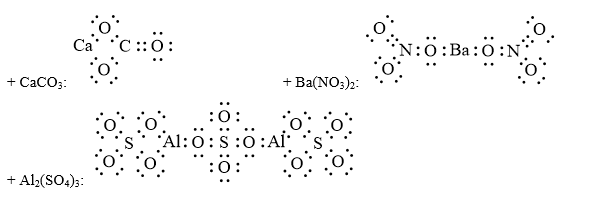
- Bước 3: Viết sự hình thành liên kết trong các phân tử
Bài 10.14 trang 29 SBT Hóa học 10: Hợp chất X tạo bởi hai nguyên tố A, D có khối lượng phân tử là 76. X là dung môi không phân cực, thưởng được sử dụng làm nguyên liệu trong tổng hợp chất hữu cơ chứa lưu huỳnh và được sử dụng rộng rãi trong sản xuất vải viscoza mềm. A có công thức hydride dạng AH4 và D có công thức oxide ứng với hoá trị cao nhất dạng DO3.
a) Hãy thiết lập công thức phân tử của X. Biết rằng A có số oxi hoá cao nhất trong X.
b) Để xuất công thức cấu tạo của X và cho biết các nguyên tử thành phần của X khi liên kết có đủ electron theo quy tắc octet không.
Phương pháp giải:
Dựa vào
- Công thức oxide cao nhất và hợp chất khí với hydrogen của các nguyên tố từ IA đến VIIA
|
Nhóm |
IA |
IIA |
IIIA |
IVA |
VA |
VIA |
VIIA |
|
Công thức oxide cao nhất |
R2O |
RO |
R2O3 |
RO2 |
R2O5 |
RO3 |
R2O7 |
|
Hợp chất khí với hydrogen |
|
|
|
RH4 |
RH3 |
H2R |
HR |
- Các bước thực hiện:
+ Bước 1: Viết cấu hình electron của các nguyên tử
+ Bước 2: Xác định số electron lớp ngoài cùng của các nguyên tử
+ Bước 3: Viết sự hình thành liên kết trong các phân tử
+ Bước 4: Kiểm tra
Lời giải:
- A có công thức hydride dạng AH4 => A thuộc nhóm IVA (1)
- D có công thức oxide ứng với hoá trị cao nhất dạng DO3 => D thuộc nhóm VIA (2)
=> Công thức của X ó dạng: AD2
- Có MX = 76 = MA + 2.MD
=> Nguyên tử khối trung bình của A và D là: (3)
- Từ (1), (2) và (3) => A là Carbon (C) và D là Sulfur (S)
b)
|
|
Phân tử CS2 |
|
- Bước 1: Viết cấu hình electron của các nguyên tử |
- Cấu hình electron của C: 1s22s22p2 - Cấu hình electron của S: 1s22s22p63s23p4 |
|
- Bước 2: Xác định số electron lớp ngoài cùng của các nguyên tử |
- C có 4 electron lớp ngoài cùng - S có 6 electron lớp ngoài cùng |
|
- Bước 3: Viết sự hình thành liên kết trong các phân tử |
|
|
- Bước 4: Kiểm tra |
=> Phù hợp với quy tắc octet |
Xem thêm lời giải vở bài tập Hóa học lớp 10 Kết nối tri thức với cuộc sống hay, chi tiết khác:
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.