Với giải Luyện tập trang 32 Hóa học lớp 10 Chân trời sáng tạo chi tiết trong Bài 4: Cấu trúc lớp vỏ electron của nguyên tử giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Hóa học 10. Mời các bạn đón xem:
Viết cấu hình electron nguyên tử của nguyên tố aluminium (Z = 13) và biểu diễn
Luyện tập trang 32 Hoá học 10: Viết cấu hình electron nguyên tử của nguyên tố aluminium (Z = 13) và biểu diễn cấu hình electron của aluminium theo ô orbital. Từ đó, xác định số electron độc thân của nguyên tử này.
Phương pháp giải:
Bước 1: Xác định số electron: 13
Bước 2: Viết thứ tự các lớp và phân lớp electron theo chiều tăng dần của năng lượng:
1s 2s 2p 3s 3p 4s 3d 4p
Bước 3: Điền các electron vào các phân lớp theo nguyên lí vững bền cho đến electron cuối cùng
Lời giải:
- Nguyên tử có Z = 13 => Có 13 electron
- Viết theo thứ tự: 1s 2s 2p 3s 3p 4s 3d… (trong đó phân lớp s chứa tối ta 2 electron, phân lớp p chứa tối đa 6 electron, phân lớp d chứa tối đa 10 electron, phân lớp f chứa tối đa 14 electron)
- Điền các electron: 1s22s22p63s23p1
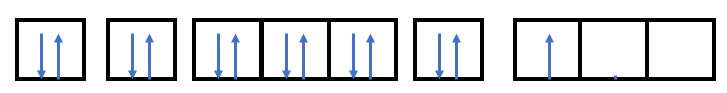
=> Nguyên tử aluminium có 1 electron độc thân
Xem thêm các bài giải Hóa học lớp 10 Chân trời sáng tạo hay, chi tiết khác:
Câu hỏi mở đầu trang 26 Hoá học 10: Trong nguyên tử, các electron chuyển động như thế nào và chiếm những mức năng lượng nào?...
Câu hỏi 1 trang 26 Hoá học 10: Quan sát Hình 4.1 và 4.2, so sánh điểm giống nhau và khác nhau giữa mô hình Rutherford – Bohr...
Câu hỏi 2 trang 27 Hoá học 10: Quan sát Hình 4.3, phân biệt khái niệm đám mây electron và khái niệm orbital nguyên tử...
Câu hỏi 3 trang 27 Hoá học 10: Cho biết khái niệm orbital nguyên tử xuất phát từ mô hình nguyên tử của Rutherford – Bohr hay mô hình nguyên tử hiện đại...
Câu hỏi 4 trang 27 Hoá học 10: Quan sát Hình 4.4, hãy cho biết điểm giống và khác nhau giữa các orbital p (px, py, pz)...
Vận dụng trang 27 Hoá học 10: Hệ Mặt Trời gồm Mặt Trời ở trung tâm và các thiên thể quay quanh theo những quỹ đạo xác định...
Câu hỏi 5 trang 28 Hoá học 10: Quan sát Hình 4.5, nhận xét cách gọi tên các lớp electron bằng các chữ cái tương ứng với các lớp từ 1 đến 7...
Câu hỏi 6 trang 28 Hoá học 10: Từ Hình 4.5, cho biết lực hút của hạt nhân với electron ở lớp nào là lớn nhất và lớp nào là nhỏ nhất...
Câu hỏi 7 trang 28 Hoá học 10: Quan sát Hình 4.6, nhận xét về số lượng phân lớp trong các các lớp từ 1 đến 4...
Câu hỏi 8 trang 29 Hoá học 10: Quan sát Hình 4.7, nhận xét chiều tăng năng lượng của các electron trên các AO ở trạng thái cơ bản (trạng thái có năng lượng thấp nhất)...
Câu hỏi 9 trang 30 Hoá học 10: Quan sát Hình 4.8, cho biết cách biểu diễn 2 electron trong một orbital dựa trên cơ sở nào...
Câu hỏi 10 trang 30 Hoá học 10: Quan sát Hình 4.9, hãy cho biết nguyên tử oxygen có bao nhiêu electron ghép đôi và bao nhiêu electron độc thân...
Câu hỏi 11 trang 31 Hoá học 10: Từ Bảng 4.1, hãy chỉ ra mối quan hệ giữa số thứ tự lớp và số electron tối đa trong mỗi lớp...
Câu hỏi 12 trang 31 Hoá học 10: Quan sát Hình 4.10, hãy nhận xét số lượng electron độc thân ở mỗi trường hợp...
Câu hỏi 13 trang 31 Hoá học 10: Hãy đề nghị cách phân bố electron vào các orbital để số electron độc thân là tối đa...
Luyện tập 1 trang 31 Hoá học 10: Nguyên tử nitrogen có 2 lớp electron trong đó có 2 phân lớp s và 1 phân lớp p. Các phân lớp s đều chứa số electron tối đa...
Luyện tập 2 trang 31 Hoá học 10: Trong các trường hợp (a) và (b) dưới đây, trường hợp nào có sự phân bố electron vào các orbital tuân theo và không tuân theo quy tắc Hund...
Câu hỏi 14 trang 32 Hoá học 10: Cấu hình electron của một nguyên tử cho biết những thông tin gì?...
Câu hỏi 15 trang 33 Hoá học 10: Quan sát Bảng 4.2, hãy cho biết dựa trên cơ sở nào để dự đoán phosphorus là nguyên tố phi kim...
Vận dụng trang 33 Hoá học 10: Lithium là một nguyên tố có nhiều công dụng, được sử dụng trong chế tạo máy bay và trong một số loại pin nhất định...
Bài tập 1 trang 34 Hoá học 10: Trong các cách biểu diễn electron và các orbital của phân lớp 2p ở trạng thái cơ bản, hãy chọn cách phân bố đúng...
Bài tập 2 trang 34 Hoá học 10: Cho nguyên tố X có 2 lớp electron, lớp thứ 2 có 6 electron. Xác định số hiệu nguyên tử của X...
Bài tập 3 trang 34 Hoá học 10: Ở trạng thái cơ bản, nguyên tử của những nguyên tố nào dưới đây có electron độc thân?...
Bài tập 4 trang 34 Hoá học 10: Viết cấu hình electron nguyên tử của các nguyên tố: carbon (Z = 6), sodium (Z = 11) và oxygen (Z = 8)....
Xem thêm các bài giải Hóa học lớp 10 Chân trời sáng tạo hay, chi tiết khác:
Câu hỏi mở đầu trang 26 Hoá học 10: Trong nguyên tử, các electron chuyển động như thế nào và chiếm những mức năng lượng nào?...
Câu hỏi 1 trang 26 Hoá học 10: Quan sát Hình 4.1 và 4.2, so sánh điểm giống nhau và khác nhau giữa mô hình Rutherford – Bohr...
Câu hỏi 2 trang 27 Hoá học 10: Quan sát Hình 4.3, phân biệt khái niệm đám mây electron và khái niệm orbital nguyên tử...
Câu hỏi 3 trang 27 Hoá học 10: Cho biết khái niệm orbital nguyên tử xuất phát từ mô hình nguyên tử của Rutherford – Bohr hay mô hình nguyên tử hiện đại...
Câu hỏi 4 trang 27 Hoá học 10: Quan sát Hình 4.4, hãy cho biết điểm giống và khác nhau giữa các orbital p (px, py, pz)...
Vận dụng trang 27 Hoá học 10: Hệ Mặt Trời gồm Mặt Trời ở trung tâm và các thiên thể quay quanh theo những quỹ đạo xác định...
Câu hỏi 5 trang 28 Hoá học 10: Quan sát Hình 4.5, nhận xét cách gọi tên các lớp electron bằng các chữ cái tương ứng với các lớp từ 1 đến 7...
Câu hỏi 6 trang 28 Hoá học 10: Từ Hình 4.5, cho biết lực hút của hạt nhân với electron ở lớp nào là lớn nhất và lớp nào là nhỏ nhất...
Câu hỏi 7 trang 28 Hoá học 10: Quan sát Hình 4.6, nhận xét về số lượng phân lớp trong các các lớp từ 1 đến 4...
Câu hỏi 8 trang 29 Hoá học 10: Quan sát Hình 4.7, nhận xét chiều tăng năng lượng của các electron trên các AO ở trạng thái cơ bản (trạng thái có năng lượng thấp nhất)...
Câu hỏi 9 trang 30 Hoá học 10: Quan sát Hình 4.8, cho biết cách biểu diễn 2 electron trong một orbital dựa trên cơ sở nào...
Câu hỏi 10 trang 30 Hoá học 10: Quan sát Hình 4.9, hãy cho biết nguyên tử oxygen có bao nhiêu electron ghép đôi và bao nhiêu electron độc thân...
Câu hỏi 11 trang 31 Hoá học 10: Từ Bảng 4.1, hãy chỉ ra mối quan hệ giữa số thứ tự lớp và số electron tối đa trong mỗi lớp...
Câu hỏi 12 trang 31 Hoá học 10: Quan sát Hình 4.10, hãy nhận xét số lượng electron độc thân ở mỗi trường hợp...
Câu hỏi 13 trang 31 Hoá học 10: Hãy đề nghị cách phân bố electron vào các orbital để số electron độc thân là tối đa...
Luyện tập 1 trang 31 Hoá học 10: Nguyên tử nitrogen có 2 lớp electron trong đó có 2 phân lớp s và 1 phân lớp p. Các phân lớp s đều chứa số electron tối đa...
Luyện tập 2 trang 31 Hoá học 10: Trong các trường hợp (a) và (b) dưới đây, trường hợp nào có sự phân bố electron vào các orbital tuân theo và không tuân theo quy tắc Hund...
Câu hỏi 14 trang 32 Hoá học 10: Cấu hình electron của một nguyên tử cho biết những thông tin gì?...
Luyện tập trang 32 Hoá học 10: Viết cấu hình electron nguyên tử của nguyên tố aluminium (Z = 13) và biểu diễn cấu hình electron của aluminium theo ô orbital...
Câu hỏi 15 trang 33 Hoá học 10: Quan sát Bảng 4.2, hãy cho biết dựa trên cơ sở nào để dự đoán phosphorus là nguyên tố phi kim...
Vận dụng trang 33 Hoá học 10: Lithium là một nguyên tố có nhiều công dụng, được sử dụng trong chế tạo máy bay và trong một số loại pin nhất định...
Bài tập 1 trang 34 Hoá học 10: Trong các cách biểu diễn electron và các orbital của phân lớp 2p ở trạng thái cơ bản, hãy chọn cách phân bố đúng...
Bài tập 2 trang 34 Hoá học 10: Cho nguyên tố X có 2 lớp electron, lớp thứ 2 có 6 electron. Xác định số hiệu nguyên tử của X...
Bài tập 3 trang 34 Hoá học 10: Ở trạng thái cơ bản, nguyên tử của những nguyên tố nào dưới đây có electron độc thân?...
Bài tập 4 trang 34 Hoá học 10: Viết cấu hình electron nguyên tử của các nguyên tố: carbon (Z = 6), sodium (Z = 11) và oxygen (Z = 8)....
Xem thêm các bài giải SGK Hoá học lớp 10 Chân trời sáng tạo hay, chi tiết khác:
Bài 3: Nguyên tố hoá học
Bài 5: Cấu tạo bảng tuần hoàn các nguyên tố hoá học
Bài 6: Xu hướng biến đổi một số tính chất của nguyên tử các nguyên tố, thành phần và một số tính chất của hợp chất trong một chu kì và nhóm
Bài 7: Định luật tuần hoàn - Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học
Bài 8: Quy tắc octet
