Với giải Câu hỏi trang 115 SGK Hoá học10 Chân trời sáng tạo trong Bài 18: Hydrogen halide và một số phản ứng của ion halide giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Hoá học 10. Mời các bạn đón xem:
Hoá học 10 Chân trời sáng tạo trang 115 Bài 18: Hydrogen halide và một số phản ứng của ion halide
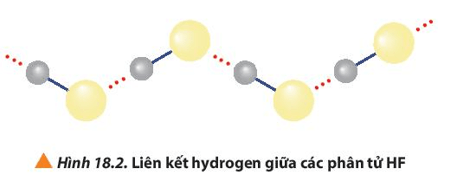
Lời giải:
Các phân tử hydrogen fluoride hình thành liên kết hydrogen liên phân tử, loại liên kết này bền hơn tương tác van der Waals, nên nhiệt độ sôi của hydrogen flouride cao bất thường so với các hydrogen halide còn lại.
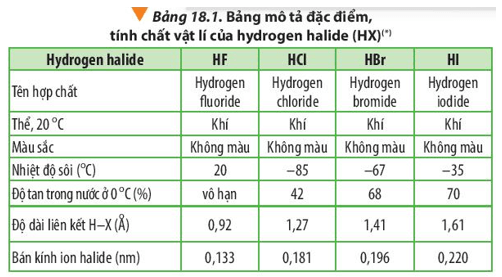
Lời giải:
Fluorine là nguyên tố có độ âm điện lớn nhất ⇒ Liên kết H-F phân cực mạnh nhất ⇒ Tạo liên kết hydrogen bền với các phân tử H2O ⇒ hydrogen fluoride (HF) tan vô hạn trong nước.
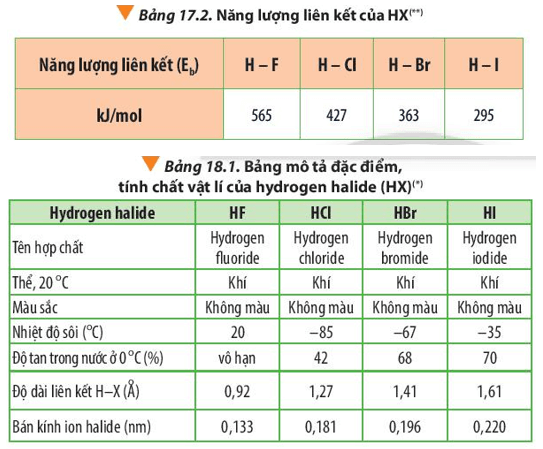
Lời giải:
Năng lượng liên kết nhỏ + độ dài liên kết lớn ⇒ Liên kết H-X dễ dàng bị phá vỡ ⇒ Nguyên tử H càng linh động hay càng dễ phân ly ra H+ ⇒ Tính acid càng mạnh.
Năng lượng liên kết H-X giảm dần từ HF đến HI. Đồng thời độ dài liên kết cũng giảm dần từ HF đến HI ⇒ Tính acid tăng dần từ HF đến HI
Luyện tập trang 115 Hóa học 10: Hoàn thành phương trình hóa học của các phản ứng sau:
(1) NaOH + HCl →
(2) Zn + HCl →
(3) CaO + HBr →
(4) K2CO3 + HI →
Lời giải:
(1) NaOH + HCl → NaCl + H2O
(2) Zn + 2HCl → ZnCl2 + H2
(3) CaO + 2HBr → CaBr2 + H2O
(4) K2CO3 + 2HI → 2KI + H2O + CO2
Xem thêm các bài giải Hóa học lớp 10 Chân trời sáng tạo hay, chi tiết khác:
Mở đầu trang 114 Hóa học 10: Thủy tinh vốn cứng, trơn và khá trơ về mặt hóa học nên việc chạm khắc là điều không đơn giản...
Luyện tập trang 115 Hóa học 10: Hoàn thành phương trình hóa học của các phản ứng sau...
Vận dụng trang 116 Hóa học 10: Em hãy đề xuất cách bảo quản hydrofluoric aicd trong phòng thí nghiệm...
Câu hỏi 5 trang 116 Hóa học 10: Viết quá trình các ion halide bị oxi hóa thành đơn chất tương ứng...
Luyện tập trang 116 Hóa học 10: Phản ứng nào dưới đây chứng minh tính khử của các ion halide...
Câu hỏi 7 trang 118 Hóa học 10: Tìm những ứng dụng khác của hydrogen halide trong đời sống, sản xuất...
Bài 1 trang 119 Hóa học 10: Viết phương trình hóa học của phản ứng xảy ra trong các trường hợp...
Xem thêm các bài giải SGK Hoá học lớp 10 Chân trời sáng tạo hay, chi tiết khác:
Bài 17: Tính chất vật lí và hóa học các đơn chất nhóm VIIA
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.