Với giải Câu hỏi trang 71 SGK Hoá học10 Cánh Diều Bài 13: Phản ứng oxi hoá - khử giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Hoá học 10. Mời các bạn đón xem:
Hoá học 10 Cánh Diều trang 71 Bài 13: Phản ứng oxi hoá - khử
Lời giải:
Al2O3; CaF2 là các hợp chất ion.
: Số oxi hóa của Al là +3, của O là -2.
: Số oxi hóa của Ca là +2, của F là -1.
Luyện tập 2 trang 71 Hóa học 10: Xác định số oxi hóa của mỗi nguyên tử trong hợp chất sau: NO, CH4.
Lời giải:
NO: Giả định là hợp chất ion, hai cặp electron sẽ lệch hoàn toàn về phía nguyên tử O (có độ âm điện cao hơn), trong liên kết đôi có hai electron của N bị chuyển sang O nên hợp chất ion giả định là N2+=O2-
Vậy số oxi hóa của N là +2, O là -2
CH4 gồm 1 nguyên tử C liên kết đơn với 4 nguyên tử H
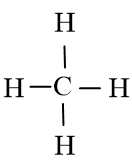
Giả định CH4 là hợp chất ion, cặp electron lệch hoàn toàn về phía nguyên tử C (có độ âm điện cao hơn), trong mỗi liên kết đơn C-H có một electron của H bị chuyển sang C nên hợp chất ion giả định là
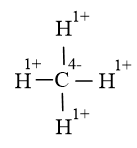
Vậy số oxi hóa của H là +1, C là -4
Lời giải:
- Nguyên tử O có 6 electron lớp vỏ ngoài cùng, theo quy tắc octet nguyên tử O có xu hướng nhận thêm 2 electron để đạt được cấu hình bền vững giống như khí hiếm và trở thành ion mang điện tích -2.
Số oxi hóa của một nguyên tử một nguyên tố trong hợp chất là điện tích của nguyên tử nguyên tố đó với giả định đây là hợp chất ion.
⇒ Số oxi hóa của O trong hợp chất là 2-.
Tương tự như vậy đối với kim loại nhóm IA, IIA và Al.
- Nguyên tử kim loại nhóm IA có 1 electron lớp vỏ ngoài cùng, theo quy tắc octet nguyên tử kim loại nhóm IA có xu hướng nhường đi 1 electron này để đạt được cấu hình bền vững giống như khí hiếm và trở thành ion mang điện tích +1.
⇒ Số oxi hóa của kim loại nhóm IA là 1+.
- Nguyên tử kim loại nhóm IIA có 1 electron lớp vỏ ngoài cùng, theo quy tắc octet nguyên tử kim loại nhóm IIA có xu hướng nhường đi 2 electron này để đạt được cấu hình bền vững giống như khí hiếm và trở thành ion mang điện tích +2.
⇒ Số oxi hóa của kim loại nhóm IIA là 2+.
- Nguyên tử Al có 3 electron lớp vỏ ngoài cùng, theo quy tắc octet nguyên tử Al có xu hướng nhường đi 3 electron này để đạt được cấu hình bền vững giống như khí hiếm và trở thành ion mang điện tích +3.
⇒ Số oxi hóa của Al là 3+.
Xem thêm các bài giải Hóa học lớp 10 Cánh Diều hay, chi tiết khác:
Luyện tập 2 trang 71 Hóa học 10: Xác định số oxi hóa của mỗi nguyên tử trong hợp chất sau: NO, CH4...
Luyện tập 5 trang 72 Hóa học 10: Xác định số oxi hóa của mỗi nguyên tử trong NH3 theo cách 2...
Câu hỏi 4 trang 73 Hóa học 10: Nguyên tố Cl thể hiện bao nhiêu số oxi hóa trong phản ứng (3)?...
Bài 1 trang 76 Hóa học 10: Xác định số oxi hóa của mỗi nguyên tử trong phân tử và ion sau đây...
Xem thêm các bài giải Hoá học lớp 10 Cánh Diều hay, chi tiết khác:
Bài 12: Liên kết hydrogen và tương tác Van Der Waals
Bài 14: Phản ứng hoá học học và enthalpy
Bài 15: Ý nghĩa và cách tính biến thiên enthalpy phản ứng hoá học
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.