Với giải Câu hỏi trang 61 SBT Hoá học10 Kết nối tri thức Bài 19: Tốc độ phản ứng giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập SBT Hoá học 10. Mời các bạn đón xem:
SBT Hoá học 10 Kết nối tri thức trang 61 Bài 19: Tốc độ phản ứng
Bài 19.34 trang 61 SBT Hóa học 10: Xúc tác có hiệu quả cao là xúc tác làm tăng nhanh tốc độ phản ứng. Hai chất MnO2 và Fe2O3 đều có khả năng xúc tác cho phản ứng phân huỷ H2O2. Đo nồng độ H2O2 theo thời gian, thu được đồ thị sau:
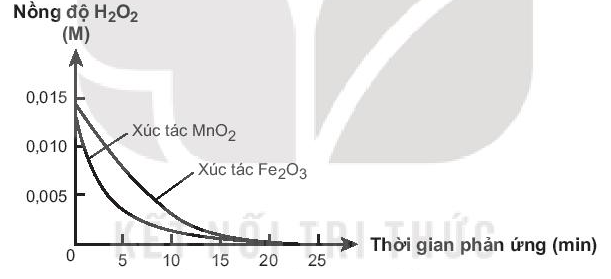
Cho biết xúc tác nào có hiệu quả hơn. Giải thích.
Phương pháp giải:
Dựa vào sự ảnh hưởng của các yếu tố đến tốc độ phản ứng:
- Chất xúc tác làm tăng tốc độ của phản ứng hóa học (cụ thể là làm giảm năng lượng hoạt hóa của phản ứng) nhưng vẫn bảo toàn về chất và lượng khi phản ứng kết thúc
Lời giải:
- Dựa vào đồ thị ta thấy, chất xúc tác MnO2 trong cùng 1 khoảng thời gian khiến cho nồng độ H2O2 giảm xuống nhiều hơn so với chất xúc tác Fe2O3 → Phản ứng diễn ra nhanh hơn → MnO2 là chất xúc tác hiệu quả hơn
Bài 19.35 trang 61 SBT Hóa học 10: Khí oxygen và hydrogen có thể cùng tồn tại trong một bình kín ở điều kiện bình thường mà không nguy hiểm. Nhưng khi có tia lửa điện hoặc một ít bột kim loại được thêm vào bình thì lập tức có phản ứng mãnh liệt xảy ra và có thể gây nổ.
a) Tia lửa điện có phải chất xúc tác không? Giải thích.
b) Bột kim loại có phải chất xúc tác không? Giải thích.
Phương pháp giải:
Dựa vào sự ảnh hưởng của các yếu tố đến tốc độ phản ứng:
- Chất xúc tác làm tăng tốc độ của phản ứng hóa học (cụ thể là làm giảm năng lượng hoạt hóa của phản ứng) nhưng vẫn bảo toàn về chất và lượng khi phản ứng kết thúc
Lời giải:
a) Tia lửa điện không phải chất xúc tác vì chỉ cung cấp năng lượng để H2 và O2 có năng lượng cao hơn mức năng lượng hoạt hóa → phản ứng xảy ra (không làm giảm năng lượng hoạt hóa của phản ứng)
b) Bột kim loại là chất xúc tác vì giúp làm giảm năng lượng hoạt hóa của phản ứng → phản ứng xảy ra
Xem thêm các bài giải SBT Hoá học lớp 10 Kết nối tri thức hay, chi tiết khác:
Bài 19.1 trang 53 SBT Hóa học 10: Cho phản ứng xảy ra trong pha khí sau: H2 + Cl2 -> 2HCl...
Bài 19.3 trang 53 SBT Hóa học 10: Sục khí CO2 vào bình chứa dung dịch Na2CO3...
Bài 19.4 trang 54 SBT Hóa học 10: Cho các phản ứng hoá học sau: a) Fe3O4(s) + 4CO(g) → 3Fe(s) + 4CO2(g)...
Bài 19.6 trang 54 SBT Hóa học 10: Cho phản ứng hoá học xảy ra trong pha khí sau: N2 + 3H2 → 2NH3...
Bài 19.7 trang 54 SBT Hóa học 10: Cho bột magnesium vào nước, phản ứng xảy ra rất chậm....
Bài 19.8 trang 54 SBT Hóa học 10: Cho phản ứng hóa học sau: Zn(s) + H2SO4(aq) → ZnSO4(aq) + H2(g)...
Bài 19.9 trang 54 SBT Hóa học 10: Phát biểu nào sau đây là đúng về xúc tác?...
Bài 19.10 trang 55 SBT Hóa học 10: Cho phản ứng thuỷ phân tinh bột có xúc tác là HCl....
Bài 19.11 trang 55 SBT Hóa học 10: Cho các phản ứng hoá học sau: (1) FeCl3 + 3NaOH → Fe(OH)3 + 3NaCl...
Bài 19.14 trang 55 SBT Hóa học 10: Xét phản ứng: 3O2 → 2O3...
Bài 19.15 trang 55 SBT Hóa học 10: Cho các phản ứng hoá học sau: a) CH3COOC2H5(l) + H2O(l) → CH3COOH(l) + C2H5OH(l)...
Bài 19.17 trang 56 SBT Hóa học 10: Cho phân ứng hóa học sau: H2O2 → H2O + O2...
Bài 19.18 trang 56 SBT Hóa học 10: Cách nào sau đây sẽ làm củ khoai tây chín nhanh nhất?...
Bài 19.25 trang 57 SBT Hóa học 10: Thực hiện phản ứng sau: CaCO3 + 2HCl → CaCl + CO2 + H2O...
Bài 19.26 trang 58 SBT Hóa học 10: Thực hiện phản ứng sau: H2SO4 + Na2S2O3 →Na2SO4 + SO2 + S + H2O...
Bài 19.27 trang 58 SBT Hóa học 10: Đề bài: Xét phản ứng sau: 2ClO2 + 2NaOH → NaClO3 + NaClO2 + H2O...
Bài 19.29 trang 59 SBT Hóa học 10: Thực hiện phản ứng 2ICl + H2 → I2 + 2HCl...
Bài 19.31 trang 60 SBT Hóa học 10: Cho phản ứng hoá học sau: Zn(s) + H2SO4(aq) → ZnSO4(aq) + H2(g)...
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.