Toptailieu biên soạn và giới thiệu tới quý Thầy/Cô bộ Giáo án Hóa học 10 sách Kết nối tri thức chuẩn theo mẫu Bộ GD & ĐT nhằm hỗ trợ quý Thầy/Cô trong quá trình lập kế hoạch giảng dạy và biên soạn giáo án môn Hóa lớp 10. Rất mong nhận được những đóng góp ý kiến và sự đón nhận của quý Thầy/Cô.
Chỉ từ 300k mua trọn bộ Giáo án Hóa 10 Kết nối tri thức bản word chi tiết, trình bày đẹp mắt, dễ dàng chỉnh sửa:
B1: Gửi phí vào tài khoản 01113002558311 - NGUYEN THANH TUYEN - Ngân hàng Vietcombank
B2: Nhắn tin tới zalo Vietjack Official - nhấn vào đây để thông báo và nhận giáo án.
Xem thử tài liệu tại đây: Link tài liệu
Giáo án Hóa học 10 (Kết nối tri thức 2023) Bài 12: Liên kết cộng hóa trị
I. MỤC TIÊU
1. Kiến thức
- Trình bày được khái niệm và lấy được ví dụ về liên kết cộng hóa trị (liên kết đơn, đôi, ba) khi áp dụng quy tắc octet.
- Viết được công thức Lewis của một số chất đơn giản.
- Trình bày được khái niệm về liên kết cho - nhận
- Phân biệt được các loại liên kết (liên kết cộng hóa trị không phân cực, liên kết cộng hóa trị phân cực, liên kết ion) dựa theo độ âm điện.
- Giải thích được sự hình thành liên kết σ và liên kết π qua sự xen phủ AO.
- Trình bày được khái niệm năng lượng liên kết (cộng hóa trị).
- Lắp ráp được mô hình một số phân tử có liên kết cộng hóa trị.
2. Năng lực
2.1. Năng lực chung
- Năng lực tự chủ và tự học: Kĩ năng tìm kiếm thông tin trong SGK, quan sát hình ảnh về mô hình phân tử để tìm hiểu về liên kết cộng hóa trị, sự xen phủ các orbital nguyên tử.
- Năng lực giao tiếp và hợp tác: Làm việc nhóm tìm hiểu về sự tạo thành liên kết cộng hóa trị, lắp ráp mô hình phân tử, mô tả liên kết cộng hóa trị bằng sự xen phủ các AO.
- Năng lực giải quyết vấn đề và sáng tạo: Giải thích được tại sao các phân tử có liên kết cộng hóa trị được hình thành bằng sự góp chung electron.
2.2. Năng lực hóa học
a. Nhận thức hoá học: Học sinh đạt được các yêu cầu sau:
Trình bày được:
- Liên kết cộng hóa trị trong các phân tử Cl2, HCl, NH3, O2, CO2, N2…
- Liên kết cho – nhận trong ion NH![]() ; H3O+ …
; H3O+ …
- Mối quan hệ giữa hiệu độ âm điện với liên kết hóa học.
- Mô tả sự xen phủ s – s, s – p, p – p của AO.
- Năng lượng liên kết đặc trưng cho độ bền liên kết.
b. Tìm hiểu tự nhiên dưới góc độ hóa học được thực hiện thông qua các hoạt động: Thảo luận, tìm hiểu SGK, lắp ráp các mô hình phân tử, cắt dán sự xen phủ AO.
c. Vận dụng kiến thức, kĩ năng đã học để giải thích được tại sao có liên kết đơn, liên kết đôi, liên kết ba, liên kết cho – nhận trong các hợp chất có liên kết cộng hóa trị.
3. Phẩm chất
- Chăm chỉ, tự tìm tòi thông tin trong SGK về sự hình thành liên kết cộng hóa trị.
- HS có trách nhiệm trong việc hoạt động nhóm, hoàn thành các nội dung được giao.
II. THIẾT BỊ DẠY HỌC VÀ HỌC LIỆU
- Hình ảnh, video ...
- Phiếu bài tập số 1, số 2....
III. TIẾN TRÌNH DẠY HỌC
Kiểm tra bài cũ: Không kiểm tra đầu giờ, kiểm tra bài cũ lồng vào trong tiết học.
1. Hoạt động 1: Khởi động
a) Mục tiêu:
Huy động kiến thức đã học của HS, tạo nhu cầu tiếp tục tìm hiểu kiến thức mới.
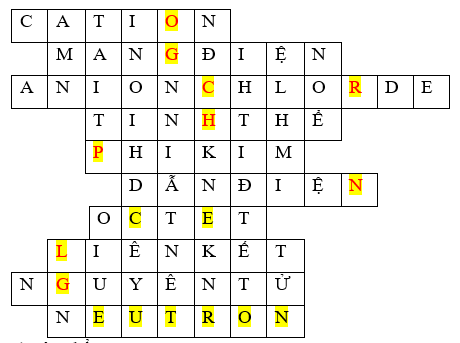
b) Nội dung: GV tổ chức cho HS chơi trò chơi ô chữ. Mỗi ô hàng ngang được lật sẽ chứa các chữ của từ khóa.
Hàng ngang 1: Phần tử mang điện tích dương được gọi là gì? (đáp án: CATION).
Hàng ngang 2: Hoàn thành câu sau: “Khi nguyên tử nhường hay nhận electron thì nguyên tử trở thành phần tử .....” (đáp án: MANG ĐIỆN).
Hàng ngang 3: Ion Cl- có tên gọi là? (đáp án: ANION CHLORIDE).
Hàng ngang 4: Ở điều kiện thường, dạng tồn tại của NaCl là? (đáp án: TINH THỂ).
Hàng ngang 5: Nguyên tử của loại nguyên tố hóa học nào thường có xu hướng nhận electron để tạo thành phần tử mang điện âm ? (đáp án: PHI KIM).
Hàng ngang 6: Dung dịch nóng chảy của hợp chất ion có khả năng gì? (đáp án: DẪN ĐIỆN).
Hàng ngang 7: Quy tắc bát tử còn có tên gọi khác là quy tắc ....? (đáp án: OCTET).
Hàng ngang 8: Sự kết hợp giữa ion Na+ và ion Cl- tạo thành tinh thể NaCl gọi là gì? (đáp án: LIÊN KẾT)
Hàng ngang 9: Hạt vô cùng nhỏ cấu tạo nên chất? (đáp án: NGUYÊN TỬ).
Hàng ngang 10: Trong nguyên tử, hạt không mang điện là? (đáp án: NEUTRON).
Từ khóa : GÓP CHUNG ELECTRON
c) Sản phẩm:
- Câu trả lời của học sinh
d) Tổ chức thực hiện:
- GV gọi HS chọn từ hàng ngang ngẫu nhiên
- Trong mỗi đáp án của từ hàng ngang có chứa chữ cái của từ khóa (được bôi đậm)
- HS có thể trả lời từ khóa khi chưa mở hết các từ hàng ngang
2. Hoạt động 2: Hình thành kiến thức mới
|
Hoạt động 1: Sự hình thành liên kết cộng hóa trị trong đơn chất, hợp chất Mục tiêu: - Trình bày được khái niệm và lấy được ví dụ về liên kết cộng hóa trị (liên kết đơn, đôi, ba) khi áp dụng quy tắc octet. - Viết được công thức Lewis của 1 số chất đơn giản. - Trình bày được khái niệm về liên kết cho – nhận |
|
HOẠT ĐỘNG GV VÀ HS |
SẢN PHẨM DỰ KIẾN |
|
Giao nhiệm vụ học tập: Cách chia nhóm: “Nhóm chuyên gia”: Chia lớp thành 6 nhóm, mỗi nhóm từ 6 đến 8 HS. Trong mỗi nhóm, mỗi thành viên đánh số thứ tự từ 1 đến 6. “Nhóm mảnh ghép”: + Các thành viên có STT 1,2 lập thành nhóm mới. |
Phiếu học tập số 1 Cấu hình electron: |
………………………………………….
………………………………………….
………………………………………….
Trên đây là tóm tắt 3 trang đầu của Giáo án Hóa 10 Bài 12 Kết nối tri thức
Để mua Giáo án Hóa 10 Bài 12 Kết nối tri thức năm 2024 mới nhất, mời Thầy/Cô liên hệ:
Xem thêm Giáo án Hóa 10 Kết nối tri thức hay, chi tiết khác:
Giáo án Hóa học Bài 10: Quy tắc Octet
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.