Toptailieu biên soạn và giới thiệu tới quý Thầy/Cô bộ Giáo án Hóa 10 sách Cánh diều chuẩn theo mẫu Bộ GD & ĐT nhằm hỗ trợ quý Thầy/Cô trong quá trình lập kế hoạch giảng dạy và biên soạn giáo án môn Hóa lớp 10. Rất mong nhận được những đóng góp ý kiến và sự đón nhận của quý Thầy/Cô.
Chỉ 300k mua trọn bộ Giáo án Hóa 10 Cánh diều bản word trình bày đẹp mắt, dễ dàng chỉnh sửa:
B1: Gửi phí vào tài khoản 011110002558311 - NGUYEN THANH TUYEN - Ngân hàng Vietcombank
B2: Nhắn tin tới zalo Vietjack Official - nhấn vào đây để thông báo và nhận giáo án.
Xem thử tài liệu tại đây: Link tài liệu
Giáo án Hóa 10 (Cánh diều 2024) Bài 10: Liên kết ion
I. MỤC TIÊU
1) Kiến thức
Học xong bài này, học sinh có thể:
- Trình bày được khái niệm và sự hình thành liên kết ion (nêu một số ví dụ điển hình tuân theo quy tắc octet).
- Nêu được cấu tạo tinh thể NaCl. Giải thích được vì sao các hợp chất ion thường ở trạng thái rắn trong điều kiện thường (dạng tinh thể ion).
- Lắp được mô hình tinh thể NaCl (theo mô hình có sẵn).
2) Năng lực
a) Năng lực chung
- Năng lực tự chủ và tự học: học sinh xác định đúng đắn động cơ, thái độ học tập, tự đánh giá và điều chỉnh được kế hoạch học tập; tự nhận ra được những sai sót và khắc phục.
- Năng lực giao tiếp: tiếp thu kiến thức, trao đổi học hỏi bạn bè thông qua việc thực hiện nhiệm vụ các hoạt động cặp đôi, nhóm; có thái độ tôn trọng, lắng nghe, có phản ứng tích cực trong giao tiếp.
- Năng lực hợp tác: học sinh xác định được nhiệm vụ của tổ/ nhóm, trách nhiệm của bản thân, đề xuất được những ý kiến đóng góp, góp phần hoàn thành nhiệm vụ học tập.
b) Năng lực chuyên biệt
- Năng lực nhận thức hóa học:
+ Trình bày được khái niệm liên kết ion.
+ Mô tả được sự hình thành liên kết ion, vận dụng vào một số trường hợp cụ thể.
+ Nêu được khái niệm và đặc điểm của tinh thể ion.
+ Lắp ráp được mô hình tinh thể ion.
- Năng lực tìm hiểu thế giới tự nhiên dưới góc độ hóa học: Thông qua các kiến thức đã học kết hợp với thông tin trong SGK, học sinh tự lực thu nhận kiến thức về liên kết ion.
- Năng lực vận dụng kiến thức, kỹ năng đã học:
+ Vận dụng đặc điểm của liên kết ion giải thích được lí do vì sao các hợp chất ion thường là tinh thể rắn ở điều kiện thường, các hợp chất ion có nhiệt độ nóng chảy và nhiệt độ sôi khá cao.
+ Thực hành nuôi cấy được tinh thể muối ăn.
3) Phẩm chất
- Yêu nước: nhận biết được vẻ đẹp của tự nhiên, của đất nước thông qua bộ môn Hóa học.
- Trách nhiệm: nghiêm túc thực hiện các nhiệm vụ học tập được giao đúng tiến độ.
- Trung thực: thành thật trong việc thu thập các tài liệu, viết báo cáo và các bài tập.
- Chăm chỉ: tích cực trong các hoạt động cá nhân, tập thể.
- Nhân ái: quan tâm, giúp đỡ, chia sẻ những khó khăn trong việc thực hiện nhiệm vụ học tập.
II. THIẾT BỊ DẠY HỌC VÀ HỌC LIỆU
- Giáo viên: Sưu tầm hình ảnh, video mô phỏng nội dung có liên quan đến bài học; thiết kế phiếu học tập; dụng cụ lắp ráp mô hình NaCl.
- Học sinh: Ôn tập bài cũ và chuẩn bị bài mới.
III. TIẾN TRÌNH DẠY HỌC
A. HOẠT ĐỘNG KHỞI ĐỘNG
a) Mục tiêu: Tạo tình huống có vấn đề và tâm lý hứng thú cho HS khi bắt đầu bài học mới.
b) Nội dung: GV trình bày vấn đề, HS lắng nghe và trả lời câu hỏi.
c) Sản phẩm:
- Câu trả lời của học sinh:
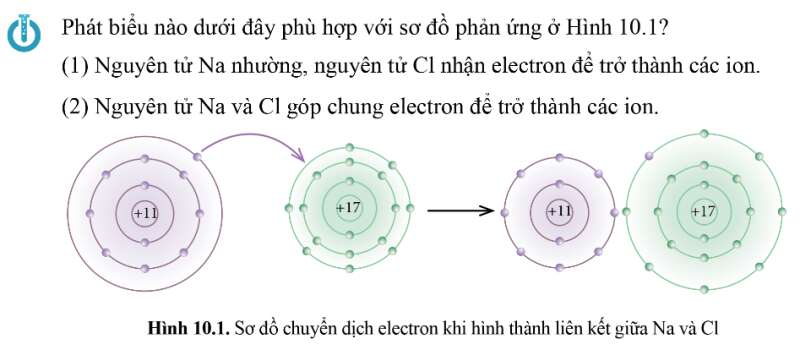
Phát biểu đúng: (1) Nguyên tử Na nhường, nguyên tử Cl nhận electron để trở thành các ion.
Cụ thể theo sơ đồ ta thấy:
+ Nguyên tử Na (Z = 11) nhường đi 1 electron ở lớp ngoài cùng trở thành ion mang điện tích dương, kí hiệu là Na+.
+ Nguyên tử Cl (Z = 17) nhận 1 electron từ nguyên tử Na trở thành ion mang điện tích âm, kí hiệu là Cl-.
Các ion Na+ và Cl- hút nhau tạo thành liên kết trong phân tử NaCl.
- HS biết được những vấn đề liên quan đến bài học mới.
d) Tổ chức thực hiện: GV yêu cầu HS trả lời câu hỏi trong SGK:
B. HOẠT ĐỘNG HÌNH THÀNH KIẾN THỨC MỚI
|
Hoạt động 1: Khái niệm liên kết ion và sự hình thành liên kết ion (18 phút) Mục tiêu: Học sinh nắm được sự hình thành anion, cation từ đó nêu được khái niệm về liên kết ion, sự hình thành liên kết ion. |
|
|
HOẠT ĐỘNG CỦA GV VÀ HS |
SẢN PHẨM DỰ KIẾN |
|
Giao nhiệm vụ học tập: GV sử dụng kĩ thuật mảnh ghép chia lớp thành 4 nhóm thực hiện 3 nhiệm vụ sau: - Nhiệm vụ 1 (4 phút): Tìm hiểu theo nhóm chuyên gia + Nhóm 1, 3: nghiên cứu phiếu học tập nhóm A. + Nhóm 2, 4: nghiên cứu phiếu học tập nhóm B. - Nhiệm vụ 2 (4 phút): Tạo nhóm mảnh ghép (nhóm mới), trao đổi với bạn về kiến thức mình đã tìm hiểu ở nhóm chuyên gia, tiếp nhận và ghi lại kiến thức của bạn. - Nhiệm vụ 3 (5 phút): Cùng nhóm mảnh ghép tìm hiểu kiến thức mới. Thực hiện nhiệm vụ: HS hoàn thành phiếu học tập theo 4 nhóm.
|
Nhóm A 1.1. Nguyên tử F (Z = 9): a) Số electron ở lớp ngoài cùng của nguyên tử F là 7. b) Để đạt được lớp e ngoài cùng bền vững như Ne, nguyên tử F phải nhận 1 thêm electron. c) Sau khi nhận 1 electron, nguyên tử F sẽ trở thành anion F-. Cấu hình electron của ion: 1s22s22p6 1.2. |
………………………………………….
………………………………………….
………………………………………….
Tài liệu có 14 trang, trên đây là tóm tắt 4 trang đầu của Giáo án Hóa 10 Bài 10 Cánh diều.
Để mua Giáo án Hóa 10 Cánh diều năm 2023 mới nhất, mời Thầy/Cô liên hệ
Xem thêm Giáo án Hóa 10 Cánh diều hay, chi tiết khác:
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.