Với giải Bài tập trang 51 Khoa học tự nhiên 7 Chân trời sáng tạo chi tiết trong Bài 7: Hóa trị và công thức hóa học môn Khoa học tự nhiên giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Khoa học tự nhiên 7. Mời các bạn đón xem:
Viết công thức hóa học các hợp chất tạo bởi oxygen và mỗi nguyên tố sau
Bài tập trang 51 KHTN 7
Bài tập 1 trang 51 KHTN 7: Viết công thức hóa học các hợp chất tạo bởi oxygen và mỗi nguyên tố sau: potassium, magnesium, aluminium, phosphorus (hóa trị V)
Phương pháp giải:
Bước 1: Đặt công thức hóa học tổng quát là AxOy
Bước 2: Áp dụng quy tắc hóa trị => Tìm ra giá trị của x và y
Lời giải:
- Xét hợp chất của oxygen và potassium:
+ Gọi công thức phân tử: KxOy (K có hóa trị I, O có hóa trị II)
+ Áp dụng quy tắc hóa trị => I.x = II.y
+ Thường thì tỉ lệ số nguyên tử trong phân tử là những số nguyên đơn giản nhất => x = 2 và y =1
=> Công thức hóa học của hợp chất: K2O
- Xét hợp chất của oxygen và magnesium:
+ Gọi công thức phân tử: MgxOy (Mg có hóa trị II, O có hóa trị II)
+ Áp dụng quy tắc hóa trị => II.x = II.y
+ Thường thì tỉ lệ số nguyên tử trong phân tử là những số nguyên đơn giản nhất => x = 1 và y =1
=> Công thức hóa học của hợp chất: MgO
- Xét hợp chất của oxygen và aluminium:
+ Gọi công thức phân tử: AlxOy (Al có hóa trị III, O có hóa trị II)
+ Áp dụng quy tắc hóa trị => III.x = II.y
+ Thường thì tỉ lệ số nguyên tử trong phân tử là những số nguyên đơn giản nhất => x = 2 và y =3
=> Công thức hóa học của hợp chất: Al2O3
- Xét hợp chất của oxygen và phosphorus:
+ Gọi công thức phân tử: PxOy (P có hóa trị V, O có hóa trị II)
+ Áp dụng quy tắc hóa trị => V.x = II.y
+ Thường thì tỉ lệ số nguyên tử trong phân tử là những số nguyên đơn giản nhất => x = 2 và y =5
=> Công thức hóa học của hợp chất: P2O5
Bài tập 2 trang 51 KHTN 7: Dựa vào bảng hóa trị ở Phụ lục trang 187, em hãy hoàn thành bảng sau:
Phương pháp giải:
- Công thức hóa học: Áp dụng quy tắc hóa trị
- Khối lượng phân tử = tổng khối lượng các nguyên tử tạo nên phân tử đó
Lời giải:
- Xét phân tử sodium sulfide: NaxSy (Na hóa trị I, S hóa trị II)
+ Áp dụng quy tắc hóa trị => I.x = II.y
+ Thường thì tỉ lệ số nguyên tử trong phân tử là những số nguyên đơn giản nhất => x = 2 và y =1
=> Công thức hóa học của hợp chất: Na2S
=> Khối lượng phân tử = 23 x 2 + 32.1 = 78 amu
- Xét phân tử Aluminium nitride: AlxNy (Al hóa trị III, N hóa trị III)
+ Áp dụng quy tắc hóa trị => III.x = III.y
+ Thường thì tỉ lệ số nguyên tử trong phân tử là những số nguyên đơn giản nhất => x = 1 và y =1
=> Công thức hóa học của hợp chất: AlN
=> Khối lượng phân tử = 27 x 1 + 14 x 1 = 41 amu
- Xét phân tử Copper (II) sulfate: CuxSy (Cu hóa trị II, S hóa trị II)
+ Áp dụng quy tắc hóa trị => II.x = II.y
+ Thường thì tỉ lệ số nguyên tử trong phân tử là những số nguyên đơn giản nhất => x = 1 và y =1
=> Công thức hóa học của hợp chất: CuS
=> Khối lượng phân tử = 64 x 1 + 32 x 1 = 96 amu
- Xét phân tử Iron(III) hydroxide: Fex(OH)y (Fe hóa trị III, OH hóa trị I)
+ Áp dụng quy tắc hóa trị => III.x = I.y
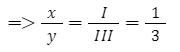
+ Thường thì tỉ lệ số nguyên tử trong phân tử là những số nguyên đơn giản nhất => x = 1 và y =3
=> Công thức hóa học của hợp chất: Fe(OH)3
=> Khối lượng phân tử = 56x1 + (16x1 + 1x1) x 1 = 107 amu
- Hoàn thành bảng:
Bài tập 3 trang 51 KHTN 7: Thạch nhũ trong hang động có thành phần chính là hợp chất (T). Phân tử (T) có cấu tạo từ nguyên tố calcium, carbon và oxygen với các tỉ lệ phần trăm tương ứng là 40%, 12% và 48%. Khối lượng phân tử (T) là 100 amu. Hãy xác định công thức hóa học của T
Phương pháp giải:
Bước 1: Đặt công thức hóa học cần tìm (công thức tổng quát): CaxCyOz
Bước 2: Lập biểu thức tính phần trăm nguyên tố có trong hợp chất
Bước 3: Xác định số nguyên tử của mỗi nguyên tố và viết công thức hóa học cần tìm
Lời giải:
Xem thêm các bài giải Khoa học tự nhiên 7 Chân trời sáng tạo hay, chi tiết khác:
Câu hỏi thảo luận trang 46 KHTN 7
Câu hỏi thảo luận trang 47 KHTN 7
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.