Với Giải SBT Hóa học 10 trang 17 trong Bài 6: Xu hướng biến đổi một số tính chất của nguyên tử các nguyên tố trong một chu kì và trong một nhóm Sách bài tập Hóa học lớp 10 Kết nối tri thức hay nhất, chi tiết sẽ giúp học sinh dễ dàng làm bài tập trong SBT Hóa học 10 trang 17.
Nội dung bài viết
SBT Hóa học 10 trang 17
Bài 6.15 trang 17 sách bài tập Hóa học 10: Cho các nguyên tố X, Y, Z có số hiệu nguyên tử lần lượt là 6, 9, 14. Thứ tự tính phi kim tăng dần của các nguyên tố đó là
A. X < Z < Y
B. Z < X < Y
C. Z < Y < X
D. Y < X < Z
Lời giải:
Đáp án đúng là: B
Chú ý: Theo chiều tăng dần điện tích hạt nhân nguyên tử:
- Trong một chu kì, tính kim loại giảm dần và tính phi kim tăng dần.
- Trong một nhóm, tính kim loại tăng dần và tính phi kim giảm dần.
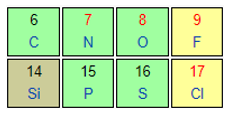
X và Y cùng thuộc một chu kì ⇒ Tính phi kim X < Y
X và Z cùng thuộc một nhóm ⇒ Tính phi kim Z < X
Thứ tự tính phi kim tăng dần của các nguyên tố được sắp xếp là: Z < X < Y
Bài 6.16 trang 17 sách bài tập Hóa học 10: Dãy nguyên tố nào sau đây được xếp theo chiều tăng dần tính phi kim?
A. N, P, As, Bi
B. F, Cl, Br, I
C. C, Si, Ge, Sn
D. Te, Se, S, O
Lời giải:
Đáp án đúng là: D
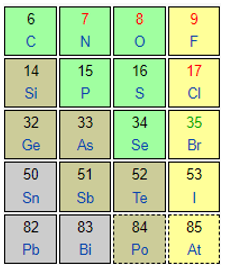
A. N, P, As, Bi thuộc cùng một nhóm.
Tính phi kim tăng dần theo chiều Bi < As < P < N.
⇒ A sai.
B. F, Cl, Br, I thuộc cùng một nhóm.
Tính phi kim tăng dần theo chiều I < Br < Cl < F.
⇒ B sai.
C. C, Si, Ge, Sn thuộc cùng một nhóm.
Tính phi kim tăng dần theo chiều Sn < Ge < Si < C.
⇒ C sai.
D. Te, Se, S, O thuộc cùng một nhóm.
Tính phi kim tăng dần theo chiều Te < Se < S < O
⇒ D đúng.
Bài 6.17 trang 17 sách bài tập Hóa học 10: Trong bảng tuần hoàn, hai nguyên tố X và Y có cùng số thứ tự nhóm. X thuộc nhóm A và Y thuộc nhóm B. So sánh số electron hóa trị và tính chất của X, Y. Minh họa bằng nguyên tố Cl và Mn ở nhóm VII.
Lời giải:
- Sự giống nhau: trong cùng một nhóm, các nguyên tử của nguyên tố nhóm A và B đều có số electron hóa trị bằng nhau nên có hóa trị cao nhất bằng nhau.
- Sự khác nhau: số electron lớp ngoài cùng và cấu hình electron của các nguyên tố nhóm A và B không giống nhau nên tính chất vật lí, hóa học của chúng cũng khác nhau.
Ví dụ: Cấu hình electron: 17Cl: [Ne]3s23p5 (nhóm VIIA) và 25Mn: [Ar]3d54s2 (nhóm VIIB).
+ Cl và Mn đều có 7 electron hóa trị nên đều có hóa trị cao nhất là 7 và số oxi hóa dương cao nhất +7.
+ 7 electron hóa trị của Cl là electron s, p còn 7 electron hóa trị của Mn là electron s, d.
+ Nguyên tử Cl có 7 electron lớp ngoài cùng, nguyên tử Mn chỉ có 2 electron lớp ngoài cùng.
+ Nguyên tố chlorine là phi kim điển hình còn nguyên tố manganese là kim loại chuyển tiếp.
Bài 6.18 trang 17 sách bài tập Hóa học 10: Cho cấu hình electron của nguyên tử hai nguyên tố sau:
X: 1s22s22p63s23p3
Y: 1s22s22p63s23p63d34s2
a) X, Y có ở trong cùng một nhóm nguyên tố không? Giải thích.
b) X, Y cách nhau bao nhiêu nguyên tố hóa học? Có cùng chu kì không?
Lời giải:
a) Nguyên tử X, Y đều có 5 electron hóa trị nên chúng ở cùng nhóm V.
Nguyên tử X có 5 electron lớp ngoài cùng, là nguyên tố p, thuộc nhóm VA.
Nguyên tử Y có 5 electron ở lớp ngoài cùng và sát lớp ngoài cùng, là nguyên tố d, thuộc nhóm VB.
b) X có 15 electron = số hiệu nguyên tử nguyên tố X.
Y có 23 electron = số hiệu nguyên tử nguyên tố Y
⇒ Chúng cách nhau 23 – 15 = 8 nguyên tố.
Nguyên tử X có 3 lớp electron ⇒ thuộc chu kì 3.
Nguyên tử Y có 4 lớp electron ⇒ thuộc chu kì 4.
Bài 6.19 trang 17 sách bài tập Hóa học 10: Cho các nguyên tố sau: K (Z = 19), N (Z = 7), Si (Z = 14), Mg (Z = 12). Hãy sắp xếp các nguyên tố trên theo chiều giảm dần bán kính nguyên tử.
Lời giải:
Liên hệ giữa các nguyên tố đó trong bảng tuần hoàn được mô tả trong bảng sau:
|
7N |
||||
|
12Mg
|
14Si |
|||
|
19K |
Bán kính nguyên tử: K > Mg, Si > N
Theo chu kì, bán kính nguyên tử giảm từ trái qua phải: Mg > Si.
Thứ tự giảm dần bán kính nguyên tử: K > Mg > Si > N.
Bài 6.20 trang 17 sách bài tập Hóa học 10: Cho các nguyên tố X, T, Z và T với số hiệu nguyên tử lần lượt là 9, 17, 33 và 35. Hãy sắp xếp thứ tự tăng dần độ âm điện và giải thích.
Lời giải:
Liên hệ giữa các nguyên tố đó trong bảng tuần hoàn được mô tả trong bảng sau:
|
9X |
||||
|
17Y
|
||||
|
33Z |
35T |
Độ âm điện tăng dần: Z < T < Y < X.
Giải thích: theo nhóm A, độ âm điện giảm dần từ trên xuống dưới nên ta có:
9X > 17Y > 35T.
Theo chu kì, độ âm điện tăng dần từ trái qua phải nên ta có: 33Z < 35T.
Bài 6.21 trang 17 sách bài tập Hóa học 10: Cho các nguyên tố cùng thuộc chu kì 3: 11Na, 13Al và 17Cl và các giá trị độ âm điện là 3,16; 1,61; 0,93. Hãy gán mỗi giá trị độ âm điện cho mỗi nguyên tố và giải thích
Lời giải:
Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân, độ âm điện tăng dần.
Các giá trị độ âm điện tương ứng: 11Na (0,93); 13Al (1,61) và 17Cl (3,16)
Bài 6.22 trang 17 sách bài tập Hóa học 10: Cho các nguyên tố X, Y, Z có số hiệu nguyên tử lần lượt là 6, 9, 14
a) Xác định vị trí của các nguyên tố đó trong bảng tuần hoàn
b) Xếp các nguyên tố đó theo thứ tự bán kính nguyên tử tăng dần.
c) Xếp các nguyên tố đó theo thứ tự độ âm điện giảm dần.
d) Xếp các nguyên tố đó theo thứ tự tính phi kim tăng dần.
Lời giải:
a) Cấu hình electron:
6X: 1s22s22p2
9Y: 1s22s22p5
14Z: 1s22s22p63s23p2
6X và 9Y thuộc chu kì 2 và 14Z thuộc chu kì 3.
9Y thuộc nhóm VIIA, 6X thuộc nhóm IVA, 14Z thuộc nhóm IVA.
b) X và Y cùng thuộc chu kì 2, ZX < ZY
⇒ Bán kính nguyên tử của X > Y.
X và Z cùng thuộc nhóm IVA, ZX < ZZ
⇒ Bán kính nguyên tử Z > X
Vậy bán kính nguyên tử tăng dần là Y < X < Z
c) X và Y cùng thuộc chu kì 2, ZX < ZY
⇒ Độ âm điện của X < Y
X và Z cùng thuộc nhóm IVA, ZX < ZZ
⇒ Độ âm điện của Z < X.
Vậy thứ tự độ âm điện giảm dần là Y > X > Z
d) Thứ tự tính phi kim tăng dần là Z < X < Y.
Bài 6.23 trang 17 sách bài tập Hóa học 10: Cho các nguyên tố X, Y, Z có số hiệu nguyên tử lần lượt là 11, 13, 19
a) Xác định vị trí của các nguyên tố đó trong bảng tuần hoàn.
b) Xếp các nguyên tố đó theo thứ tự bán kính nguyên tử tăng dần.
c) Gán các giá trị độ âm điện (0,82; 1,31 và 0,93) cho X, Y, Z.
d) Xếp các nguyên tố đó theo thứ tự tính kim loại giảm dần.
Lời giải:
a) Cấu hình electron:
11X: 1s22s22p63s1
13Y: 1s22s22p63s23p1
19Z: 1s22s22p63s23p64s1
11X và 13Y thuộc chu kì 3 và 19Z thuộc chu kì 4.
11X thuộc nhóm IA, 13Y thuộc nhóm IIIA và 19Z thuộc nhóm IA.
b) X và Y cùng thuộc chu kì 3, ZX < ZY
⇒ Bán kính nguyên tử của X > Y.
X và X cùng thuộc nhóm IA, ZX < ZZ
⇒ Bán kính nguyên tử Z > X.
Vậy thứ tự bán kính nguyên tử tăng dần là Y < X < Z
c) X và Y cùng thuộc chu kì 3, ZX < ZY
⇒ Độ âm điện của X < Y.
X và Z cùng thuộc nhóm IA, ZX < ZZ
⇒ Độ âm điện của Z < X
Vậy độ âm điện Y (1,31); X (0,93); Z (0,82)
d) Thứ tự tính kim loại giảm dần là Z > X > Y
Bài 6.24 trang 17 sách bài tập Hóa học 10: So sánh tính kim loại của các nguyên tố: Al, Ca, Rb
Lời giải:
Bước 1: Xác định vị trí (chu kì, nhóm) trong bảng tuần hoàn và xếp các nguyên tố vào trong bảng: Al (3, IIIA); Ca (4, IIA); Rb (5, IA).
|
Nhóm Chu kì |
IA |
IIA |
IIIA |
|
3 |
Al |
||
|
4 |
K (*) |
Ca |
Ga (*) |
|
5 |
Rb |
Bước 2: Chọn các nguyên tố trung gian: Ga cùng nhóm với Al và cùng chu kì với Ca; K cùng nhóm với Rb và cùng chu kì với Ca.
Bước 3: Dựa vào xu hướng biến đổi tính kim loại và tính phi kim của các nguyên tố trong chu kì và nhóm A để so sánh tính chất của chúng.
- So sánh Al và Ga: từ trên xuống trong nhóm IIIA, tính kim loại tăng dần
⇒ Tính kim loại Ga > Al.
- So sánh K, Ca và Ga: từ trái qua phải trong chu kì, tính kim loại giảm dần
⇒ Tính kim loại K > Ca > Ga.
- So sánh K và Rb: từ trên xuống trong nhóm IA, tính kim loại tăng dần
⇒ Tính kim loại Rb > k
Vậy tính kim loại Rb > Ca > Al.
Xem thêm lời giải vở bài tập Hóa học lớp 10 Kết nối tri thức với cuộc sống hay, chi tiết khác:
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.