Toptailieu biên soạn và sưu tầm lời giải bài tập Hóa học lớp 10 Bài 14: Ôn tập chương III sách Kết nối tri thức hay, chi tiết sẽ giúp học sinh dễ dàng trả lời câu hỏi Hóa học 10 Bài 14 từ đó học tốt môn Hóa học 10.
Nội dung bài viết
Hoá học 10 Kết nối tri thức Bài 14: Ôn tập chương III
I. Hệ thống hoá kiến thức
II. Luyện tập
Câu 1 trang 69 Hóa học 10: Dãy các chất nào dưới đây mà tất cả các phân tử đều có liên kết ion?
A. Cl2, Br2, I2, HCl.
B. Na2O, KCl, BaCl2, Al2O3.
C. HCl, H2S, NaCl, N2O.
D. MgO, H2SO4, H3PO4, HCl.
Lời giải:
Đáp án B
Các hợp chất ion thường được tạo bởi các kim loại điển hình (IA, IIA) với phi kim điển hình (O, VIIA).
⇒ Na2O, KCl, BaCl2, Al2O3 là các hợp chất ion.
A N2, CO2, Cl2, H2.
B. N2, Cl2, H2, HCl.
C. N2, Hl, Cl2, CH4.
D. Cl2, O2, N2, F2.
Lời giải:
Đáp án D
Liên kết cộng hóa trị không phân cực là loại liên kết trong các đơn chất.
Câu 3 trang 69 Hóa học 10: Viết công thức cấu tạo và công thức Lewis của các phân tử sau PH3, H2O, C2H6. Trong phân tử nào có liên kết phân cực mạnh nhất.
Lời giải:
|
|
Công thức cấu tạo |
Công thức Lewis |
|
PH3 |
|
|
|
H2O |
H – O – H |
|
|
C2H6 |
|
|
- Các nguyên tử O, P, N đều tạo liên kết phân cực với H, trong đó nguyên tử O có độ âm điện lớn hơn cả nên liên kết O – H sẽ phân cực nhất.
⇒ Phân tử H2O có liên kết phân cực mạnh nhất.
Lời giải:
Trong phân tử CH4, hiệu độ âm điện của C và H: 2,55 – 2,2 = 0,35
⇒ Liên kết giữa C và H là liên kết cộng hóa trị không phân cực.
Trong phân tử CaCl2, hiệu độ âm điện của Ca và Cl: 3,16 – 1 = 2,16
⇒ Liên kết giữa Ca và Cl là liên kết ion.
Trong phân tử HBr, hiệu độ âm điện của H và Br: 2,96 – 2,2 = 0,76
⇒ Liên kết giữa H và Br là liên kết cộng hóa trị phân cực.
Trong phân tử NH3, hiệu độ âm điện của N và H: 3,04 – 2,2 = 0,84
⇒ Liên kết giữa N và H là liên kết cộng hóa trị phân cực.
Câu 5 trang 69 Hóa học 10: Cho dãy các oxide sau Na2O, MgO, Al2O3, SiO2, P2O5, SO3, Cl2O7.
a) Độ phân cực của các liên kết trong dãy các oxide trên thay đổi thế nào?
b) Dựa vào giá trị độ âm điện của các nguyên tố trong Bảng 6.2, cho biết loại liên kết (ion, cộng hoá trị phân cực, cộng hóa trị không phân cực) trong từng phân tử oxide.
Lời giải:
a) Độ phân cực trong dãy oxide giảm dần theo chiều từ trái sang phải:
Na2O, MgO, Al2O3, SiO2, P2O5, SO3, Cl2O7
Do hiệu độ âm điện giảm dần.
b) Hiệu độ âm điện của nguyên tố kim loại với oxi là:
Na2O: |∆χNa - O| = 2,51 ⇒ Liên kết giữa Na và O là liên kết ion.
MgO: |∆χMg - O| = 2,13 ⇒ Liên kết giữa Mg và O là liên kết ion.
Al2O3: |∆χAl - O| = 1,83 ⇒ Liên kết giữa Al và O là liên kết ion.
SiO2: |∆χSi - O| = 1,54 ⇒ Liên kết giữa Si và O là liên kết cộng hóa trị có cực
P2O5: |∆χP - O| = 1,25 ⇒ Liên kết giữa P và O là liên kết cộng hóa trị có cực
SO3: |∆χS - O| = 0,86 ⇒ Liên kết giữa S và O là liên kết cộng hóa trị có cực
Cl2O7: |∆χCl - O| = 0,28 ⇒ Liên kết giữa Cl và O là liên kết cộng hóa trị không cực
b) Vẽ sơ đồ biểu diễn liên kết hydrogen giữa các phân tử đó.
Lời giải:
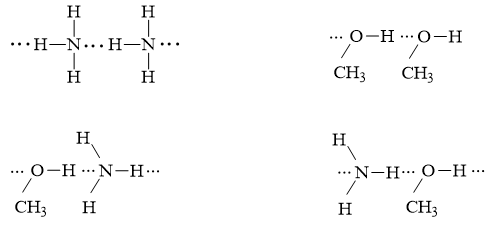
a) Phân tử CH3OH và NH3 có thể tạo liên kết hydrogen vì trong phân tử chứa nguyên tử có độ âm điện lớn (O và N) có cặp electron chưa liên kết và nguyên tử H linh động (có một phần điện tích dương (δ+) đủ lớn để hút cặp electron chưa liên kết của các nguyên tử O, N).
b) Sơ đồ biểu diễn liên kết hydrogen:
Xem thêm các bài giải SGK Hoá học lớp 10 Kết nối tri thức hay, chi tiết khác:
Bài 13: Liên kết hydrogen và tương tác van der Waals
Bài 15: Phản ứng oxi hoá - khử
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.