Toptailieu biên soạn và sưu tầm lời giải bài tập Hóa học lớp 10 Bài 13: Liên kết hydrogen và tương tác van der Waals sách Kết nối tri thức hay, chi tiết sẽ giúp học sinh dễ dàng trả lời câu hỏi Hóa học 10 Bài 13 từ đó học tốt môn Hóa học 10.
Nội dung bài viết
Hoá học 10 Kết nối tri thức Bài 13: Liên kết hydrogen và tương tác van der Waals
Lời giải:
- Các chất trên đều là hợp chất cộng hóa trị phân cực.
- Các tính chất vật lí của các chất có liên kết cộng hóa trị được quyết định bởi lực tương tác giữa các phân tử, hình dạng phân tử và mức độ phân cực của liên kết.
⇒ Các chất khác nhau có nhiệt độ sôi khác nhau.
I. Liên kết hydrogen
Câu hỏi 1 trang 66 Hóa học 10: Vẽ sơ đồ biểu diễn liên kết hydrogen giữa:
a) hai phân tử hydrogen fluoride (HF).
b) phân tử hydrogen fluoride (HF) và phân tử ammonia (NH3).
Lời giải:
a) H – F … H – F.
b)
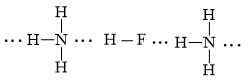
Lời giải:
Những nguyên tử H không gắn nguyên tử O thì không tham gia vào liên kết hydrogen.
Vì để tham gia vào liên kết hydrogen, nguyên tử hydrogen phải liên kết với các nguyên tử có độ âm điện lớn như F, O, N, … và các nguyên tử này phải có ít nhất 1 cặp electron hóa trị chưa tham gia liên kết.
⇒ Chỉ có nguyên tử H gắn vào O trong ethanol tham gia vào liên kết hydrogen.
III. Tương tác Van der waals
Câu hỏi 3 trang 67 Hóa học 10: Hãy giải thích sự khác nhau về nhiệt độ sôi của butane và isobutane.
Lời giải:
Butane và isobutane là hợp chất cộng hóa trị không phân cực và có cùng công thức phân tử là C4H10. Đồng phân butane có nhiệt độ sôi cao hơn isobutane vì diện tích tiếp xúc của các phân tử butane lớn hơn so isobutane.
⇒ Năng lượng để phá vỡ lực liên phân tử giữa các phân tử butane cần nhiều hơn isobutane nên có nhiệt độ sôi cao hơn.
Lời giải:
Để so sánh được tính chất vật lí giữa các phân tử, chúng ta cần nắm được những ý sau:
- Liên kết hydrogen được hình thành giữa nguyên tử H (đã liên kết với một nguyên tử có độ âm điện lớn) với một nguyên tử khác (có độ âm điện lớn) còn cặp electron hóa trị chưa tham gia liên kết.
⇒ Liên kết hydrogen làm tăng nhiệt độ nóng chảy và nhiệt độ sôi của nước.
- Tương tác van der Waals là tương tác tĩnh điện lưỡng cực – lưỡng cực được hình thành giữa các phân tử hay nguyên tử.
⇒ Tương tác van der Waals làm tăng nhiệt độ nóng chảy và nhiệt độ sôi của các chất.
Xem thêm các bài giải SGK Hoá học lớp 10 Kết nối tri thức hay, chi tiết khác:
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.