Toptailieu biên soạn và sưu tầm lời giải bài tập Hóa học lớp 10 Bài 16: Các yếu tố ảnh hướng đến tốc độ phản ứng hoá học sách Chân trời sáng tạo hay, chi tiết sẽ giúp học sinh dễ dàng trả lời câu hỏi Hóa học 10 Bài 16 từ đó học tốt môn Hóa học 10.
Nội dung bài viết
Hoá học 10 Chân trời sáng tạo Bài 16: Các yếu tố ảnh hưởng đến tốc độ phản ứng hoá học
Mở đầu trang 98 Hóa học 10: Thực phẩm bảo quản trong tủ lạnh sẽ giữ được lâu hơn (a), khi nấu một loại thực phẩm bằng nồi áp suất sẽ nhanh chín hơn (b), bệnh nhân sẽ dễ hô hấp hơn khi dùng oxygen từ bình chứa khí oxygen so với từ không khí (c),…

Những yếu tố nào ảnh hưởng đến tốc độ của các quá trình biến đổi trên.
Lời giải:
(a) Thực phẩm bảo quản trong tủ lạnh sẽ giữ được lâu hơn ⇒ Ảnh hưởng của nhiệt độ đến tốc độ phản ứng.
(b) Khi nấu một loại thực phẩm bằng nồi áp suất sẽ nhanh chín hơn ⇒ Ảnh hưởng của áp suất đến tốc độ phản ứng.
(c) Bệnh nhân sẽ dễ hô hấp hơn khi dùng oxygen từ bình chứa khí oxygen so với từ không khí ⇒ Ảnh hưởng của nồng độ đến tốc độ phản ứng.
Thí nghiệm 1: Ảnh hưởng của nồng độ đến tốc độ phản ứng
Hóa chất: Dung dịch sodium thiosulfate (Na2S2O3) 0,15M; sulfuric acid (H2SO4) 0,10M; nước cất.
Dụng cụ: cốc thủy tinh 100 mL (được đánh dấu thập ở mặt ngoài đáy cốc), ống đong 50 mL.
Tiến hành:
Bước 1: Pha loãng dung dịch Na2S2O3 0,15 M để được các dung dịch có nồng độ khác nhau theo Bảng 16.1.
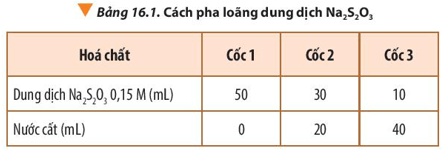
Bước 2: Rót đồng thời 10 mL dung dịch H2SO4 0,1 M vào mỗi cốc và khuấy đều.
Phương trình hóa học của phản ứng:
Na2S2O3(aq) + H2SO4(aq) → Na2SO4(aq) + S(s) + SO2(g) + H2O(l)

Lời giải:
Thể tích dung dịch Na2S2O3 0,15 M càng nhỏ ⇒ Nồng độ Na2S2O3 càng nhỏ (hay dung dịch Na2S2O3 càng loãng) ⇒ Thời gian xuất hiện kết tủa càng lâu.
Na2S2O3(aq) + H2SO4(aq) → Na2SO4(aq) + S(s) + SO2(g) + H2O(l)
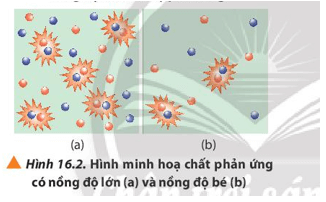
Lời giải:
Nồng độ Na2S2O3 giảm ⇒ Các hạt phân tử Na2S2O3 giảm ⇒ Số va chạm hiệu quả giữa các phân tử Na2S2O3 và phân tử H2SO4 giảm ⇒ Kết tủa tạo thành chậm tức là tốc độ phản ứng chậm hơn.
Luyện tập trang 99 Hóa học 10: Giữ nguyên nồng độ dung dịch Na2S2O3 ban đầu, pha loãng dung dịch H2SO4 tương tự như cách pha loãng dung dịch Na2S2O3 theo Bảng 16.1, kết quả thí nghiệm sẽ thay đổi thế nào?
Lời giải:
Pha loãng dung dịch H2SO4 ⇒ Nồng độ H2SO4 giảm ⇒ Các hạt phân tử H2SO4 giảm ⇒ Số va chạm hiệu quả giữa các phân tử Na2S2O3 và phân tử H2SO4 giảm ⇒ Kết tủa tạo thành chậm tức là tốc độ phản ứng chậm hơn.

Lời giải:
Trong cùng một khoảng thời gian, cốc (1) được đun nóng bị mất màu, cốc (2) không được đun nóng màu chỉ nhạt hơn. Chứng tỏ nhiệt độ cao hơn đã làm phản ứng ở cốc (1) xảy ra nhanh hơn.
Lời giải:
Phương trình hóa học của phản ứng:
2KMnO4(aq) + 5H2C2O4(aq) + 3H2SO4(aq) → 2MnSO4(aq) + K2SO4(aq) + 10CO2(g) + 8H2O(l)
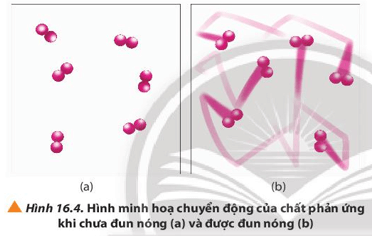
Ở nhiệt độ thường, các chất phản ứng chuyển động với tốc độ nhỏ.
Khi tăng nhiệt độ, các chất sẽ phản ứng với tốc độ lớn hơn, dẫn đến số va chạm hiệu quả tăng nên tốc độ phản ứng tăng.
Luyện tập trang 100 Hóa học 10: Biết rằng, khi nhiệt độ tăng thêm 10oC, tốc độ của một phản ứng hóa học tăng 4 lần; cho biết tốc độ phản ứng giảm bao nhiêu lần khi nhiệt độ giảm từ 70oC xuống 40oC
Lời giải:
Khi nhiệt độ tăng thêm 10oC, tốc độ của một phản ứng hóa học tăng 4 lần
⇒ γ = 4
γt2−t110=440−7010=164
Khi nhiệt độ giảm từ 70oC xuống 40oC thì tốc độ phản ứng giảm 64 lần.
Lời giải:
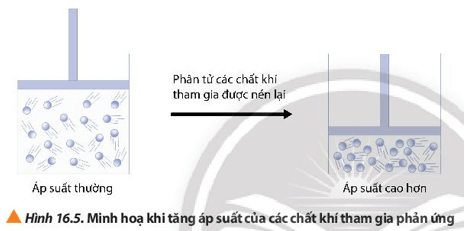
Ở áp suất bình thường, các phân tử khí tham gia chuyển động xa nhau hơn.
Khi bị nén dưới áp suất cao hơn, các phân tử khí tham gia được nén lại gần nhau dẫn đến số va chạm hiệu quả tăng lên.
Luyện tập trang 101 Hóa học 10: Xét các phản ứng xảy ra trong bình kín: 2CO(g) + O2(g) → 2CO2(g) (1)
NH4Cl(s) → NH3(g) + HCl(g) (2)
Yếu tố áp suất ảnh hưởng đến tốc độ của phản ứng nào? Khi tăng áp suất, tốc độ phản ứng thay đổi như thế nào?
Lời giải:
Trong phản ứng hóa học có sự tham gia của chất khí, áp suất có thể ảnh hưởng đến tốc độ phản ứng.
Yếu tố áp suất ảnh hưởng đến tốc độ của phản ứng (1). Khi tăng áp suất tốc độ phản ứng tăng.
Thí nghiệm 2: Ảnh hưởng của bề mặt tiếp xúc đến tốc độ phản ứng
Hóa chất: Dung dịch HCl 1 M, đá vôi (CaCO3) dạng khối và dạng hạt nhỏ.
Dụng cụ: bình tam giác 100 mL, ống đong 50 mL, cân.
Tiến hành:
Bước 1: Cân khoảng 2 g CaCO3, mỗi loại, cho vào 2 bình tam giác (1), (2).
Bước 2: Đong khoảng 20 mL dung dịch HCl, rót đồng thời vào mỗi bình tam giác.
Phương trình hóa học của phản ứng:
CaCO3(s) + 2HCl(aq) → CaCl2(aq) + H2O(l) + CO2(g)

Lời giải:
Bình (1) chứa đá vôi dạng khối.
Bình (2) chứa đá vôi dạng hạt.
Nhận thấy khí thoát ra ở bình (2) nhanh hơn khí thoát ra ở bình (1).
Câu hỏi 7 trang 101 Hóa học 10: Nhận xét mối liên hệ giữa tốc độ phản ứng với kích thước của CaCO3.
Lời giải:
Kích thước của hạt đá vôi (CaCO3) càng nhỏ thì tốc độ phản ứng càng lớn.
Câu hỏi 8 trang 102 Hóa học 10: Quan sát Hình 16.7, giải thích kết quả của thí nghiệm 2.
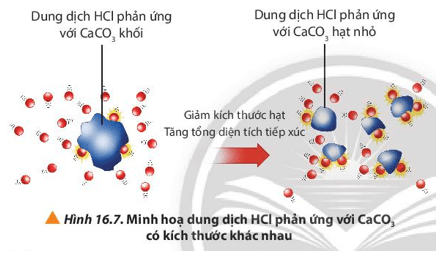
Lời giải:
Khi HCl phản ứng với CaCO3 dạng hạt, diện tích tiếp xúc giữa các phân tử HCl và CaCO3 tăng lên ⇒ số va chạm hiệu quả tăng ⇒ tốc độ phản ứng tăng.
Lời giải:
Củi được chẻ nhỏ ⇒ diện tích tiếp xúc giữa củi (nhiên liệu) với oxygen trong không khí tăng ⇒ tốc độ phản ứng cháy tăng.
Thí nghiệm 3: Ảnh hưởng của xúc tác đến tốc độ phản ứng
Hóa chất: dung dịch hydrogen peroxide (H2O2) 30%, bột MnO2.
Dụng cụ: Ống nghiệm, tàn đóm đỏ.
Tiến hành:
Bước 1: Rót khoảng 2 mL dung dịch H2O2 vào 2 ống nghiệm (1), (2).
Bước 2: Thêm một ít bột MnO2 vào ống nghiệm (2) và đưa nhanh tàn đóm đỏ vào miệng 2 ống nghiệm (Hình 16.8).
Phương trình hóa học của phản ứng:
2H2O2(aq) MnO2→ 2H2O(l) + O2(g)
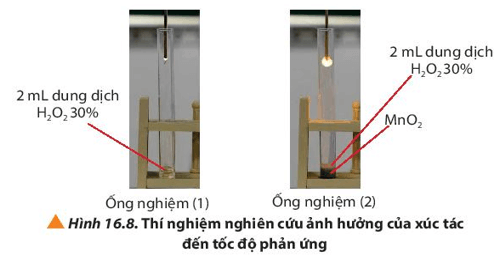
Lời giải:
Hiện tượng:
- Tàn đóm ở ồng nghiệm (1) chỉ cháy nhẹ.
- Tàn đóm ở ống nghiệm (2) bùng cháy mãnh liệt hơn.
Luyện tập trang 103 Hóa học 10: Tại sao nhai kĩ cơm, cảm nhận cơm có vị ngọt hơn?
Lời giải:
Enzyme amylase có trong nước bọt là chất xúc tác đẩy nhanh quá trình tiêu hóa tinh bột.
Khi nhai kĩ, thức ăn được chia nhỏ hơn ⇒ tăng diện tích tiếp xúc giữa thức ăn với các enzyme, khiến các phản ứng trong quá trình tiêu hóa tinh bột xảy ra nhanh hơn, hiệu quả hơn.

Lời giải:
- Hình 16.9a) Ảnh hưởng của nồng độ đến tốc độ phản ứng:
Nồng độ oxygen trong không khí chỉ chiếm 21%. Dùng bình chứa oxygen mục đích làm tăng nồng độ chất tham gia ⇒ Tăng tốc độ phản ứng cháy
- Hình 16.9b) Ảnh hưởng của áp suất đến tốc độ phản ứng.
Dùng nồi áp suất làm tăng áp suất trong nồi ⇒ tăng tốc độ phản ứng ⇒ Làm thức ăn nhanh chín hơn.
- Hình 16.9c) Ảnh hưởng của diện tích tiếp xúc đến tốc độ phản ứng.
Đậy nắp lò làm giảm diện tích tiếp xúc của than với oxygen trong không khí ⇒ Giảm tốc độ phản ứng cháy ⇒ Than cháy được lâu hơn.
- Hình 16.9d) Ảnh hưởng của nhiệt độ đến tốc độ phản ứng.
Bảo quản thức ăn trong tủ lạnh ⇒ Giảm nhiệt độ ⇒ Giảm tốc độ phản ứng oxi hóa thức ăn ⇒ Thức ăn lâu bị ôi thiu.
Lời giải:
Vận dụng yếu tố ảnh hưởng của chất xúc tác đến tốc độ phản ứng.
Chuối và nước dừa chứa các enzyme có vai trò là chất xúc tác cho quá trình lên men giấm.
Bài 1 trang 104 Hóa học 10: Hai nhân vật minh họa trong hình bên đang chế biến món gà rán, được thực hiện bằng hai cách. Một người chọn cách chia ra từng phần nhỏ, người còn lại chọn cách để nguyên, giả thiết các điều kiện đều giống nhau (nhiệt độ, lượng dầu ăn,…). Hãy cho biết cách nào món ăn nhanh chín hơn? Giải thích

Lời giải:
Khi chia từng phần nhỏ làm tăng diện tích tiếp xúc của gà với chảo dầu nóng
⇒ giúp gà nhanh chín hơn.
Lời giải:
- Khi tăng nồng độ chất phản ứng, tốc độ phản ứng tăng
- Khi tăng nhiệt độ, tốc độ phản ứng tăng
- Đối với phản ứng có chất khí tham gia, tốc độ phản ứng tăng khi tăng áp suất
- Khi tăng diện tích bề mặt tiếp xúc của chất phản ứng, tốc độ phản ứng tăng
- Chất xúc tác làm tăng tốc độ của phản ứng hóa học, nhưng vẫn được bảo toàn về chất lượng khi kết thúc phản ứng
Zn(s) + 2HCl(aq) → ZnCl2(aq) + H2(g)
Tốc độ khí H2 thoát ra như thế nào khi thay đổi các yếu tố dưới đây
a) Thay a g Zn hạt bằng a g bột Zn
b) Thay dung dịch HCl 2M bằng dung dịch HCl 1M
c) Thực hiện phản ứng ở nhiệt độ cao hơn bằng cách đun nóng nhẹ dung dịch HCl.
Lời giải:
a) Thay a g Zn hạt bằng a g bột Zn
⇒ Tăng diện tích tiếp xúc của chất phản ứng
⇒ Tăng tốc độ phản ứng
⇒ Khí H2 thoát ra nhanh hơn.
b) Thay dung dịch HCl 2M bằng dung dịch HCl 1M
⇒ Nồng độ chất tham gia giảm.
⇒ Tốc độ phản ứng giảm
⇒ Khí H2 thoát ra chậm hơn.
c) Thực hiện phản ứng ở nhiệt độ cao hơn bằng cách đun nóng nhẹ dung dịch HCl.
⇒ Tăng nhiệt độ của phản ứng
⇒ Tăng tốc độ phản ứng
⇒ Khí H2 thoát ra nhanh hơn.
Bài 4 trang 104 Hóa học 10: Cho phương trình hóa học của phản ứng: 2CO(g) + O2(g) → 2CO2(g)
Nếu hệ số nhiệt độ Van’t Hoff bằng 2, tốc độ phản ứng thay đổi như thế nào khi tăng nhiệt độ của phản ứng từ 30oC lên 60oC?
Lời giải:
Hệ số nhiệt độ Van’t Hoff γ = 2.
γt2−t110=260−3010=8
Khi tăng nhiệt độ của phản ứng từ 30oC lên 60oC tốc độ phản ứng tăng 8 lần.
Xem thêm các bài giải SGK Hoá học lớp 10 Chân trời sáng tạo hay, chi tiết khác:
Bài 15: Phương trình tốc độ phản ứng và hằng số tốc độ phản ứng
Bài 17: Tính chất vật lí và hóa học các đơn chất nhóm VIIA
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.