Với Giải SBT Hoá học 10 Bài 11.16 trang 32 trong Bài 11: Liên kết cộng hoá trị Sách bài tập Hoá học lớp 10 Cánh Diều hay nhất, chi tiết sẽ giúp học sinh dễ dàng làm bài tập trong SBT Hoá học 10.
Ghép mỗi nguyên tử hoặc phân tử sau với một hoặc các đặc điểm
Bài 11.16 trang 32 sách bài tập Hóa học 10: Ghép mỗi nguyên tử hoặc phân tử sau với một hoặc các đặc điểm tương ứng của nó: N2, Ar, CO, H2.
(1) Liên kết trong phân tử là liên kết cộng hoá trị không phân cực.
(2) Liên kết trong phân tử là liên kết cộng hoá trị phân cực.
(3) Các nguyên tử trong phân tử đều tuân theo quy tắc octet.
(4) Là khí trơ.
(5) Có hai cặp electron hoá trị riêng.
(6) Liên kết trong phân tử là liên kết đơn.
Lời giải:
- N2, công thức Liwis:
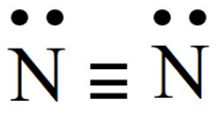
Các nhận định thỏa mãn:
(1) Liên kết trong phân tử là liên kết cộng hoá trị không phân cực.
(3) Các nguyên tử trong phân tử đều tuân theo quy tắc octet.
(5) Có hai cặp electron hoá trị riêng.
- Ar, nhận định thỏa mãn:
(4) Là khí trơ.
- CO, công thức Lewis:
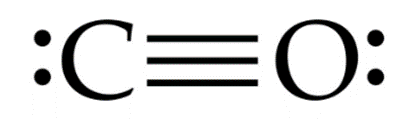
Các nhận định thỏa mãn:
(2) Liên kết trong phân tử là liên kết cộng hoá trị phân cực.
(3) Các nguyên tử trong phân tử đều tuân theo quy tắc octet.
(5) Có hai cặp electron hoá trị riêng.
- H2, công thức cấu tạo: H – H, các nhận định thỏa mãn:
(1) Liên kết trong phân tử là liên kết cộng hoá trị không phân cực.
(6) Liên kết trong phân tử là liên kết đơn.
Xem thêm lời giải SBT Hoá học lớp 10 Cánh Diều hay, chi tiết khác:
Bài 11.1 trang 30 sách bài tập Hóa học 10: Trong nguyên tử C, những electron có khả năng tham gia hình thành liên kết cộng hoá trị thuộc phân lớp nào sau đây?...
Bài 11.2 trang 30 sách bài tập Hóa học 10: Những phát biểu nào sau đây là không đúng?...
Bài 11.3 trang 30 sách bài tập Hóa học 10: Liên kết cộng hoá trị thường được hình thành giữa...
Bài 11.4 trang 30 sách bài tập Hóa học 10: Số lượng cặp electron dùng chung trong các phân tử H2, O2, N2, F2 lần lượt là..
Bài 11.5 trang 30 sách bài tập Hóa học 10: Trong phân tử HF, số cặp electron dùng chung và cặp electron hoá trị riêng của nguyên tử F lần lượt là..
Bài 11.6 trang 31 sách bài tập Hóa học 10: Cho công thức Lewis của các phân tử sau...
Bài 11.7 trang 31 sách bài tập Hóa học 10: Công thức nào sau đây ứng với công thức Lewis của phân tử PCl3?...
Bài 11.8 trang 31 sách bài tập Hóa học 10: Dựa vào hiệu độ âm điện giữa hai nguyên tố, cho biết liên kết trong phân tử nào sau đây là phân cực nhất...
Bài 11.9 trang 31 sách bài tập Hóa học 10: Hãy điền từ/ công thức thích hợp vào chỗ trống trong đoạn thông tin sau...
Bài 11.10 trang 31 sách bài tập Hóa học 10: Dựa vào hiệu độ âm điện, hãy nối các liên kết hình thành giữa các nguyên tử cột A với loại liên kết tương ứng ở cột B...
Bài 11.11 trang 31 sách bài tập Hóa học 10: Khi tham gia hình thành liên kết trong các phân tử HF, F2; orbital tham gia xen phủ tạo liên kết của nguyên tử...
Bài 11.12 trang 31 sách bài tập Hóa học 10: Số orbital của cả hai nguyên tử N tham gia xen phủ tạo liên kết trong phân tử N2 là...
Bài 11.13 trang 31 sách bài tập Hóa học 10: Liên kết trong phân tử nào dưới đây không được hình thành do sự xen phủ giữa các orbital cùng loại (ví dụ cùng là orbital s, hoặc cùng là orbital p)?...
Bài 11.14 trang 32 sách bài tập Hóa học 10: Phát biểu nào sau đây không đúng?...
Bài 11.15 trang 32 sách bài tập Hóa học 10: Số lượng electron tham gia hình thành liên kết đơn, đôi và ba lần lượt là...
Bài 11.16 trang 32 sách bài tập Hóa học 10: Ghép mỗi nguyên tử hoặc phân tử sau với một hoặc các đặc điểm tương ứng của nó: N2, Ar, CO, H2...
Bài 11.17 trang 32 sách bài tập Hóa học 10: Xét phân tử H2O, những phát biểu nào sau đây là đúng?...
Bài 11.18 trang 32 sách bài tập Hóa học 10: Xét phân tử CO2, những phát biểu nào sau đây là không đúng?..
Bài 11.19 trang 33 sách bài tập Hóa học 10: Cho biết hóa trị của một nguyên tố trong phân tử bằng tổng số liên kết σ và π mà nguyên tử nguyên tố đó tạo thành khi liên kết...
Bài 11.20 trang 33 sách bài tập Hóa học 10: Cho biết năng lượng liên kết H – I và H – Br lần lượt là 297 kJ mol-1 và 364 kJ mol-1. Những phát biểu nào sau đây là không đúng?...
Bài 11.21 trang 33 sách bài tập Hóa học 10: Cho biết năng lượng liên kết H – H là 436 kJ mol-1. Hãy tính năng lượng cần thiết (theo eV) để phá vỡ liên kết...
Bài 11.22 trang 33 sách bài tập Hóa học 10: Thiết lập công thức Lewis cho các phân tử H2O, NH3 và CH4. Mỗi phân tử này có bao nhiêu cặp electron hóa trị riêng?...
Bài 11.23 trang 33 sách bài tập Hóa học 10: Sử dụng bảng năng lượng của một số liên kết ở điều kiện chuẩn....
Bài 11.24 trang 33 sách bài tập Hóa học 10: Các phân tử như F2, N2 khi phản ứng với H2 thì cần cắt đứt liên kết giữa các nguyên tử.
Bài 11.25 trang 33 sách bài tập Hóa học 10: Giải thích vì sao ở điều kiện thường không tồn tại phân tử NaCl riêng biệt mà là tinh thể NaCl...
Xem thêm các bài giải SBT Hoá học lớp 10 Cánh Diều hay, chi tiết khác:
Bài 10: Liên kết Ion
Bài 12: Liên kết hydrogen và tương tác Van Der Waals
Bài 13: Phản ứng oxi hoá - khử
Bài 14: Phản ứng hoá học và enthalpy
Bài 15: Ý nghĩa và cách tính biến thiên enthalpy phản ứng hoá học