Với giải Câu hỏi trang 86 SGK Hoá học10 Cánh Diều Bài 15: Ý nghĩa và cách tính biến thiên enthalpy phản ứng hóa học giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Hoá học 10. Mời các bạn đón xem:
Hoá học 10 Cánh Diều trang 86 Bài 15: Ý nghĩa và cách tính biến thiên enthalpy phản ứng hóa học
Lời giải:
Ta có phản ứng:
Phân tử CH4 gồm 4 liên kết C-H
Phân tử Cl2 gồm 1 liên kết Cl-Cl
Phân tử CH3Cl gồm 3 liên kết C-H và 1 liên kết C-Cl
Phân tử HCl gồm 1 liên kết H-Cl
Luyện tập 3 trang 86 Hóa học 10: Dựa vào năng lượng liên kết, tính ∆r các phản ứng sau:
a) Các phản ứng đốt cháy hoàn toàn 1 mol mỗi chất C2H4, C2H6, H2 ở thể khí.
b) F2(g) + H2O(g) → 2HF(g) + O2(g)
Dự đoán các phản ứng trên là thuận lợi hay không thuận lợi.
Lời giải:
a) C2H4(g) + 3O2(g) → 2CO2(g) + 2H2O(g)
∆r = 1 × Eb(C2H4) + 3 × Eb(O2) – 2 × Eb(CO2) – 2 × Eb(H2O)
∆r = 1 × (1EC=C + 4EC-H) + 3 × EO=O – 2 × 2EC=O – 2 × 2 × EO-H
∆r = 1 × (611 + 4 × 414) + 3 × 498 – 2 × 2 × 799 – 2 × 2 × 464
∆r = -1291 kJ < 0
⇒ Phản ứng này là thuận lợi
C2H6(g) + O2(g) → 2CO2(g) + 3H2O(g)
∆r = 1 × Eb(C2H6) + × Eb(O2) – 2 × Eb(CO2) – 3 × Eb(H2O)
∆r =1 × (1EC-C + 6EC-H) + × Eb(O2) – 2 × 2EC=O – 3 × 2 × EO-H
∆r = 1 × (347 + 6 × 414) + × 498 – 2 × 2 × 799 – 3 × 2 × 464
∆r = -1406 kJ < 0
⇒ Phản ứng này là thuận lợi
H2(g) + O2(g) → H2O(g)
∆r = 1 × Eb(H2) + × Eb(O2) – 1 × Eb(H2O)
∆r = 1 × EH-H + × Eb(O2) – 1 × 2 × EO-H
∆r = 1 × 436 + × 498 – 1 × 2 × 464 = -243 kJ < 0
⇒ Phản ứng này là thuận lợi
b) F2(g) + H2O(g) → 2HF(g) + O2(g)
∆r = 1 × E(F2) + 1 × E(H2O) - 2 × E(HF) - × E(O2)
∆r = 1 × EF-F + 1 × 2 × EO-H - 2 × EH-F - × E(O2)
∆r = 1 × 159 + 1 × 2 × 464 - 2 × 565 - × 498 = -292 kJ < 0
⇒ Phản ứng này là thuận lợi.
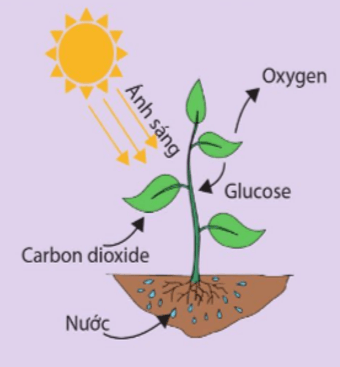
Vận dụng 5 trang 86 Hóa học 10: Phản ứng quang hợp là phản ứng thu năng lượng dưới dạng ánh sáng:
6CO2(g) + 6H2O(l) → C6H12O6 (s) + 6O2(g)
Hãy tính xem cần phải cung cấp bao nhiêu năng lượng dưới dạng ánh sáng cho những phản ứng quang hợp để tạo thành 1 mol glucose C6H12O6(s), biết enthalpy tạo thành chuẩn của chất này là -1271,1 kJ mol-1. Biến thiên enthalpy tạo thành chuẩn của các chất khác được cho ở phụ lục 3.
Lời giải:
Để tạo thành 1 mol glucose C6H12O6(s) ta có
6CO2(g) + 6H2O(l) → C6H12O6(s) + 6O2(g)
∆r = 1 × ∆f (C6H12O6) + 6 × ∆f (O2) – 6 × ∆f (CO2) – 6 × ∆f (H2O)
∆r = 1 × (-1271,1) + 6 × 0 – 6 × (-393,5) – 6 × (-285,8) = 2804,7 kJ
Vậy cần phải cung cấp năng lượng là 2804,7 kJ dưới dạng ánh sáng cho những phản ứng quang hợp để tạo thành 1 mol glucose C6H12O6(s).
Xem thêm các bài giải SGK Hoá học lớp 10 Cánh Diều hay, chi tiết khác:
Mở đầu trang 82 Hóa học 10: Cho hai phản ứng đốt cháy: (1) C(s) + O2(g) → CO2(g) ∆r = -393,5 kJ...
Luyện tập 1 trang 83 Hóa học 10: Cho phản ứng: CH4(g) + H2O(l) → CO(g) + 3H2(g) ∆r = 249,9 kJ. Ở điều kiện chuẩn...
Câu hỏi 2 trang 84 Hóa học 10: Phản ứng đốt cháy cồn hay phản ứng nung vôi dễ thực hiện hơn?...
Vận dụng 4 trang 85 Hóa học 10: Cho biết: 2NaHCO3(s) → Na2CO3(s) + CO2(g) + H2O(l) có ∆r = 91,6 kJ..
Câu hỏi 4 trang 85 Hóa học 10: Cho phản ứng sau ở điều kiện chuẩn: H-H(g) + F-F(g) → 2H-F(g)...
Luyện tập 3 trang 86 Hóa học 10: Dựa vào năng lượng liên kết, tính ∆r các phản ứng sau...
Vận dụng 5 trang 86 Hóa học 10: Phản ứng quang hợp là phản ứng thu năng lượng dưới dạng ánh sáng...
Xem thêm các bài giải Hoá học lớp 10 Cánh Diều hay, chi tiết khác:
Bài 14: Phản ứng hoá học học và enthalpy
Bài 17: Nguyên tố đơn chất halogen
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.