Toptailieu.vn xin giới thiệu 15 câu trắc nghiệm Ý nghĩa và cách tính biến thiên enthalpy phản ứng hóa học Cánh diều (có đáp án 2023) CHỌN LỌC, hay nhất giúp học sinh lớp 10 ôn luyện kiến thức để đạt kết quả cao trong các bài thi môn Hóa học.
Mời các bạn đón xem:
15 câu trắc nghiệm Ý nghĩa và cách tính biến thiên enthalpy phản ứng hóa học Cánh diều (có đáp án 2023) CHỌN LỌC
Lý thuyết
I. Ý nghĩa về dấu và giá trị của biến thiên enthalpy phản ứng
Có hai phản ứng kèm theo sự trao đổi năng lượng dưới dạng nhiệt:
- Phản ứng tỏa nhiệt: Biến thiên enthalpy của phản ứng có giá trị âm. Biến thiên enthalpy càng âm, phản ứng tỏa ra càng nhiều nhiệt.

- Phản ứng thu nhiệt: Biến thiên enthalpy của phản ứng có giá trị dương. Biến thiên enthalpy càng dương, phản ứng thu vào càng nhiều nhiệt.

- Các phản ứng tỏa nhiệt (![]() < 0) thường diễn ra thuận lợi hơn các phản ứng thu nhiệt (
< 0) thường diễn ra thuận lợi hơn các phản ứng thu nhiệt (![]() >0)
>0)
Ví dụ: Sau khi được đốt nóng, Na tự cháy trong oxygen cho đến hết do phản ứng này có ![]() rất âm.
rất âm.
![]()
II. Cách tính biến thiên Enthalpy phản ứng
Có 2 cách:
1. Tính biến thiên enthapy phản ứng theo enthalpy tạo thành
Giả sử có phương trình tổng quát: aA + bB -> mM + nN
- Biến thiên enthalpy của phản ứng được xác định bằng hiệu số giữa tổng nhiệt tạo thành các chất sản phẩm (sp) và tổng nhiệt tạo thành của các chất đầu (cđ)
- Biến thiên enthalpy chuẩn của phản ứng được tín theo công thức:
![]()
VÍ dụ: Cho phản ứng:
![]()
Biến thiên Enthalpy chuẩn của phản ứng này được tính như sau:
![]()
Thay các giá trị tương ứng:
![]()
2. Tính biến thiên Enthalpy phản ứng theo năng lượng liên kết
Giả sử có phản ứng tổng quát:
aA(g) + bB(g) -> mM(g) + nN(g)
Biến thiên Enthalpy chuẩn của phản ứng này được tính như sau:
![]()

Ví dụ: Cho phản ứng:
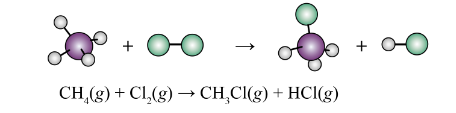
Biến thiên Enthalpy chuẩn của phản ứng tính theo năng lượng liên kết như sau:
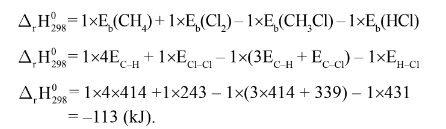
Bài tập
Câu 1. Biến thiên enthalpy của phản ứng nào sau đây có giá trị âm?
A. Phản ứng tỏa nhiệt.
B. Phản ứng thu nhiệt.
C. Phản ứng oxi hóa – khử.
D. Phản ứng phân hủy.
Đáp án: A
Phản ứng tỏa nhiệt biến thiên enthalpy có giá trị âm.
Phản ứng thu nhiệt biến thiên enthalpy có giá trị dương.
Câu 2. Phát biểu nào sau đây là không đúng?
A. Biến thiên enthalpy càng âm, phản ứng tỏa ra càng nhiều nhiệt.
B. Biến thiên enthalpy càng dương, phản ứng thu vào càng nhiều nhiệt.
C. Với phản ứng tỏa nhiệt, năng lượng của hệ chất phản ứng cao hơn năng lượng của hệ sản phẩm.
D. Với phản ứng thu nhiệt, năng lượng của hệ chất phản ứng cao hơn năng lượng của hệ sản phẩm.
Đáp án: D
Với phản ứng thu nhiệt, năng lượng của hệ chất phản ứng thấp hơn năng lượng của hệ sản phẩm, do đó phản ứng diễn ra kèm theo sự hấp thu năng lượng dưới dạng nhiệt.
Câu 3. Cho phản ứng sau: H2(g) + Cl2(k) → 2HCl ![]() = -184,6 kJ. Phản ứng trên là
= -184,6 kJ. Phản ứng trên là
A. phản ứng thu nhiệt.
B. phản ứng tỏa nhiệt.
C. phản ứng thế.
D. phản ứng phân hủy.
Đáp án: B
![]() < 0 → Phản ứng là phản ứng tỏa nhiệt.
< 0 → Phản ứng là phản ứng tỏa nhiệt.
Câu 4. Cho các phản ứng sau:
(1) C(s) + O2(g) → CO2(g) ![]() = -393,5 kJ
= -393,5 kJ
(2) 2Al(s) + ![]() O2(g) → Al2O3(s)
O2(g) → Al2O3(s) ![]() = -1675,7 kJ
= -1675,7 kJ
(3) CH4(g) + 2O2(g) → CO2(g) + 2H2O(l) ![]() = -890,36 kJ
= -890,36 kJ
(4) C2H2(g) + ![]() O2(g) → 2CO2(g) + H2O (l)
O2(g) → 2CO2(g) + H2O (l) ![]() = -1299,58 kJ
= -1299,58 kJ
Trong các phản ứng trên, phản ứng nào tỏa nhiều nhiệt nhất?
A. (1).
B. (2).
C. (3).
D. (4).
Đáp án: D
Phản ứng tỏa nhiệt biến thiên enthalpy có giá trị âm. Biến thiên enthalpy càng âm, phản ứng tỏa ra càng nhiều nhiệt.
→ Phản ứng tỏa nhiều nhiệt nhất là phản ứng (4).
Câu 5. Người ta sử dụng chất nào trong đèn xì hàn, cắt kim loại?
A. CH4.
B. C2H2.
C. C2H4.
D. C2H6.
Đáp án: B
Người ta sử dụng C2H2 trong đèn xì hàn, cắt kim loại do phản ứng đốt cháy C2H2 tỏa rất nhiều nhiệt.
C2H2(g) + ![]() O2(g) → 2CO2(g) + H2O (l)
O2(g) → 2CO2(g) + H2O (l) ![]() = -1299,58 kJ
= -1299,58 kJ
Câu 6. Vì sao khi nung vôi, người ta phải xếp đá vôi lẫn với than trong lò?
A. Vì phản ứng nung vôi là phản ứng tỏa nhiệt.
B. Vì phải ứng nung vôi là phản ứng thu nhiệt, cần nhiệt từ quá trình đốt cháy than.
C. Để rút ngắn thời gian nung vôi.
D. Vì than hấp thu bớt lượng nhiệt tỏa ra của phản ứng nung vôi.
Đáp án: B
Khi nung vôi, người ta phải xếp đá vôi lẫn với than trong lò. Vì phản ứng nung vôi là phản ứng thu nhiệt, cần nhiệt từ quá trình đốt cháy than, nếu dừng cung cấp nhiệt thì phản ứng nung vôi sẽ không tiếp diễn.
Câu 7. Phản ứng nào sau đây cần phải khơi mào?
A. Phản ứng tạo gỉ sắt.
B. Phản ứng tạo gỉ đồng.
C. Phản ứng nổ.
D. Phản ứng trung hòa acid – base.
Đáp án: C
Đối với các phản ứng tỏa nhiệt, một số phản ứng cần phải khơi mào. Chẳng hạn phải đốt nóng để gây phản ứng cho một lượng nhỏ chất ban đầu trong các phản ứng cháy, nổ, …; sau đó, phản ứng tỏa nhiệt có thể tiếp diễn mà không cần tiếp tục đun nóng.
Câu 8. Cho các phát biểu sau:
(1) Hầu hết các phản ứng thu nhiệt và tỏa nhiệt đều cần thiết khơi mào (đun hoặc đốt nóng …).
(2) Khi đốt cháy tờ giấy hay đốt lò than, ta cần thực hiện giai đoạn khơi mào như đun hoặc đốt nóng.
(3) Một số phản ứng thu nhiệt diễn ra bằng cách lấy nhiệt từ môi trường bên ngoài, nên làm cho nhiệt độ của môi trường xung quanh giảm đi.
(4) Sau giai đoạn khơi mào, phản ứng tỏa nhiệt cần phải tiếp tục đun hoặc đốt nóng.
Trong các phát biểu trên, số phát biểu đúng là
A. 1.
B. 2.
C. 3.
D. 4.
Đáp án: C
Phát biểu đúng: (2), (3), (4).
Phát biểu (1) không đúng, vì:
+ Hầu hết các phản ứng thu nhiệt cần thiết khơi mào (đun hoặc đốt nóng …)
+ Phản ứng tỏa nhiệt có thể có, có thể không cần khơi mào, tùy phản ứng cụ thể.
Câu 9. Cho phản ứng: CH4(g) + H2O(l) → CO2(g) + 3H2(g) ![]() = 250 kJ.
= 250 kJ.
Ở điều kiện chuẩn, để thu được 2 gam H2, phản ứng này cần hấp thu nhiệt lượng bằng bao nhiêu?
A. 250 kJ.
B. 83,33 kJ.
C. 125 kJ.
D. 50 kJ.
Đáp án: B
CH4(g) + H2O(l) → CO2(g) + 3H2(g) ![]() = 250 kJ.
= 250 kJ.
Để tạo thành 3 mol (tương ứng với 6 gam) H2 thì phản ứng cần hấp thu nhiệt lượng là 250 kJ.
→ Để tạo thành 2 gam H2 thì phản ứng cần hấp thu nhiệt lượng là: ![]() ≈ 83,33 kJ.
≈ 83,33 kJ.
Câu 10. Các phản ứng tỏa nhiệt thường diễn ra
A. thuận lợi hơn các phản ứng thu nhiệt.
B. khó khăn hơn các phản ứng thu nhiệt.
C. thuận lợi hơn khi càng tỏa nhiều nhiệt.
D. thuận lợi hơn khi càng tỏa ít nhiệt.
Đáp án: A
Phản ứng tỏa nhiệt (![]() < 0) thường diễn ra thuận lợi hơn các phản ứng thu nhiệt (
< 0) thường diễn ra thuận lợi hơn các phản ứng thu nhiệt (![]() > 0).
> 0).
Câu 11. Cho phản ứng sau: CaCO3(s) → CaO(s) + CO2(g) có ![]() = 178,29 kJ. Phát biểu nào sau đây là đúng?
= 178,29 kJ. Phát biểu nào sau đây là đúng?
A. Để tạo thành 1 mol CaO thì phản ứng giải phóng một lượng nhiệt là 178,29 kJ.
B. Phản ứng là phản ứng tỏa nhiệt.
C. Phản ứng diễn ra thuận lợi.
D. Phản ứng diễn ra không thuận lợi.
Đáp án: D
CaCO3(s) → CaO(s) + CO2(g) có ![]() = 178,29 kJ
= 178,29 kJ
Phản ứng trên là phản ứng thu nhiệt (![]() > 0).
> 0).
Để tạo thành 1 mol CaO thì cần phải cung cấp một lượng nhiệt là 178,29 kJ.
Phản ứng thu nhiệt (![]() > 0) nên phản ứng là không thuận lợi (Các phản ứng tỏa nhiệt thường diễn ra thuận lợi hơn các phản ứng thu nhiệt).
> 0) nên phản ứng là không thuận lợi (Các phản ứng tỏa nhiệt thường diễn ra thuận lợi hơn các phản ứng thu nhiệt).
Câu 12. Cho các phản ứng sau:
(1) 2Na(s) + ![]() O2(g) → Na2O(s)
O2(g) → Na2O(s) ![]() = -417,98 kJ
= -417,98 kJ
(2) ![]() H2(g) +
H2(g) + ![]() I2(r) → HI(g)
I2(r) → HI(g) ![]() = 26,48 kJ
= 26,48 kJ
Nhận định nào sau đây là đúng?
A. Phản ứng (2) diễn ra thuận lợi hơn rất nhiều phản ứng (1).
B. Phản ứng (1) diễn ra thuận lợi hơn rất nhiều phản ứng (2).
C. Phản ứng (1) và (2) mức độ diễn ra thuận lợi như nhau.
D. Không xác định được phản ứng nào diễn ra thuận lợi hơn.
Đáp án: B
Phản ứng tỏa nhiệt (![]() < 0) thường diễn ra thuận lợi hơn các phản ứng thu nhiệt (
< 0) thường diễn ra thuận lợi hơn các phản ứng thu nhiệt ( ![]() > 0).
> 0).
→ Phản ứng (1) là phản ứng tỏa nhiệt diễn ra thuận lợi hơn rất nhiều phản ứng (2) là phản ứng thu nhiệt. Ở điều kiện chuẩn, phản ứng (2) chỉ xảy ra khi được đốt nóng (cung cấp nhiệt); dừng đốt nóng, phản ứng sẽ dừng lại.
Câu 13. Tính biến thiên enthalpy của phản ứng sau:
NaHCO3(s) → Na2CO3(s) + CO2(g) + H2O(l)
Biết: ![]() (NaHCO3) = -950,8 kJ mol-1;
(NaHCO3) = -950,8 kJ mol-1; ![]() (Na2CO3) = -1130,7 kJ mol-1;
(Na2CO3) = -1130,7 kJ mol-1;
![]() (CO2) = -393,5 kJ mol-1;
(CO2) = -393,5 kJ mol-1; ![]() (H2O) = -285,8 kJ mol-1.
(H2O) = -285,8 kJ mol-1.
A. -102,8 kJ.
B. 102,8 kJ.
C. 91,6 kJ.
D. -91,6 kJ.
Đáp án: C
2NaHCO3(s) → Na2CO3(s) + CO2(g) + H2O(l)
Biến thiên enthalpy chuẩn của phản ứng là:
![]() =
= ![]() (Na2CO3) +
(Na2CO3) + ![]() (CO2) +
(CO2) + ![]() (H2O) – 2 ×
(H2O) – 2 × ![]() (NaHCO3)
(NaHCO3)
= (-1130,7) + (-393,5) + (-285,8) - 2×(-950,8) = 91,6 kJ.
Câu 14. Tính biến thiên enthalpy của phản ứng đốt cháy hoàn toàn 1 mol ethane (C2H6).
C2H6(g) + ![]() O2(g) → 2CO2(g) + 3H2O(l)
O2(g) → 2CO2(g) + 3H2O(l)
Biết: ![]() (C2H6) = -84,0 kJ mol-1
(C2H6) = -84,0 kJ mol-1 ![]() (CO2) = -393,5 kJ mol-1;
(CO2) = -393,5 kJ mol-1;
![]() (H2O) = -285,8 kJ mol-1.
(H2O) = -285,8 kJ mol-1.
A. 256,8 kJ.
B. -256,8 kJ.
C. -1560,4 kJ.
D. 1560,4 kJ.
Đáp án: D
![]() (O2) = 0 kJ mol-1 (đơn chất).
(O2) = 0 kJ mol-1 (đơn chất).
Biến thiên enthalpy chuẩn của phản ứng là:
![]() = 2×
= 2× ![]() (CO2) + 3 ×
(CO2) + 3 × ![]() (H2O) -
(H2O) - ![]() (C2H6)
(C2H6)
= 2×(-393,5) + 3×(-285,8) – (-84,0) = -1560,4 kJ.
Câu 15. Dựa vào năng lượng liên kết, tính ![]() của phản ứng sau:
của phản ứng sau:
F2(g) + H2O(g) → 2HF(g) + ![]() O2(g)
O2(g)
Biết năng lượng liên kết: EF-F = 159 kJ mol-1; EO-H = 464 kJ mol-1; EH-F = 565 kJ mol-1;
EO2 =498kJ mol-1.
A. -114kJ.
B. 114kJ.
C. 180 kJ.
D. -180kJ.
Đáp án: A
F2(g) + H2O(g) → 2HF(g) + ![]() O2(g)
O2(g)
Biến thiên chuẩn của phản ứng được tính như sau:
![]() = 1 × Eb(F2) + 1 × Eb(H2O) – 2 × Eb(HF) -
= 1 × Eb(F2) + 1 × Eb(H2O) – 2 × Eb(HF) - ![]() × Eb(O2)
× Eb(O2)
= 1×EF-F + 1×2×EO-H - 2×EH-F - ![]() × EO2
× EO2
= 159 + 2 × 464 – 2 × 565 - ![]() × 498 = -292 kJ.
× 498 = -292 kJ.
Xem thêm các bài giải Trắc nghiệm Hóa lớp 10 Cánh diều hay, chi tiết khác:
Bài 14: Phản ứng hóa học và enthalpy
Bài 16: Tốc độ phản ứng hóa học
Bài 17: Nguyên tố và đơn chất halogen
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.