Với giải Câu hỏi trang 114 SGK Hoá học10 Cánh Diều Bài 18: Hydrogen halide và hydrohalic acid giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Hoá học 10. Mời các bạn đón xem:
Nội dung bài viết
Hoá học 10 Cánh Diều trang 114 Bài 18: Hydrogen halide và hydrohalic acid
Lời giải:
Nhiệt độ sôi của hydrogen bromide (HBr) cao hơn nhiệt độ sôi của hydrogen chloride (HCl) được giải thích bằng hai nguyên nhân:
- Thứ nhất, khối lượng phân tử của HBr cao hơn khối lượng phân tử HCl nên năng lượng cần thiết cho quá trình sôi của HBr cao hơn.
- Thứ hai, kích thước và số lượng electron trong phân tử HBr lớn hơn làm tăng cường thêm khả năng xuất hiện các lưỡng cực tạm thời trong phân tử. Khi đó làm tăng tương tác van der Waals giữa các phân tử HBr.'
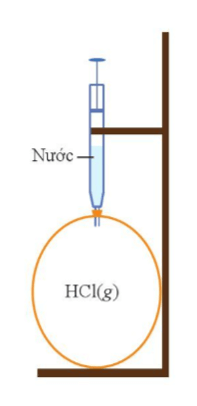
Lời giải:
Hydrogen chloride ở thể khí chiếm toàn bộ thể tích quả bóng. Khi bơm nước vào xi-xanh, hydrogen chloride tan trong nước tạo dung dịch hydrochloric acid khiến thể tích giảm
⇒ Quả bóng bị xẹp đi
4HCl + MnO2 t°→ Cl2 + MnCl2 + 2H2O
Cho biết khí chlorine thu được có thể lẫn với chất nào. Chỉ ra chất khử và chất oxi hóa trong phản ứng trên.
b) Hãy dự đoán, hydroiodic acid có phản ứng được với manganese(IV) oxide không. Giải thích.
Lời giải:
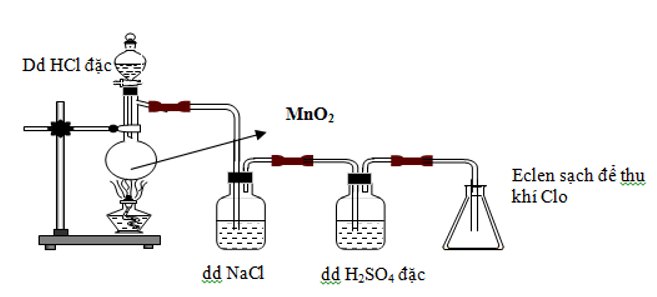
a) Khí chlorine có thể bị lẫn khí HCl và hơi nước. Dẫn khí tạo thành qua bình đựng dung dịch NaCl để giữ lại HCl. Dẫn khí qua bình đựng dung dịch H2SO4 đặc để giữ hơi nước. Khí chlorine thu được cuối cùng là tinh khiết.
4+1H−1Cl++4Mn−2O2→0Cl2++2Mn−1Cl2+2+1H2−1O
Chất khử: HCl (số oxi hóa của Cl tăng từ -1 lên 0)
Chất oxi hóa: MnO2 (số oxi hóa của Mn giảm từ +4 xuống +2)
b) Hydroiodic acid (HI) có phản ứng được với mangan(IV) oxide (MnO2). Vì tính khử của I- lớn hơn Cl-
4+1H−1I++4Mn−2O2→0I2++2Mn−1I2+2+1H2−1O
Chất khử: HI (số oxi hóa của I tăng từ -1 lên 0)
Chất oxi hóa: MnO2 (số oxi hóa của Mn giảm từ +4 xuống +2)
a) Từ hiện tượng được mô tả trên, hãy dự đoán sản phẩm của quá trình dung dịch hydrobromic acid bị oxi hóa bởi oxygen trong không khí.
b) Thực tế, hydrobromic acid được bảo quản trong các lọ kín tối màu. Giải thích.
Lời giải:
a) Dự đoán sản phẩm gồm: Br2 (màu vàng nâu) và H2O
Phương trình hóa học của phản ứng: 4HBr + O2 → 2Br2 + 2H2O
b) Thực tế, hydrobromic acid dễ bị phân hủy khi có ánh sáng nên thường được bảo quản trong các lọ kín tối màu.
Xem thêm các bài giải Hoá học lớp 10 Cánh Diều hay, chi tiết khác:
Vận dụng trang 112 Hóa học 10: Vật dụng bằng kim loại đồng dễ bị phủ bởi lớp copper(II) oxide...
Thực hành trang 113 Hóa học 10: Nhận biết các dung dịch. Có bốn bình nhỏ được đậy bằng nút có ống nhỏ giọt. Mỗi bình chứa một trong các dung dịch sodium chloride...
Xem thêm các bài giải SGK Hoá học lớp 10 Cánh Diều hay, chi tiết khác:
Bài 17: Nguyên tố đơn chất halogen
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.