Toptailieu.vn biên soạn và giới thiệu Công thức Lewis của CS2 (Carbon disulfide) (chương trình mới) của ba bộ sách Kết nối tri thức, Cánh diều, Chân trời sáng tạo giúp học sinh dễ dàng nắm vững Công thức Lewis của CS2 (Carbon disulfide) từ đó học tốt môn Hóa học.
Nội dung bài viết
Công thức Lewis của CS2 (Carbon disulfide) chương trình mới
1. Công thức Lewis của CS2
a) Cách 1: Viết công thức Lewis dựa vào công thức electron
Từ công thức electron, thay 1 cặp electron dùng chung bằng 1 gạch nối “–” giữa hai nguyên tử ta được công thức Lewis
Từ công thức electron của CS2, thay mỗi cặp electron bằng một gạch nối. Ta được công thức Lewis của CS2 là:
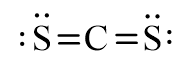
b) Cách 2: Viết công thức Lewis dựa theo các bước sau:
Bước 1: Tính tổng số electron hóa trị trong phân tử
Carbon có 4 electron hóa trị, S có 6 electron hóa trị. Trong phân tử CS2 có 1 nguyên tử carbon và 2 nguyên tử sulfur.
Vậy tổng số electron hóa trị = 4 + 6.2 = 16 electron.
Bước 2. Vẽ khung phân tử tạo bởi liên kết đơn giữa các nguyên tử
Trong phân tử CS2, nguyên tử C cần 4 electron để đạt octet, nguyên tử S cần 2 electron hóa trị để đạt octet. Vì vậy, C là nguyên tử trung tâm, còn các nguyên tử S được xếp xung quanh:
Vẽ một gạch (một liên kết) từ nguyên tử trung tâm tới mỗi nguyên tử xung quanh.
S – C – S (1)
Bước 3. Tính số electron hóa trị chưa tham gia liên kết bằng cách lấy tổng số electron trừ số electron tham gia tạo liên kết.
Số electron hóa trị chưa tham gia liên kết trong sơ đồ là:
16 – 2.2 = 12
Hoàn thiện octet cho các nguyên tử có độ âm điện lớn hơn trong sơ đồ.
Trong công thức (1), xung quanh mỗi nguyên tử S mới có 2 electron nên cần phải bổ sung 6 electron vào mỗi nguyên tử này. Ta được công thức (2)
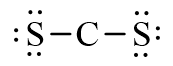
Số electron hóa trị còn lại: 12 – 6.2 = 0
Nguyên tử trung tâm C có 4 electron hóa trị, chưa đạt octet.
Bước 4. Chuyển cặp electron chưa liên kết trên nguyên tử xung quanh thành electron liên kết sao cho nguyên tử trung tâm thỏa mãn quy tắc octet.
Vì C chưa đạt octet, cần chuyển một cặp electron của mỗi nguyên tử S thành cặp electron chung giữa C và S để C đạt octet.
Công thức Lewis của phân tử CS2 thu được là:
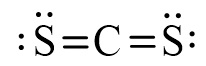
- Nhận xét:
+ Hiệu độ âm điện giữa C và S = |2,55 – 2,58| = 0,03 < 0,4 ⇒ liên kết C = S trong phân tử CS2 thuộc loại liên kết cộng hóa trị không phân cực.
2. Công thức electron của CS2
- Sự tạo thành phân tử CS2:
Nguyên tử carbon (C) có cấu hình electron là 1s22s22p2, nguyên tử sulfur (S) có cấu hình electron là 1s22s22p63s23p4. Để đạt được cấu hình electron bền vững của khí hiếm gần nhất, nguyên tử C cần 4 electron, nguyên tử S cần 2 electron. Trong phân tử CS2, mỗi nguyên tử S góp chung 2 electron với nguyên tử C tạo thành 2 cặp electron dùng chung.
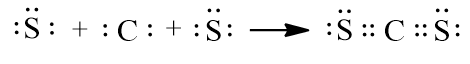
- Công thức electron của CS2 là:
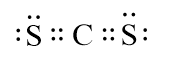
- Nhận xét:
+ Phân tử CS2 có 4 cặp electron chung, trong đó C liên kết với mỗi nguyên tử S bằng 2 cặp electron chung.
+ Trong phân tử CS2, C không có electron tự do, mỗi nguyên tử S còn 2 cặp electron tự do.
3. Công thức cấu tạo của CS2
Từ công thức Lewis, ta loại bỏ đi các electron tự do (electron không tham gia liên kết) thu được công thức cấu tạo.
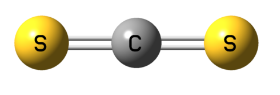
- Công thức cấu tạo của CS2 là:
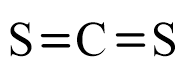
- Nhận xét:
+ Phân tử CS2 có hai liên kết đôi C = S (trong mỗi liên kết đôi có chứa 1 liên kết σ và một liên kết π).
+ Phân tử CS2 có cấu tạo thẳng
4. Bài tập mở rộng về CS2 (Carbon disulfide)
Câu 1. Số liên kết σ và liên kết π trong phân tử CS2 lần lượt là:
A. 1 và 2
B. 2 và 2
C. 1 và 1
D. 3 và 1
Hướng dẫn giải
Đáp án đúng là: B
Phân tử CS2 có hai liên kết đôi C = S (trong mỗi liên kết đôi có chứa 1 liên kết σ và một liên kết π).
Vậy tổng số liên kết σ và liên kết π trong phân tử CS2 lần lượt là: 2 và 2
Câu 2. Biết nguyên tử C có 4 electron hóa trị, nguyên tử S có 6 electron hóa trị. Công thức electron của hợp chất CS2 là:
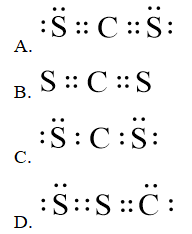
Hướng dẫn giải
Đáp án đúng là: A
Để đạt được cấu hình electron bền vững của khí hiếm gần nhất, nguyên tử C cần 4 electron, nguyên tử S cần 2 electron. Trong phân tử CS2, mỗi nguyên tử S góp chung 2 electron với nguyên tử C tạo thành 2 cặp electron dùng chung.
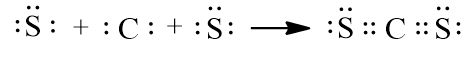
- Công thức electron của CS2 là:
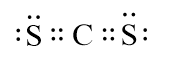
Xem thêm các bài giải Công thức Lewis của một số chất thường gặp chương trình mới hay, chi tiết khác:
Cách viết công thức Lewis (chương trình mới)
Công thức Lewis của CO2 (carbon dioxide) theo chương trình mới
Công thức Lewis của Cl2 theo chương trình mới
Công thức Lewis của H2 (Hydrogen) theo chương trình mới
Công thức Lewis của O2 (Oxygen) theo chương trình mới
Công thức Lewis của F2 theo chương trình mới
Công thức Lewis của N2 (nitrogen) theo chương trình mới
Công thức Lewis của HCl (hydrogen chloride) theo chương trình mới
Công thức Lewis của H2O theo chương trình mới
Công thức Lewis của H2S theo chương trình mới
Công thức Lewis của NH3 theo chương trình mới
Công thức Lewis của CH4 (Methane) theo chương trình mới
Công thức Lewis của SO2 theo chương trình mới
Công thức Lewis của CO theo chương trình mới
Công thức Lewis của SO3 theo chương trình mới
Công thức Lewis của HNO3 (Nitric acid) theo chương trình mới
Công thức Lewis của C2H2 theo chương trình mới
Công thức Lewis của C2H4 (Ethylene) theo chương trình mới
Công thức Lewis của CS2 (Carbon disulfide) theo chương trình mới
Công thức Lewis của HOCl theo chương trình mới
Công thức Lewis của HCN theo chương trình mới
Công thức Lewis của PH3 theo chương trình mới
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.