Toptailieu.vn xin giới thiệu Lý thuyết KHTH 8 (Kết nối tri thức) Bài 10: Oxide. Bài viết gồm phần lý thuyết trọng tâm nhất được trình bày một cách dễ hiểu, dễ nhớ bên cạnh đó là bộ câu hỏi trắc nghiệm có hướng dẫn giải chi tiết để học sinh có thể vận dụng ngay lý thuyết, nắm bài một cách hiệu quả nhất. Mời các bạn đón xem:
Nội dung bài viết
Lý thuyết KHTH 8 (Kết nối tri thức) Bài 10: Oxide
Bài giảng Bài 10: Oxide
A. Kiến thức trọng tâm KHTN 8 Bài 10: Oxide
I. Khái niệm về oxide
1. Khái niệm về oxide
- Oxide là hợp chất của hai nguyên tố, trong đó có một nguyên tố là oxygen.
2. Phân loại oxide
- Dựa vào thành phần nguyên tố, oxide có thể phân thành hai loại: oxide kim loại và oxide phi kim. Oxide kim loại được tạo thành từ phản ứng của kim loại với oxygen, ví dụ như phản ứng giữa Ba và O2 tạo ra BaO. Oxide phi kim được tạo thành từ phản ứng của phi kim với oxygen, ví dụ như phản ứng giữa C và O2 tạo ra CO2.
- Dựa vào tính chất hoá học, oxide có thể phân thành bốn loại: oxide acid, oxide base, oxide lưỡng tính và oxide trung tính.
- Quy tắc gọi tên oxide
+ Với nguyên tố chỉ có một hoá trị, ta đặt tên nguyên tố trước oxide, ví dụ như Sine oxide (ZnO).
+ Nguyên tố nhiều hoá trị: Tên nguyên tố (hoá trị của nguyên tố) + oxide
+ Cách đặt tên oxide của phi kim nhiều hoá trị:
+ (Tiền tố chỉ số nguyên tử của nguyên tố) Tên nguyên tố + (tiền tố chỉ số nguyên tử oxygen) oxide
+ (Tiền tố mono là một, đi là hai, trẻ là ba, tetra là bốn)
Ví dụ: FeO đọc là iron(II) oxide, CO đọc là carbon monoxide hoặc carbon(II) oxide, CO2 đọc là carbon dioxide hoặc carbon(IV) oxide
II. Tính chất hoá học
1. Oxide acid
- Oxide acid tác dụng với dung dịch base tạo thành muối và nước.
Ví dụ: CO2 + Ca(OH)2 → CaCO3 + H2O
- Khi sục từ từ khí CO2 vào dung dịch Ca(OH)2, ban đầu dung dịch vẩn đục do tạo muối CaCO3 không tan.
- Các oxide acid (như SO2, SO3, P2O5...) phản ứng với dung dịch base tạo thành muối và nước.
Ví dụ: SO2 + Ca(OH)2 → CaSO3 + H2O.
- Để kiểm tra tính chất của oxide acid, ta có thể thực hiện thí nghiệm bằng cách cho bột đá vôi và dung dịch hydrochloric acid vào ống nghiệm, sau đó dẫn khí carbon dioxide vào để tạo thành khí carbonic, quan sát hiện tượng xảy ra.
2. Oxide base
- Các oxide base (như CuO, Na2O, CaO...) phản ứng với dung dịch acid tạo thành muối và nước.
Ví dụ: CuO + H2SO4 → CuSO4 + H2O.
- Để kiểm tra tính chất của oxide base, ta có thể thực hiện thí nghiệm bằng cách cho bột CuO và dung dịch H2SO4 vào ống nghiệm, sau đó quan sát hiện tượng xảy ra.
Oxide lưỡng tính:
Oxide lưỡng tính (như Al2O3, ZnO...) tác dụng được với cả dung dịch acid và dung dịch base tạo thành muối và nước. Ví dụ: Al2O3 + 6HCl → 2AlCl3 + 3H2O.
3. Oxide trung tính
Oxide trung tính (như CO, N2O...) không tác dụng với dung dịch acid và dung dịch base, không tạo muối.
Sơ đồ tư duy KHTN 8 Bài 10: Oxide
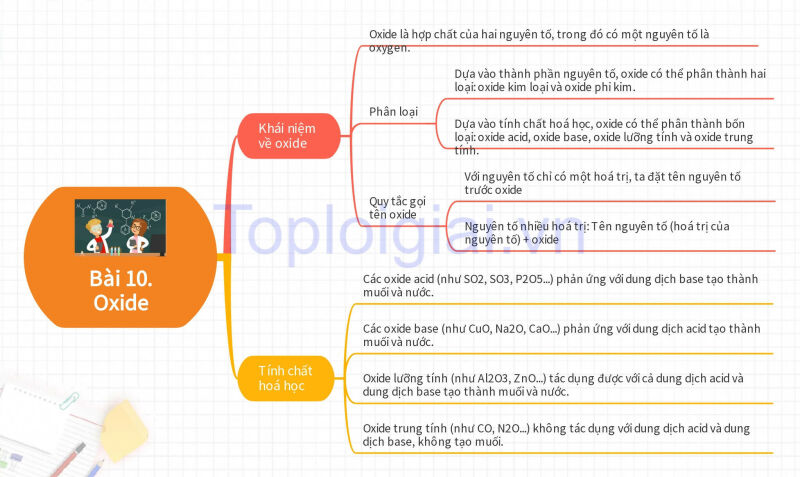
B. Bài tập KHTN 8 Bài 10: Oxide
Đang cập nhật
Xem thêm các bài lý thuyết Khoa học tự nhiên 8 Kết nối tri thức hay, chi tiết khác:
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.