Toptailieu.vn xin giới thiệu Lý thuyết KHTN 8 (Cánh diều) Bài 6: Nồng độ dung dịch. Bài viết gồm phần lý thuyết trọng tâm nhất được trình bày một cách dễ hiểu, dễ nhớ bên cạnh đó là bộ câu hỏi trắc nghiệm có hướng dẫn giải chi tiết để học sinh có thể vận dụng ngay lý thuyết, nắm bài một cách hiệu quả nhất. Mời các bạn đón xem:
Lý thuyết KHTN 8 (Cánh diều) Bài 6: Nồng độ dung dịch
Bài giảng Bài 6: Nồng độ dung dịch
A. Kiến thức trọng tâm KHTN 8 Bài 6: Nồng độ dung dịch
I. Độ tan của một chất trong nước
Dung dịch là hỗn hợp lỏng đồng nhất của chất tan và dung môi.
Ví dụ:
Cho một thìa muối ăn vào nước và khuấy đều.
Trong quá trình này, muối ăn là chất tan, nước là dung môi và nước muối là dung dịch.
1. Định nghĩa
Độ tan (kí hiệu là S) của một chất trong nước là số gam chất đó hoà tan trong 100 gam nước để tạo thành dung dịch bão hoà ở một nhiệt độ, áp suất xác định.
Các chất khác nhau có độ tan khác nhau.
Ví dụ:
Độ tan của NaCl trong nước ở 25oC là 36 g/100 g H2O.
2. Cách tính độ tan của một chất trong nước
Công thức tính độ tan của một chất ở nhiệt độ xác định là:
![]()
Trong đó:
mct là khối lượng của chất tan được hoà tan trong nước để tạo thành dung dịch bão hoà, có đơn vị là gam.
mnước là khối lượng của nước, có đơn vị là gam.
3. Ảnh hưởng của nhiệt độ đến độ tan của chất rắn trong nước
- Khi tăng nhiệt độ, độ tan của hầu hết các chất rắn đều tăng.
Ví dụ: Độ tan của đường ăn trong nước ở 30oC là 216,7 gam trong khi ở 60oC là 288,8 gam.
- Có một số chất khi tăng nhiệt độ, độ tan lại giảm.
II. Nồng độ dung dịch
Để biểu thị lượng chất tan có trong một lượng dung môi hoặc lượng dung dịch cụ thể người ta dùng khái niệm nồng độ dung dịch.
Có hai loại nồng độ dung dịch thường được sử dụng là nồng độ phần trăm và nồng độ mol.
1. Nồng độ phần trăm
Nồng độ phần trăm (kí hiệu là C%) của một dung dịch là số gam chất tan có trong 100 gam dung dịch.
Công thức tính nồng độ phần trăm của dung dịch là:
![]()
Trong đó:
mct là khối lượng chất tan, có đơn vị là gam.
mdd là khối lượng dung dịch, có đơn vị là gam.
Khối lượng dung dịch bằng tổng khối lượng của chất tan và khối lượng dung môi.
Nếu biết được nồng độ phần trăm của dung dịch thì ta có thể xác định được khối lượng chất tan và khối lượng dung dịch theo các biểu thức sau:
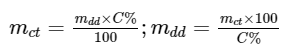
2. Nồng độ mol của dung dịch
Nồng độ mol (kí hiệu là CM) của một dung dịch là số mol chất tan có trong 1 lít dung dịch. Đơn vị của nồng độ mol là mol/L và thường được kí hiệu là M.
Công thức tính nồng độ mol của dung dịch:
![]()
Trong đó:
n là số mol chất tan, có đơn vị là mol.
V là thể tích dung dịch, có đơn vị là lít.
Nếu biết được nồng độ mol của dung dịch ta có thể xác định được số mol chất tan và thể tích dung dịch theo các biểu thức sau:
![]()
B. Bài tập KHTN 8 Bài 6: Nồng độ dung dịch
Đang cập nhật
Xem thêm các bài lý thuyết Khoa học tự nhiên 8 Cánh diều hay, chi tiết khác:
Bài 5: Tính theo phương trình hóa học
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.