Toptailieu.vn xin giới thiệu Lý thuyết Hydrocarbon không no (Kết nối tri thức) hay, chi tiết | Lý thuyết Hóa học 11. Bài viết gồm phần lý thuyết trọng tâm nhất được trình bày một cách dễ hiểu, dễ nhớ bên cạnh đó là bộ câu hỏi trắc nghiệm có hướng dẫn giải chi tiết để học sinh có thể vận dụng ngay lý thuyết, nắm bài một cách hiệu quả nhất. Mời các bạn đón xem:
Nội dung bài viết
Lý thuyết Hydrocarbon không no (Kết nối tri thức) hay, chi tiết | Lý thuyết Hóa học 11
A. Lý thuyết Hydrocarbon không no
1. Khái niệm, đồng phân, danh pháp
a. Khái niệm và công thức chung của alkene, alkyne
Hydrocarbon không no là những hydrocarbon trong phân tử có chứa liên kết đôi, liên kết ba (gọi chung là liên kết bội) hoặc đồng thời cả liên kết đôi và liên kết ba.
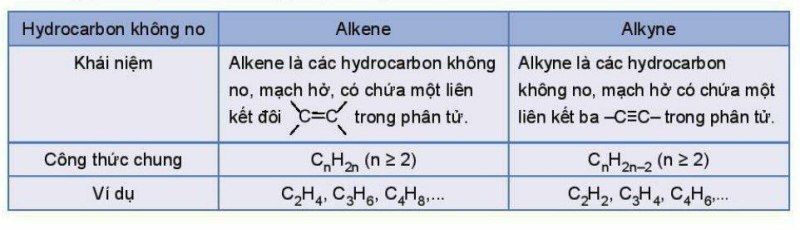
b. Đồng phân
* Đồng phân cấu tạo:
Alkene và alkyne có hai loại đồng phân cấu tạo là đồng phân vị trí liên kết bội (từ C4 trở lên ) và đồng phân mạch carbon (từ C4 trở lên với alkene và từ C5 trở lên với alkyne).
* Đồng phân hình học:
Trong phân tử alkene nếu mỗi nguyên tử carbon của liên kết đôi liên kết với hai nguyên tử hoặc hai nhóm nguyên tử khác nhau thì sẽ có đồng phân hình học.
c. Danh pháp
Tên theo danh pháp thay thế của alkene và alkynet là:

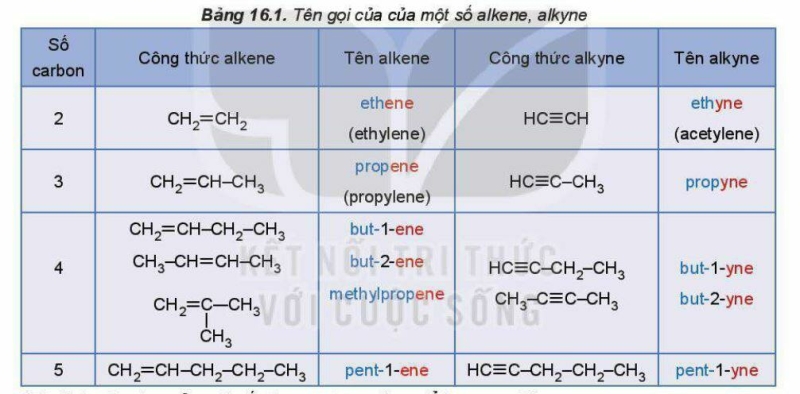
2. Đặc điểm cấu tạo của ethylene và acetylene
a. Ethylene
Phân tử ethylene (C2H4) có 2 nguyên tử carbon và 4 nguyên tử hydrogen đều nằm trên một mặt phẳng. Liên kết đôi C=C gồm một liên kết Ϭ và một liên kết π.
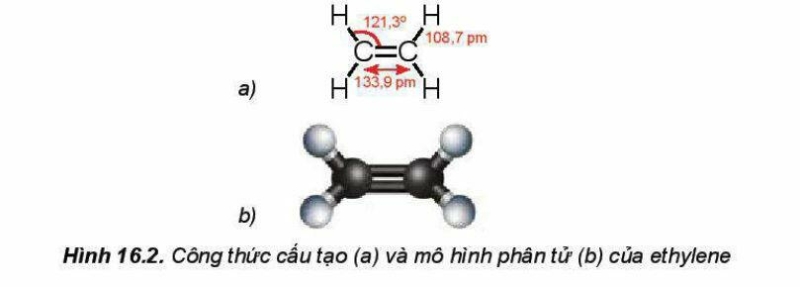
b. Acetylene
Phân tử acetylene (C2H2) có 2 nguyên tử carbon và 2 nguyên tử hydrogen nằm trên một đường thẳng, góc liên kết CCH là 180°. Liên kết ba C≡C bao gồm một liên kết Ϭ và hai liên kết π.
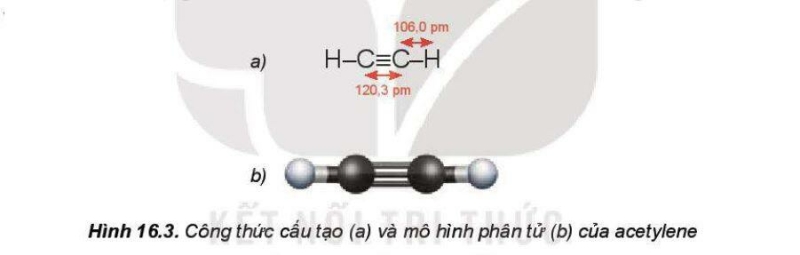
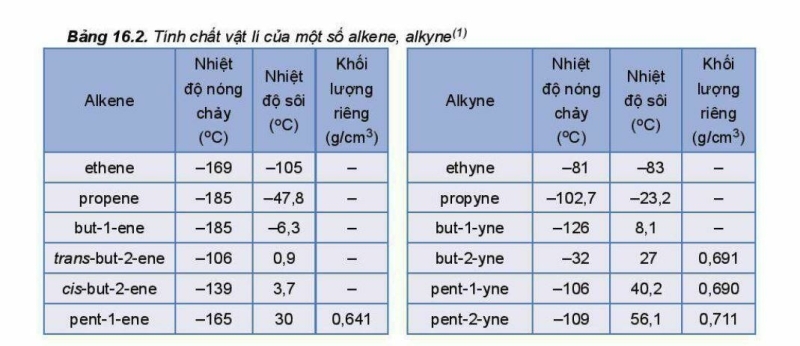
3. Tính chất vật lí
Các alkene, alkyne là những hợp chất không có mùi và đều nhẹ hơn nước.
Ở nhiệt độ thường, phần lớn các alkene và alkyne từ C2 đến C4 ở trạng thái khi, từ C5 đến C17 ở trạng thái lỏng và từ C18 trở lên ở trạng thái rắn. Chúng không tan hoặc rất it tan trong nước, tan trong một số dung môi hữu cơ.
4. Tính chất hoá học của alkene, alkyne
a. Phản ứng cộng
* Phản ứng cộng hydrogen
Hydrogen hóa alkyne, tuỳ vào điều kiện áp suất, nhiệt độ và xúc tác, có thể nhận được sản phẩm là alkene, alkane.
* Phản ứng cộng halogen
Khi cho alkene hoặc alkyne phản ứng với dung dịch bromine, dung dịch sẽ bị mất màu.
* Phản ứng cộng nước (hydrate hoá)
Phản ứng cộng nước vào alkene hay còn gọi là Hydrate hóa alkene tạo ra từ alcohol, Phản ứng thường sử dụng xúc tác phosphoric acid hoặc sulfuric acid.
CH2 = CH2 + H2O → CH3-CH2OH (điều kiện to, H3PO4)
b. Phản ứng trùng hợp của alkene
Phản ứng trùng hợp alkene là quá trình cộng hợp liên tiếp nhiều phân tử alkene giống nhau hoặc tương tự nhau (gọi là monomer) tạo thành phân tử có phân tử khối lớn (gọi là polymer).
c. Phản ứng của alk-1-yne với AgNO3, trong NH3
Các alkyne có liên kết ba ở đầu mạch (alk-1-yne) có khả năng tham gia phản ứng với dung dịch AgNO3, trong NH, tạo thành kết tủa.
d. Phản ứng oxi hóa
* Phản ứng oxi hoá không hoàn toàn
Các alkene và alkyne có khả năng làm mất màu dung dịch thuốc tím, đây là phản ứng ox hóa không hoàn toàn.
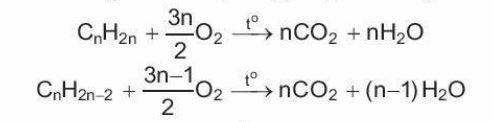
* Phản ứng cháy
Alkene và alkyne đều dễ cháy khi có mặt oxygen, phản ứng toả nhiều nhiệt:
5. Điều chế
a. Alkene
Trong phòng thí nghiệm, etylene được điều chế từ phản ứng dehydrate ethanol:
C2H5OH → C2H4 + H2O (điều kiện H2SO4 đặc, nhiệt độ)
Trong công nghiệp, alkene C2 - C4 được điều chế từ quá trình cracking alkane trong các nhà máy lọc dầu.
b. Alkyne
Acetylene được điều chế từ phản ứng giữa calcium carbide với nước:
CaC2 + 2H2O → C2H2 + Ca(OH)2
Ngoài ra, acutylene còn được điều chế bằng cách nhiệt phân methane ở nhiệt độ 1500°C, làm lạnh nhanh để tách acutylene ra khỏi hỗn hợp với hydrogen.
6. Ứng dụng
- Ethylene kích thích hoa quả mau chín.
- Công nghiệp hóa chất: sản xuất alcohol, aldehyde, ethylbenzene, cumene…
- Sản xuất dược phẩm.
- Đèn xì oxygen-acetylene.
- Tổng hợp polymer để sản xuất chất dẻo, cao su,…
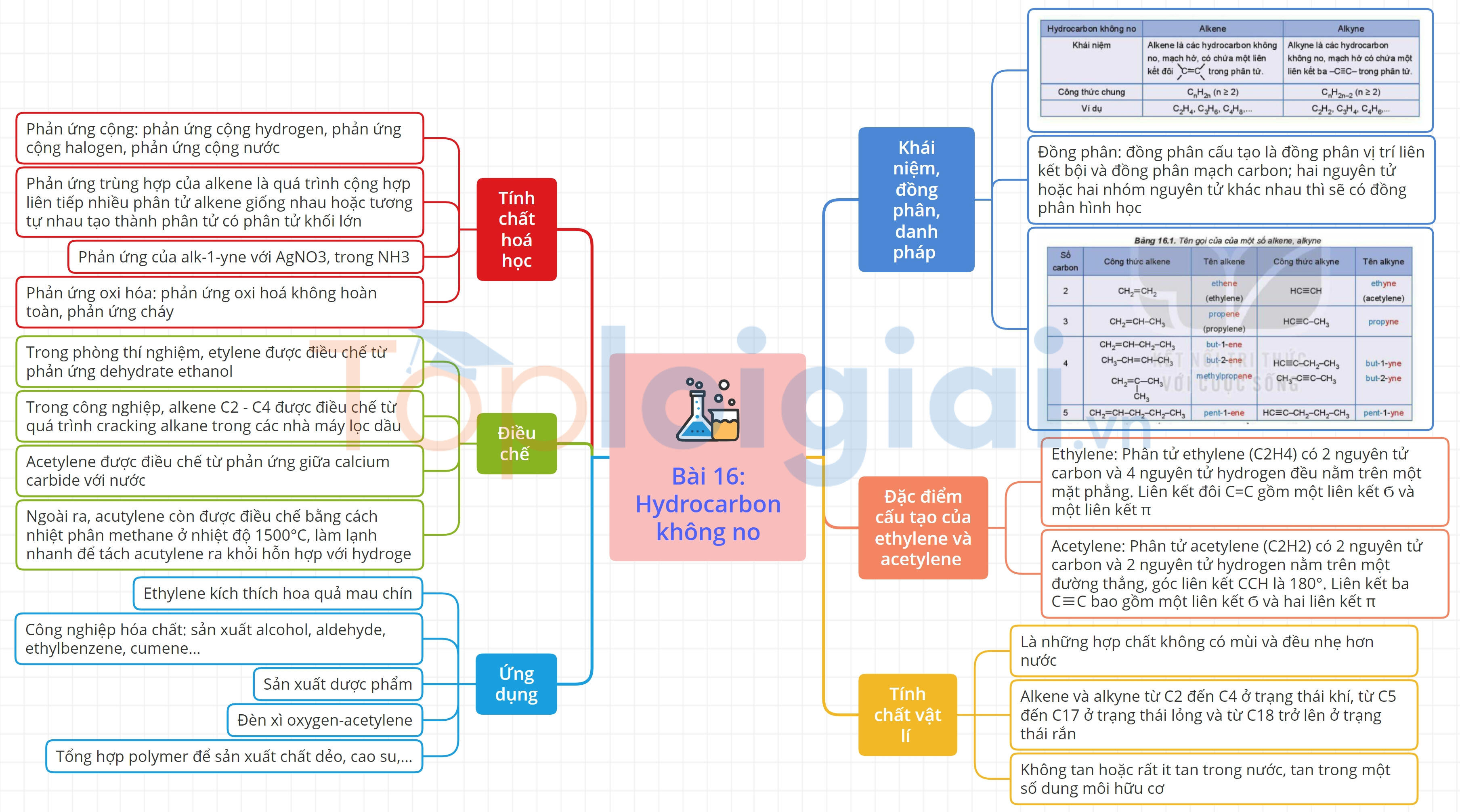
Sơ đồ tư duy Hydrocarbon không no
B. Trắc nghiệm Hydrocarbon không no
Đang cập nhật ...
Xem thêm Lý thuyết các bài Hoá học 11 Kết nối tri thức hay, chi tiết khác:
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.