Với giải Câu hỏi trang 38 SGK Hoá học10 Kết nối tri thức trong Bài 6: Xu hướng biến đổi một số tính chất của nguyên tử các nguyên tố trong một nhóm giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Hoá học 10. Mời các bạn đón xem:
Hoá học 10 Kết nối tri thức trang 38 Bài 6: Xu hướng biến đổi một số tính chất của nguyên tử các nguyên tố trong một nhóm
Hoạt động 1 trang 38 Hóa học 10: So sánh tính kim loại của sodium và magnesium
Chuẩn bị: kim loại Na, Mg, dung dịch phenolphthalein, nước, cốc thủy tinh.
Tiến hành:
- Lấy hai cốc thủy tinh, mỗi cốc có chứa khoảng 200mL nước, nhỏ tiếp vài giọt dung dịch phenolphthalein.
- Cho một mẩu nhỏ Na vào cốc (1), một dây Mg vào cốc (2).
Lưu ý: Hầu hết các kim loại kiềm phản ứng với nước mãnh liệt, chỉ sử dụng các kim loại kiềm với lượng nhỏ; cần làm sạch bề mặt dây Mg trước khi cho vào cốc (2).
Quan sát hiện tượng và trả lời các câu hỏi:
1. Viết phương trình hóa học của các phản ứng.
2. So sánh mức độ phản ứng của sodium và magnesium với nước.
Lời giải:
1. 2Na + 2H2O ⟶ 2NaOH + H2↑
Mg gần như không phản ứng.
2. Sodium phản ứng mãnh liệt với nước.
Magnesium gần như không phản ứng với nước ở nhiệt độ thường.
⇒ Sodium phản ứng với nước mãnh liệt hơn magnesium.
Hoạt động 2 trang 38 Hóa học 10: So sánh tính kim phi của chlorine và iodine
Chuẩn bị: Hình ảnh hoặc video phản ứng của nước của chlorine với dung dịch potassium iodide (∗).
Tiến hành: Quan sát hình ảnh hoặc xem video phản ứng của nước chlorine với dung dịch potassium iodide.
Câu hỏi: So sánh tính phi kim của chlorine và iodine.
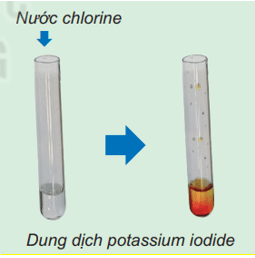
Hình 6.5. Phản ứng của nước chlorine với dung dịch potassium iodide
Lời giải:
Khi cho nước chlorine vào dung dịch potassium iodide, sau một thời gian thấy dung dịch màu vàng nâu.
⇒ Chlorine có tính phi kim mạnh hơn iodine.
Xem thêm các bài giải Hóa học lớp 10 Kết nối tri thức hay, chi tiết khác:
Hoạt động 1 trang 38 Hóa học 10: So sánh tính kim loại của sodium và magnesium...
Hoạt động 2 trang 38 Hóa học 10: So sánh tính kim phi của chlorine và iodine...
Xem thêm các bài giải SGK Hoá học lớp 10 Kết nối tri thức hay, chi tiết khác:
Bài 5: Cấu tạo của bảng tuần hoàn các nguyên tố hoá học
Bài 7: Xu hướng biến đổi thành phần và một số tính chất của hợp chất trong một chu kì
Bài 8: Định luật tuần hoàn. Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.