Với giải Câu hỏi trang 37 SGK Hoá học10 Cánh Diều Bài 6: Cấu tạo bảng tuần hoàn các nguyên tố hóa học giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Hoá học 10. Mời các bạn đón xem:
Nội dung bài viết
Hoá học 10 Cánh Diều trang 37 Bài 6: Cấu tạo bảng tuần hoàn các nguyên tố hóa học
Lời giải:
+ Với Z = 11 ta có cấu hình electron là: 1s22s22p63s1 ⇒ Là nguyên tố s.
+ Với Z = 20 ta có cấu hình electron là: 1s22s22p63s23p64s2 ⇒ Là nguyên tố s
+ Với Z = 29 ta có cấu hình electron là: 1s22s22p63s23p6 3d104s1 ⇒ thuộc nhóm B ⇒ Là nguyên tố d.
Lời giải:
Hiện nay có khoảng hơn 90 nguyên tố kim loại, gần 20 nguyên tố phi kim và 7 nguyên tố khí hiếm.
Vận dụng 3 trang 37 Hóa học 10: Hãy thu thập thông tin về các vấn đề sau:
1. Ngoài Mendeleev, còn có những nhà khoa học nào cũng có đóng góp vào việc xây dựng bảng và quy luật tuần hoàn, dù ở những mức độ khác nhau?
2. Mendeleev đã tiên đoán chi tiết về ba nguyên tố nào? Nêu cụ thể những tiên đoán đó.
3. Sưu tầm hình ảnh các bảng tuần hoàn các nguyên tố hóa học khác nhau.
Lời giải:
1. Ngoài Mendeleev, một số nhà khoa học cũng có đóng góp vào việc xây dựng bảng và quy luật tuần hoàn, ở những mức độ khác nhau như:
- Năm 1789, A. Lavoisier (La-voa-die, người Pháp) đã thực hiện xếp 33 nguyên tố hóa học thành các nhóm chất khí, kim loại, phi kim và “đất”.
- Năm 1829, J, Ư, Dobereiner (Đô-be-rai-nơ, người Đức) phân loại các nguyên tố thành các nhóm có tính chất hóa học giống nhau. Ví dụ: Lithium, sodium và potassium là nhóm các kim loại mềm, dễ phản ứng.
- Năm 1866, J Newlands (Niu-lan, người Anh) đã xếp các nguyên tố hóa học theo chiều tăng khối lượng nguyên tử thành các octave (quãng tám), trong đó nguyên tố thứ tám lặp lại tính chất của nguyên tố đầu tiên.
- Năm 1869, ngoài Mendeleev thì J.L. Meyer (May-ơ, người Đức) cũng sắp xếp các nguyên tố theo chiều tăng khối lượng nguyên tử và các hàng và cột, bắt đầu mỗi hàng (bảng của Mendeleev) hoặc cột mới (bảng của Mayer) khi các tính chất của nguyên tố bắt đầu lặp lại.
2. Nhờ định luật tuần hoàn của mình, 3 nguyên tố Sc, Ga và Ge đã được Mendeleev tiên đoán khá tỉ mỉ về tính chất của đơn chất và hợp chất của chúng.
- Năm 1871, Mendeleev đã dự đoán một nguyên tố hóa học cùng “nhóm của nhôm”, có nguyên tử lượng (nguyên tử khối) khoảng 68, tỉ trọng là 5,9 – 6,0.
Đến năm 1875, một nhà khoa học người Pháp đã tạo ra được một nguyên tố mới trong quặng kẽm trắng và đặt tên là Galium (Ga). Sau một thời gian nghiên cứu chính xác, nhà khoa học người Pháp này đã kết luận các chỉ số của nguyên tố Gali đúng như những dự đoán của Mendeleev.
- Năm 1871, Mendeleev đã dự đoán một nguyên tố hóa học nằm trong “nhóm của Bo”.
Đến năm 1879, tại Thụy Điển người ta đã sử dụng phương pháp phân tích quang phổ và tìm thấy một nguyên tố mới trong các khoáng chất euxenit và gadolinit. Nguyên tố này được đặt tên là Scandium (Sc), nó có những tính chất hóa học phù hợp với dự đoán của Mendeleev.
- Năm 1871, germanium (Ge) là một trong các nguyên tố mà Mendeleev dự đoán tồn tại như là nguyên tố tương tự nhưng còn thiếu của nhóm silic (Mendeleev gọi nó là "eka-silicon"). Sự tồn tại của nguyên tố này được Clemens Winkler (nhà hóa học người Đức) chứng minh năm 1886.
3. Một số hình ảnh các bảng tuần hoàn các nguyên tố hóa học khác nhau:
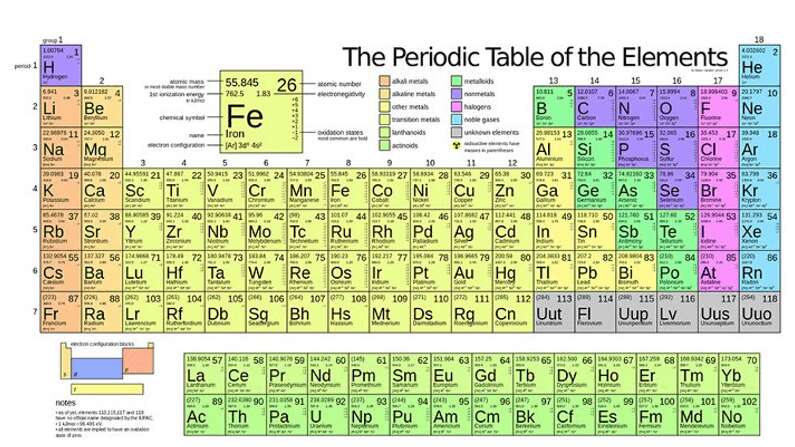
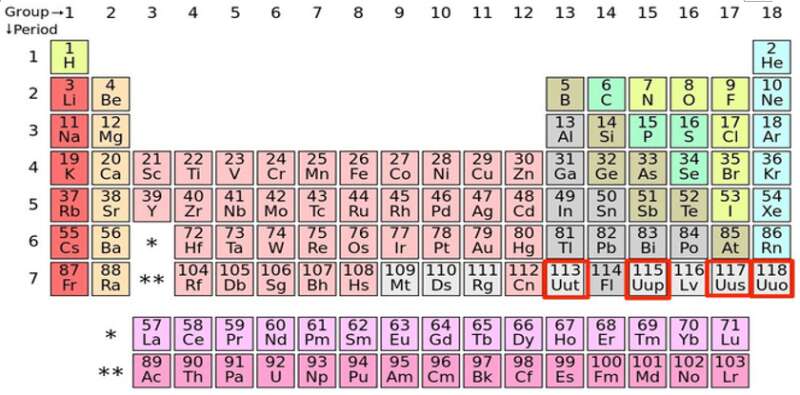
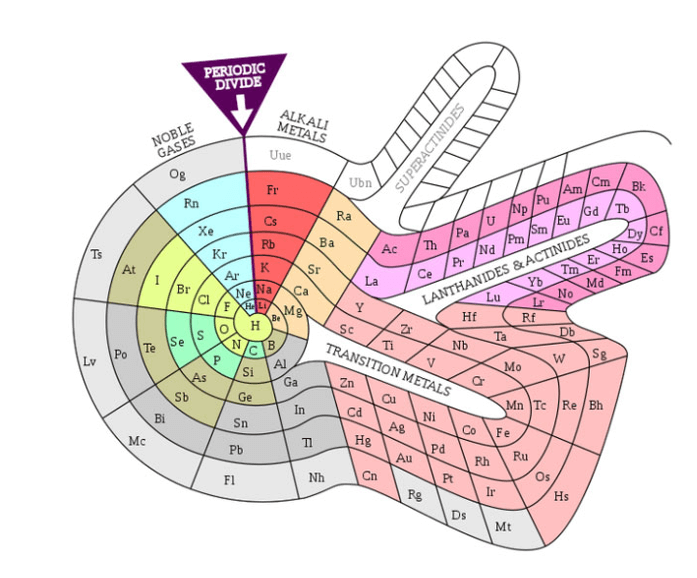
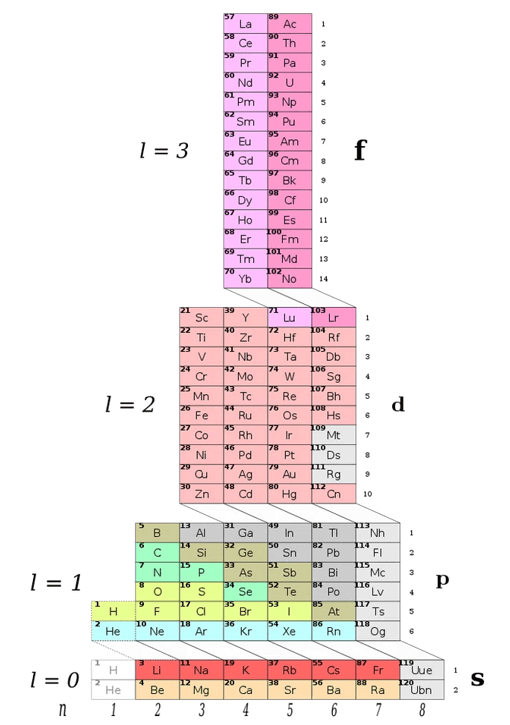
A. khối lượng nguyên tử
B. cấu hình electron
C. số hiệu nguyên tử
D. số khối
Lời giải:
Đáp án A
Mendeleev sắp xếp các nguyên tố hóa học vào bảng tuần hoàn dựa theo quy luật về khối lượng nguyên tử.
Định luật tuần hoàn của Mendeleev được phát biểu như sau: “Tính chất của các đơn chất, cấu tạo và tính chất các hợp chất của chúng có tính tuần hoàn theo khối lượng nguyên tử của các nguyên tố”
Bài 2 trang 37 Hóa học 10: Nguyên tố X và Y có số hiệu nguyên tử lần lượt là 21 và 35. Viết cấu hình electron, từ đó xác định vị trí của X, Y (số thứ tự của ô nguyên tố, chu kì và nhóm) trong bảng tuần hoàn.
Lời giải:
- Cấu hình electron của nguyên tố X (Z = 21) là: 1s22s22p63s23p6 3d14s2
+ Số hiệu nguyên tử = số thứ tự ô nguyên tố X = 21.
+ Có 4 lớp electron ⇒ X thuộc chu kì 4
+ Cấu hình electron lớp ngoài cùng và sát ngoài cùng là 3d14s2 ⇒ Thuộc nhóm IIIB
- Cấu hình electron của nguyên tố Y (Z = 35) là: 1s22s22p63s23p6 3d104s24p5
+ Số hiệu nguyên tử = số thứ tự ô nguyên tố Y = 35.
+ Có 4 lớp electron ⇒ Y thuộc chu kì 4
+ Có 7 electron lớp ngoài cùng ⇒ Thuộc nhóm VIIA.
Bài 3 trang 37 Hóa học 10: Bằng cách viết cấu hình electron, hãy xác định trong các nguyên tố thuộc chu kì 2 trong bảng tuần hoàn, những nguyên tố nào thuộc khối s, những nguyên tố nào thuộc khối p.
Lời giải:
Chu kì 2 gồm các nguyên tố có số hiệu nguyên tử từ 3 đến 10.
|
Số hiệu nguyên tử (Z) |
Cấu hình electron |
Phân loại nguyên tố |
|
3 |
1s22s1 |
Nguyên tố s |
|
4 |
1s22s2 |
Nguyên tố s |
|
5 |
1s22s22p1 |
Nguyên tố p |
|
6 |
1s22s22p2 |
Nguyên tố p |
|
7 |
1s22s22p3 |
Nguyên tố p |
|
8 |
1s22s22p4 |
Nguyên tố p |
|
9 |
1s22s22p5 |
Nguyên tố p |
|
10 |
1s22s22p6 |
Nguyên tố p |
Xem thêm các bài giải Hóa học lớp 10 Cánh Diều hay, chi tiết khác:
Câu hỏi 1 trang 32 Hóa học 10: Mendeleev sắp xếp 9 nguyên tố như bảng 6.1 theo những nguyên tắc nào?...
Câu hỏi 4 trang 34 Hóa học 10: Hãy cho biết những thông tin thu được từ ô nguyên tố vanadium...
Luyện tập 2 trang 35 Hóa học 10: Từ cấu hình electron của Fe là 1s22s22p63s23p63d64s2. Hãy xác định vị trí của Fe trong bảng tuần hoàn...
Vận dụng 3 trang 37 Hóa học 10: Hãy thu thập thông tin về các vấn đề sau...
Xem thêm các bài giải Hoá học lớp 10 Cánh Diều hay, chi tiết khác:
Bài 5: Lớp, phân lớp và cấu hình electron
Bài 8: Định luật tuần hoàn và ý nghĩa của bảng tuần hoàn các nguyên tố hóa học
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.