Toptailieu biên soạn và sưu tầm lời giải bài tập Hóa học lớp 10 Bài 10: Liên kết ion sách Cánh Diều hay, chi tiết sẽ giúp học sinh dễ dàng trả lời câu hỏi Hóa học 10 Bài 10 từ đó học tốt môn Hóa học 10.
Nội dung bài viết
Hoá học 10 Cánh Diều Bài 10: Liên kết ion
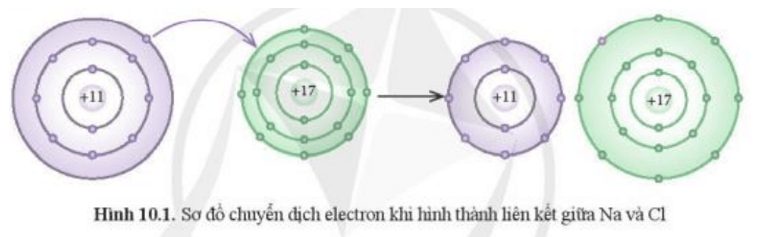
Mở đầu trang 53 Hóa học 10: Phát biểu nào dưới đây phù hợp với sơ đồ phản ứng ở Hình 10.1?
(1) Nguyên tử Na nhường, nguyên tử Cl nhận electron để trở thành các ion.
(2) Nguyên tử Na và Cl góp chung electron để trở thành các ion.
Lời giải:
Phát biểu đúng:
(1) Nguyên tử Na nhường, nguyên tử Cl nhận electron để trở thành các ion.
Cụ thể:
+ Nguyên tử Na (Z = 11) nhường đi 1 electron ở lớp ngoài cùng trở thành ion mang điện tích dương, kí hiệu là Na+.
+ Nguyên tử Cl (Z = 17) nhận 1 electron từ nguyên tử Na trở thành ion mang điện tích âm, kí hiệu là Cl-.
Các ion Na+ và Cl- hút nhau tạo thành liên kết trong phân tử NaCl.
Câu hỏi 1 trang 53 Hóa học 10: Phát biểu nào sau đây là đúng?
a) Liên kết ion chỉ có trong đơn chất.
b) Liên kết ion chỉ có trong hợp chất.
c) Liên kết ion có trong cả đơn chất và hợp chất.
Lời giải:
Phát biểu đúng là b) Liên kết ion chỉ có trong hợp chất.
Vì liên kết ion được hình thành bởi lực hút tĩnh điện giữa các ion mang điện tích trái dấu. Chỉ trong hợp chất mới có các ion mang điện tích trái dấu.
Luyện tập 1 trang 54 Hóa học 10: Hãy nêu một số hợp chất ion:
a) Tạo nên bởi các ion đơn nguyên tử.
b) Tạo nên bởi ion đơn nguyên tử và ion đa nguyên tử.
c) Tạo nên bởi các ion đa nguyên tử.
Lời giải:
a) Hợp chất ion tạo nên bởi ion đơn nguyên tử: NaCl, KF, BaCl2 ….
Na+ + Cl- → NaCl
K+ + F- → KF
Ba2+ + 2Cl- → BaCl2
b) Hợp chất ion tạo nên bởi ion đơn nguyên tử và ion đa nguyên tử: NaNO3; K2SO4; CaCO3; NH4Cl …
Na+ + NO3- → NaNO3
2K+ + SO42- → K2SO4
Ca2+ + CO32- → CaCO3
NH4+ + Cl- → NH4Cl
c) Tạo nên bởi các ion đa nguyên tử
2NH4+ + SO42- → (NH4)2SO4
NH4+ + NO3- → NH4NO3
Lời giải:
Giai đoạn 1: Hình thành các ion trái dấu từ các quá trình Ca nhường electron và O nhận electron.

Giai đoạn 2: Hai ion trái dấu Ca2+ và O2- hút nhau bằng lực hút tĩnh điện tạo nên hợp chất ion.
Ca2+ + O2- → CaO
Luyện tập 2 trang 54 Hóa học 10: Cho các ion: Li+, Ca2+, Al3+, F-, O2-, PO43-. Hãy viết công thức tất cả các hợp chất ion (tạo nên từ một loại cation và một loại anion) có thể được tạo thành từ các ion đã cho. Biết rằng tổng điện tích của các ion trong hợp chất bằng 0.
Lời giải:
Công thức các hợp chất ion có thể tạo thành là: LiF, Li2O, Li3PO4, CaF2, CaO, Ca3(PO4)2, AlF3, Al2O3, AlPO4.
Li+ + F- → LiF
2Li+ + O2- → Li2O
3Li+ + PO43- → Li3PO4
Ca2+ + 2F- → CaF2
Ca2+ + O2- → CaO
3Ca2+ + 2PO43- → Ca3(PO4)2
Al3+ + 3F- → AlF3
2Al3+ + 3O2- → Al2O3
Al3+ + PO43- → AlPO4
Luyện tập 3 trang 54 Hóa học 10: Cho các chất sau: SiO2 là thành phần chính của thạch anh, CaCO3 là thành phần của đá vôi. Hãy cho biết chất nào được tạo nên bởi liên kết ion? Giải thích.
Lời giải:
CaCO3 được tạo nên bởi liên kết ion.
Ca2+ + CO32- → CaCO3
Si và O đều là hai nguyên tố phi kim nên không tạo được ion trái dấu. Si và O sẽ góp chung electron để hình thành liên kết cộng hóa trị.
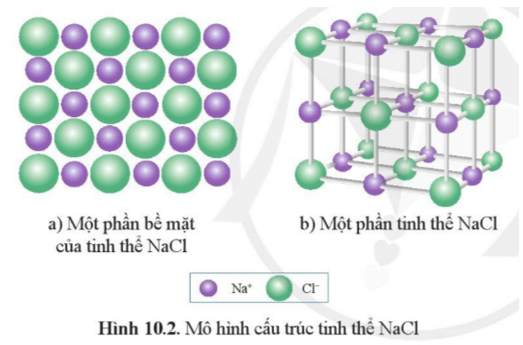
Lời giải:
Học sinh lắp ráp mô hình tinh thể NaCl từ các quả cầu (hoặc đất nặn) minh họa cho ion Na+, Cl- và que nối.

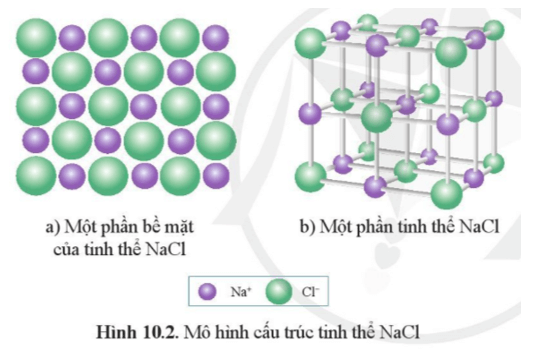
Lời giải:
Từ mô hình tinh thể NaCl xác định được, xung quanh mỗi ion Na+ có 6 ion Cl- (ở gần nhất với Na+).
Lời giải:
Một số hợp chất ion có xung quanh em:
NaCl (muối ăn) điều kiện thường tồn tại ở thể rắn.
CaO (vôi sống) điều kiện thường tồn tại ở thể rắn.
CaCO3 (đá vôi) điều kiện thường tồn tại ở thể rắn.
(a) cộng hóa trị.
(b) ion.
(c) có công thức Al2O3
(d) có công thức Al3O2
Lời giải:
Đáp án đúng là: (b) ion.
Hai ion Al3+ và O2- trái dấu hút nhau bằng lực hút tĩnh điện tạo hợp chất Al2O3
2Al3+ + 3O2- → Al2O3
⇒ Hợp chất tạo nên bởi ion Al3+ và O2- là hợp chất ion.
Bài 2 trang 56 Hóa học 10: Những tính chất nào sau đây là tính chất điển hình của hợp chất ion?
(a) Tồn tại ở thể khí trong điều kiện thường.
(b) Có nhiệt độ nóng chảy và nhiệt độ sôi cao.
(c) Thường tồn tại ở thể rắn trong điều kiện thường.
(d) Có nhiệt độ nóng chảy và nhiệt độ sôi thấp.
Lời giải:
Những tính chất là tính chất điển hình của hợp chất ion:
(b) Có nhiệt độ nóng chảy và nhiệt độ sôi cao.
(c) Thường tồn tại ở thể rắn trong điều kiện thường.
b) Vì sao cả Na2O và MgO đều là chất rắn ở điều kiện thường?
c) Vì sao nhiệt độ nóng chảy của MgO (2 852oC) cao hơn rất nhiều so với Na2O (1 132oC)?
Lời giải:
a) Nguyên tử kim loại có 1, 2, 3 electron lớp ngoài cùng, có xu hướng nhường 1, 2, 3 electron này để đạt cấu hình bền vững giống như khí hiếm. Khi nhường electron các ion kim loại mất đi 1 lớp electron ngoài cùng. Do đó bán kính ion kim loại nhỏ hơn bán kính nguyên tử kim loại tương ứng.
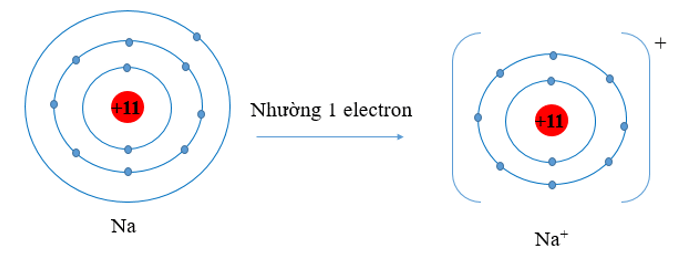
- Nguyên tử Na có 3 lớp electron, 1 electron lớp ngoài cùng. Nguyên tử Na đã nhường đi 1 electron ở lớp thứ 3 để trở thành ion Na+. Khi đó ion Na+ chỉ còn 2 lớp electron
⇒ Bán kính Na+ nhỏ hơn bán kính nguyên tử Na.
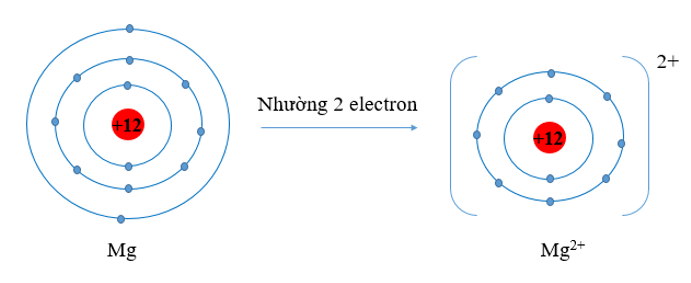
- Nguyên tử Mg có 3 lớp electron, 2 electron lớp ngoài cùng. Nguyên tử Mg đã nhường đi 2 electron ở lớp thứ 3 để trở thành ion Mg2+. Khi đó ion Mg2+ chỉ còn 2 lớp electron
⇒ Bán kính Mg2+ nhỏ hơn bán kính nguyên tử Mg2+.
b) Mỗi nguyên tử Na đã nhường 1 electron, nguyên tử O nhận 2 electron từ nguyên tử Na để hình thành hợp chất ion Na2O.
2Na+ + O2- → Na2O
Vì Na2O là hợp chất ion ⇒ Ở điều kiện thường Na2O tồn tại ở thể rắn.
Nguyên tử Mg nhường 2 electron, nguyên tử O nhận 2 electron từ nguyên tử Mg để hình thành hợp chất ion MgO.
Mg2+ + O2- → MgO
Vì MgO là hợp chất ion ⇒ Ở điều kiện thường MgO tồn tại ở thể rắn.
c) Ta có:
+ Bán kính ion Na+ > bán kính ion Mg2+
+ Điện tích ion Mg2+ > điện tích ion Na+
Vậy nhiệt độ nóng chảy của MgO (2852oC) cao hơn rất nhiều so với Na2O (1132oC) do năng lượng phân li tỉ lệ thuận với điện tích ion và tỉ lệ nghịch với bán kính ion.
Xem thêm các bài giải Hoá học lớp 10 Cánh Diều hay, chi tiết khác:
Bài 12: Liên kết hydrogen và tương tác Van Der Waals
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.