Toptailieu.vn biên soạn và giới thiệu lời giải Hoá học 11 (Cánh diều) Bài 13: Hydrocarbon không no hay, chi tiết sẽ giúp học sinh dễ dàng trả lời câu hỏi từ đó học tốt môn Hoá học 11.
Nội dung bài viết
Hoá học 11 (Cánh diều) Bài 13: Hydrocarbon không no
Lời giải:
- Hydrocarbon no: ethane (CH3 – CH3).
- Hydrocarbon không no: ethane (CH2 = CH2) và ethyne (CH ≡ CH).
Câu hỏi 1 trang 82 Hóa học 11: Cho công thức cấu tạo của các chất dưới đây: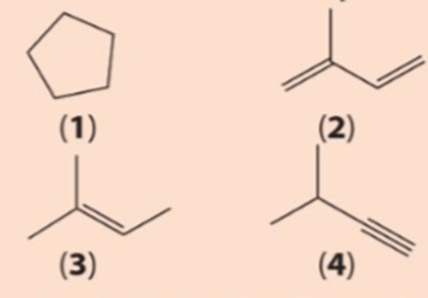
a) Viết công thức phân tử của các chất trên.
b) Cho biết trong các chất trên, chất nào là hydrocarbon không no, chất nào là alkene, chất nào là alkyne.
Lời giải:
a) Công thức phân tử các chất:
(1) C5H10;
(2) C5H8;
(3) C5H10;
(4) C5H8.
b) Chất là hydrocarbon không no: (2); (3); (4).
Chất là alkene: (3).
Chất là alkyne: (4).
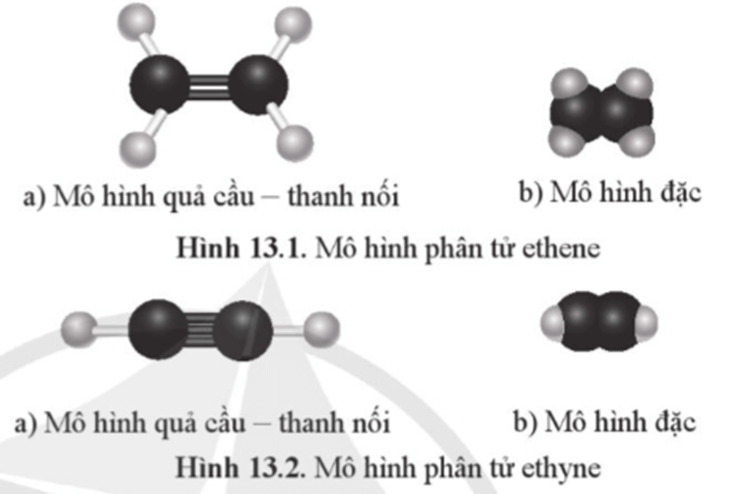
Lời giải:
Dạng hình học của phân tử ethene: hai nguyên tử C và 4 nguyên tử H đều nằm cùng trên một mặt phẳng (gọi là mặt phẳng phân tử), các góc hầu như bằng nhau và gần bằng 120o.
Dạng hình học của phân tử ethyne: C mang liên kết ba và 2 nguyên tử H liên kết trực tiếp với chúng nằm trên cùng một đường thẳng.
Lời giải:
Công thức cấu tạo của các alkene có công thức phân tử C4H8:
(1) CH2 = CH – CH2 – CH3.
(2) CH3 – CH = CH – CH3.
(3) 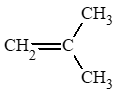
- Các chất là đồng phân mạch carbon: (1) và (3); (2) và (3).
- Các chất là đồng phân vị trí liên kết đôi: (1) và (2).
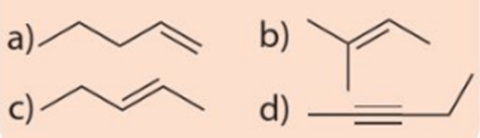
Lời giải:
a)
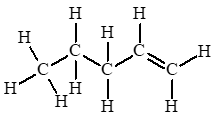
b)
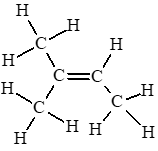
c) Đồng phân cis –
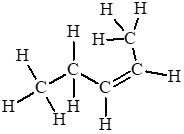
Đồng phân trans –
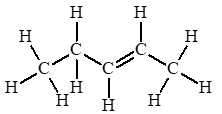
d)
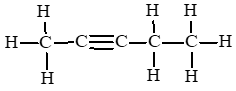
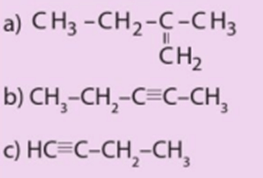
Luyện tập 2 trang 83 Hóa học 11: Gọi tên các chất có công thức cấu tạo sau:
Lời giải:
Tên gọi các chất lần lượt là:
a) 2 – methylbut – 1 – ene.
b) pent – 2 – yne.
c) but – 1 – yne.
Lời giải:
Dựa vào khối lượng riêng và độ tan của các chất, xác định được như sau:
- Khi cho hex – 1 – ene vào ống nghiệm chứa nước xảy ra sự phân lớp, trong đó hex – 1 – ene ở lớp trên và nước ở lớp dưới do hex – 1 – ene không tan trong nước và nhẹ hơn nước.
- Khi cho hex – 1 – ene vào ống nghiệm chứa chloroform không có sự phân lớp do hex – 1 – ene tan trong chloroform.ư
Lời giải:
Liên kết đôi C = C gồm 1 liên kết σ và 1 liên kết π.
Năng lượng liên kết của liên kết C – C là khoảng 368 kJ mol-1 (liên kết σ).
Vậy năng lượng liên kết của liên kết π vào khoảng 636 – 368 = 268 kJ mol-1.
Vậy liên kết π dễ bị bẻ gãy hơn khi phân tử tham gia phản ứng.
Lời giải:
Các alkene, alkyne mà khi hydrogen hoá tạo thành butane là:
CH2 = CH – CH2 – CH3: but – 1 – ene.
CH3 – CH = CH – CH3: but – 2 – ene.
CH ≡ C – CH2 – CH3: but – 1 – yne.
CH3 – C ≡ C – CH3: but – 2 – yne.
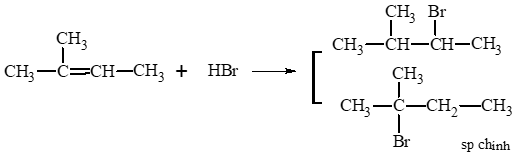
a) 2 – methylbut – 2 – ene phản ứng với HBr.
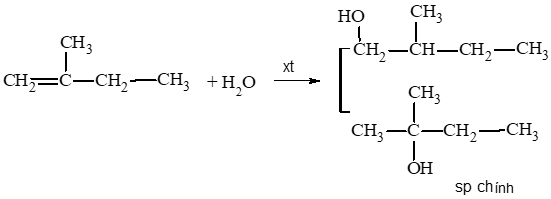
b) 2 – methylbut – 1 – ene phản ứng với nước (xúc tác H2SO4).
Lời giải:
a)
b)
Câu hỏi 6 trang 87 Hóa học 11: Viết phương trình hoá học của phản ứng trùng hợp propene.
Lời giải:
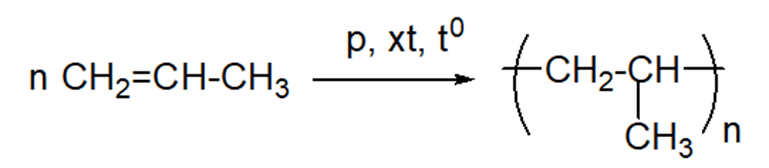
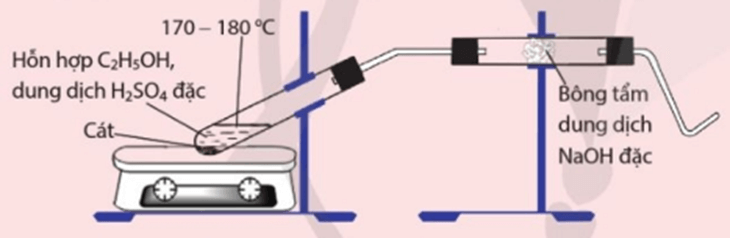
Thí nghiệm 1 trang 89 Hóa học 11: Điều chế và thử tính chất của ethylene
Chuẩn bị: Ethanol, dung dịch sulfuric acid đặc, nước bromine, dung dịch KMnO4 1%, dung dịch NaOH đặc; ống nghiệm, giá thí nghiệm, ống dẫn khí hình chữ L, ống dẫn khí hình chữ Z có một đầu được vuốt nhọn, đèn cồn, bông.
Tiến hành: Cho 2 mL ethanol vào ống nghiệm khô, thêm dần từng giọt 4 mL dung dịch sulfuric acid đặc (cho chảy dọc theo thành ống nghiệm), lắc đều. Cho vào ống nghiệm một ít cát hoặc 1 – 2 mảnh sứ xốp. Kẹp ống nghiệm lên giá và lắp với ống dẫn khí hình chữ L qua phần ống nối có mẩu bông tẩm dung dịch NaOH đặc. Đun nóng ống nghiệm và sục ống dẫn khí vào ống nghiệm có chứa khoảng 1 mL nước bromine. Khi nước bromine bị mất màu thì thay ống nghiệm bằng ống nghiệm khác có chứa 1 mL dung dịch KMnO4 1%. Khi màu tím biến mất thì thay ống dẫn khí hình chữ L bằng ống dẫn khí hình chữ Z (đầu được vuốt nhọn hướng lên phía trên) và đốt khí thoát ra ở đầu ống dẫn khí.
Yêu cầu: Quan sát, viết phương trình hoá học và giải thích hiện tượng xảy ra.
Chú ý an toàn: Ethanol dễ bắt lửa và cháy; sulfuric acid và dung dịch NaOH đặc phá huỷ vải, da,... khi tiếp xúc.
Lời giải:
Hiện tượng: có khí sinh ra, khí này làm mất màu dung dịch bromine, làm mất màu thuốc tím. Đốt khí thoát ra ở đầu ống dẫn khí, thấy khí cháy và toả nhiều nhiệt.
Phương trình hoá học giải thích hiện tượng:
C2H5OH CH2 = CH2 + H2O
CH2 = CH2 + Br2 → CH2Br – CH2Br
3CH2 = CH2 + 2KMnO4 + 4H2O → 3HO – CH2 – CH2 – OH + 2MnO2 + 2KOH
C2H4 + 3O2 2CO2 + 2H2O.
Đun ethanol với sulfuric acid đặc sinh ra khí ethylene; dẫn tiếp khí qua ống nghiệm đựng Br2 (hoặc thuốc tím) thấy dung dịch Br2 (hoặc dung dịch KMnO4) nhạt dần đến mất màu do liên kết pi ở liên kết đôi của ethylene kém bền vững.
Thí nghiệm 2 trang 89 Hóa học 11: Điều chế và thử tính chất của acetylene
Chuẩn bị: Đất đèn (thành phần chính là calcium carbide), nước bromine, dung dịch KMnO4 1%; ống nghiệm, giá thí nghiệm, ống dẫn khí hình chữ L, ống dẫn khí hình chữ Z có một đầu được vuốt nhọn.
Tiến hành: Cho 2 mL nước vào ống nghiệm, thêm vào đó vài viên đất đèn bằng hạt ngô, rồi đậy nhanh ống nghiệm bằng nút có gắn ống dẫn khí hình chữ L. Sục ống dẫn khí vào ống nghiệm có chứa khoảng 1 mL nước bromine, khi nước bromine bị mất màu thì thay ống nghiệm bằng ống nghiệm khác có chứa 1 mL dung dịch KMnO4 1%. Khi màu tím biến mất thì thay ống dẫn khí hình chữ L bằng ống dẫn khí hình chữ Z (đầu được vuốt nhọn hướng lên phía trên) và đốt khí thoát ra ở đầu ống dẫn khí.
Yêu cầu: Quan sát, viết phương trình hoá học và giải thích hiện tượng xảy ra.
Lời giải:
Hiện tượng: Đất đèn (thành phần chính CaC2) tác dụng với nước sinh ra khí acetylene (C2H2). Dẫn acetylene vào các ống nghiệm chứa dung dịch KMnO4 và nước Br2 thấy các dung dịch này nhạt dần đến mất màu do liên kết pi ở acetylene kém bền vững.
Khi đốt acetylene cháy, toả nhiều nhiệt.
Phương trình hoá học minh hoạ:
CaC2 + 2H2O → Ca(OH)2 + C2H2
CH ≡ CH + 2Br2 → CHBr2 – CHBr2
3CH ≡ CH + 8KMnO4 → 3KOOC – COOK + 8MnO2 + 2KOH + 2H2O
Lời giải:
Đánh số thứ tự từng lọ mất nhãn, trích mỗi lọ một ít sang ống nghiệm đánh số tương ứng.
Sử dụng dung dịch AgNO3/ NH3 (dung dịch silver nitrate trong ammonia) làm thuốc thử.
Nếu xuất hiện kết tủa vàng → hex – 1 – yne. Phương trình hoá học:
CH3[CH2]3C ≡ CH + Ag(NH3)2OH → CH3[CH2]3C ≡ CAg + 2NH3 + H2O.
Không có hiện tượng gì xuất hiện → hex – 2 – yne.
Lời giải:
- Phản ứng cháy hoàn toàn của alkane:
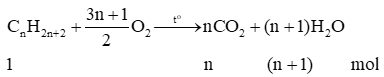
Trong phản ứng đốt cháy hoàn toàn alkane:
- Phản ứng cháy hoàn toàn của alkene:
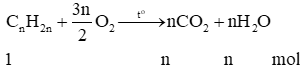
Trong phản ứng đốt cháy hoàn toàn alkene:
- Phản ứng đốt cháy hoàn toàn alkyne:
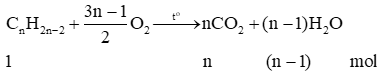
Trong phản ứng đốt cháy hoàn toàn alkene:
a) Viết phương trình hoá học của phản ứng xảy ra.
b) Vì sao cần dẫn khí từ ống nghiệm điều chế ethylene qua ống có chứa mẩu bông tẩm dung dịch NaOH đặc?
Lời giải:
a) Phương trình hoá học của phản ứng xảy ra:
C2H5OH CH2 = CH2 + H2O
b) Khí ethylene sinh ra có thể có lẫn các tạp chất như CO2, SO2… bông tẩm dung dịch NaOH đặc có tác dụng loại bỏ các tạp chất này.
Phương trình hoá học minh hoạ:
CO2 + 2NaOH → Na2CO3 + H2O
SO2 + 2NaOH → Na2SO3 + H2O.

Lời giải:
Rau khi bày bán trong các siêu thị thường được chứa trong các túi nylon có lỗ để giảm bớt tích tụ khí ethylene trong túi rau, giúp rau tươi lâu hơn.
Bài 1 trang 91 Hóa học 11: Viết công thức cấu tạo của các chất có tên dưới đây:
a) pent – 2 – ene
b) 2 – methylbut – 2 – ene
c) 3 – methylbut – 1 – yne
d) 2 – methylpropene
Lời giải:
a) pent – 2 – ene: CH3 – CH = CH – CH2 – CH3.
b) 2 – methylbut – 2 – ene: 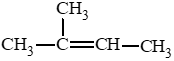
c) 3 – methylbut – 1 – yne: 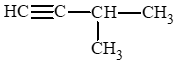
d) 2 – methylpropene: 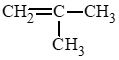
a) CH ≡ CH + 2H2
b) CH3 – C ≡ CH + 2HBr →
c) CH ≡ CH + 2Br2 →
Lời giải:
a) CH ≡ CH + 2H2 CH3 – CH3.
b) CH3 – C ≡ CH + 2HBr → CH3 – CBr2 – CH3.
c) CH ≡ CH + 2Br2 → CHBr2 – CHBr2.
Lời giải:
Dẫn lần lượt từng khí qua ống nghiệm chứa dung dịch AgNO3/ NH3 (dung dịch silver nitrate trong ammonia):
- Nếu có kết tủa vàng xuất hiện → khí acetylene.
CH ≡ CH + 2[Ag(NH3)2]OH → CAg ≡ CAg + 4NH3 + 2H2O.
- Không có hiện tượng xuất hiện là ethane, ethylene (nhóm I).
Dẫn lần lượt từng khí ở nhóm I vào ống nghiệm chứa dung dịch bromine:
- Nếu dung dịch bromine nhạt dần đến mất màu → ethylene.
CH2 = CH2 + Br2 → CH2Br – CH2Br.
- Không có hiện tượng xuất hiện → ethane.
Bài 4 trang 91 Hóa học 11: Cho các đoạn mạch polymer như ở dưới đây:
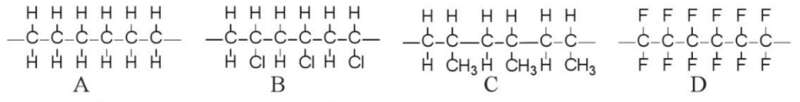
Viết phương trình hoá học tổng hợp các polymer ấy từ các alkene tương ứng.
Lời giải:
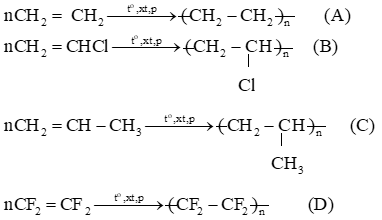
Lời giải:
- Có thể sử dụng methyl alcohol, cyclohexane làm dung môi cho phản ứng trùng hợp ethylene do các dung môi này hoà tan ethylene nhưng không hoà tan PE.
- Không sử dụng nước làm dung môi cho phản ứng trùng hợp ethylene do nước không hoà tan ethylene.
- Không sử dụng hex – 1 – ene làm dung môi cho phản ứng trùng hợp do có thể tạo ra polime khác PE.
Xem thêm các bài giải Hoá học 11 Cánh diều hay, chi tiết khác:
Hoá học 11 (Cánh diều) Bài 11 : Cấu tạo hoá học của hợp chất hữu cơ
Hoá học 11 ( Cánh diều ) Bài 12: Alkane
Hoá học 11 (Cánh diều) Bài 14: Arene (Hydrocarbon thơm)
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.