Toptailieu.vn xin giới thiệu Lý thuyết Sulfur và sulfur dioxide (Kết nối tri thức) hay, chi tiết | Lý thuyết Hóa học 11. Bài viết gồm phần lý thuyết trọng tâm nhất được trình bày một cách dễ hiểu, dễ nhớ bên cạnh đó là bộ câu hỏi trắc nghiệm có hướng dẫn giải chi tiết để học sinh có thể vận dụng ngay lý thuyết, nắm bài một cách hiệu quả nhất. Mời các bạn đón xem:
Lý thuyết Sulfur và sulfur dioxide (Kết nối tri thức) hay, chi tiết | Lý thuyết Hóa học 11
Bài giải Bài 7: Sulfur và sulfur dioxide
A. Lý thuyết Sulfur và sulfur dioxide
I. Sulfur
1. Trạng thái tự nhiên
- Là nguyên tố phổ biến thứ 17 trên vỏ TĐ.
- Trong tự nhiên, sulfur tồn tại ở cả dạng đơn chất và hợp chất.
2. Cấu tạo nguyên tử, phân tử
a, Cấu tạo nguyên tử
- Vị trí trong BTH:
+ Ô: 16.
+ Chu kì: 3.
+ Nhóm: VIA.
- Sulfur có tính phi kim.
- Số oxi hóa: -2, 0, +4, +6.
b, Cấu tạo phân tử
Phân tử sulfur gồm 8 nguyên tử (S8) có dạng vòng khép kín.
Mỗi nguyên tử sulfur liên kết với hai nguyên tử bên cạnh bằng hai liên kết CHT không phân cực.
3. Tính chất vật lí
- Có hai dạng thù hình: dạng tà phương và dạng đơn tà.
- Sulfur không tan trong nước, ít tan trong alcohol, tan nhiều trong carbon disulfide.
4. Tính chất hóa học
a, Tác dụng với hydrogen và kim loại
- Tác dụng với hydrogen
S(s) +H2(g) H2S(g)
- Tác dụng với kim loại tạo ra muối sulfide
Hg + S → HgS
2Al + 3S → Al2S3
b, Tác dụng với phi kim
S + 3F2 → SF6
S + O2 → SO2
5. Ứng dụng
- Lưu hóa cao su.
- Sản xuất sulfuric acid.
- Sản xuất thuốc trừ sâu, thuốc diệt nấm.
II. Sulfur dioxide
1. Tính chất vật lí
- SO2 là chất khí không màu, năng hơn không khí, mùi hắc, tan nhiều trong nước.
- SO2 là khí độc.
2. Tính chất hóa học
a, Tính oxi hóa
- Tác dụng với hydrogen sulfide: SO2 + 2H2S → 3S + 2H2O
b, Tính khử
- Tác dụng với nitrogen dioxide (NO2): SO2 + NO2 →SO3 + NO
3. Ứng dụng
- Là chất trung gian quan trọng trong quá trình sản xuất sulfuric acid.
- Tẩy trắng và diệt khuẩn.
- Là dung môi để thực hiện nhiều phản ứng.
4. Sulfur dioxide và ô nhiễm môi trường
a, Nguồn phát sinh
- Tự nhiên: khí thải núi lửa …
- Nhân tạo: đốt cháy nhiên liệu, quặng sulfide, luyện kim ….
b, Tác hại
- Gây ô nhiễm khí quyển, gây mưa acid và viêm đường hô hấp ở người.
c, Biện pháp cắt giảm phát thải sulfur dioxide vào khí quyển
- Tăng cường sử dụng các nguồn năng lượng mới, năng lượng sạch, năng lượng tái tạo.
- Sử dụng tiết kiệm, hiệu quả nguồn tài nguyên thiên nhiên.
- Cải tiến công nghệ sản xuất, có biện pháp xử lí khí thải và tái chế các sản phẩm phụ có chứa sulfur.
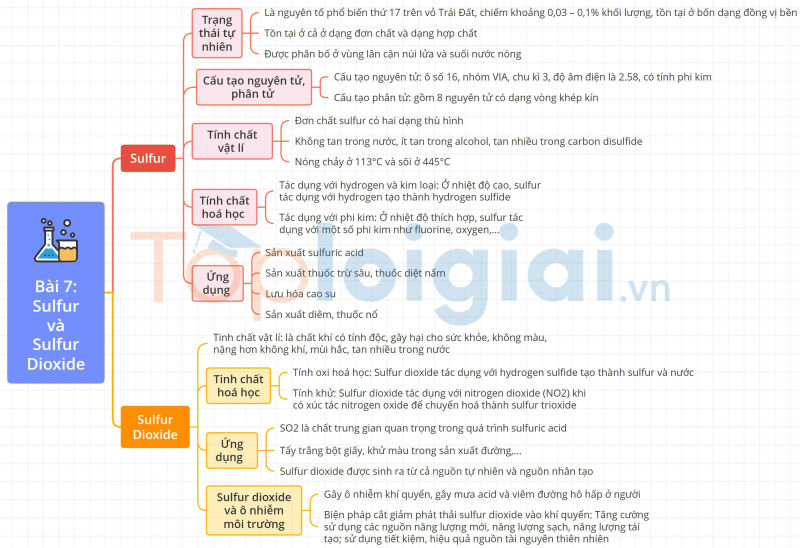
Sơ đồ tư duy Sulfur và sulfur dioxide
B. Trắc nghiệm Sulfur và sulfur dioxide
Đang cập nhật ...
Xem thêm Lý thuyết các bài Hoá học 11 Kết nối tri thức hay, chi tiết khác:
Lý thuyết Bài 6: Một số hợp chất của nitrogen với oxygen
Lý thuyết Bài 8: Sulfuric acid và muối sulfate
Lý thuyết Bài 10: Hợp chất hữu cơ và hoá học hữu cơ
Lý thuyết Bài 11: Phương pháp tách biệt và tinh chế hợp chất hữu cơ
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.