Toptailieu.vn xin giới thiệu Lý thuyết Sulfuric acid và muối sulfate (Cánh diều) hay, chi tiết | Lý thuyết Hóa học 11. Bài viết gồm phần lý thuyết trọng tâm nhất được trình bày một cách dễ hiểu, dễ nhớ bên cạnh đó là bộ câu hỏi trắc nghiệm có hướng dẫn giải chi tiết để học sinh có thể vận dụng ngay lý thuyết, nắm bài một cách hiệu quả nhất. Mời các bạn đón xem:
Lý thuyết Sulfuric acid và muối sulfate (Cánh diều) hay, chi tiết | Lý thuyết Hóa học 11
Bài giải Bài 7: Sulfuric acid và muối sulfate
A. Lý thuyết Sulfuric acid và muối sulfate
I. Sulfuric acid
1. Cấu tạo phân tử và tính chất vật lí
- Cấu tạo phân tử:
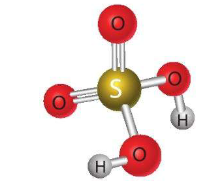
- Tính chất vật lí:
+ Là chất lỏng sánh như dầu, không màu, không bay hơi.
+ Dung dịch sulfuric acid đặc có khả năng hút ẩm.
2. Tính chất hóa học
a, Tính chất hóa học của dung dịch sulfuric acid loãng
+ Đổi màu quý tím thành đỏ
+ Tác dụng với kim loại hoạt động.
+ Tác dụng với basic oxide và base.
+ Tác dụng với nhiều muối.
b, Tính chất hóa học của dung dịch sulfuric acid đặc
- Tính oxi hóa mạnh
+ Oxi hóa hầu hết các kim loại (trừ vàng, platinium), nhiều phi kim như carbon, sulfur, phosphorus… và nhiều hợp chất
VD: H2SO4 + Cu → CuSO4 + SO2 + 2H2O
2H2SO4 + S → 3SO2 + 2H2O
- Tính háo nước
+ Dung dịch sulfuric acid đặc hấp thụ mạnh nước.
3. Bảo quản và xử lí bỏng sulfuric acid
- Bảo quản: Chai, lọ đựng sulfuric acid phải để ở nơi ít có nguy cơ bị va chạm, xa nguồn nhiệt và các hóa chất khác.
- Xử lí bỏng sulfuric acid: Sơ cứu người bị bỏng bằng cách rửa vết bỏng dưới vòi nước sạch ít nhất 20 phút trước khi đưa đến cơ sở y tế.
+ Tuyệt đối không chườm đá lạnh, khong xoa vết bỏng bằng các loại kem, gel, dầu …
4. Ứng dụng và sản xuất sulfuric acid
a, Ứng dụng
- Sản xuất phân bón.
- Chất tẩy rửa, phẩm màu, thuốc trừ sâu…
b, Sản xuất sulfuric acid bằng phương pháp tiếp xúc
S(s) + O2(g) → SO2(g)
4FeS2(s) + 11O2(g) → 2Fe2O3(s) + 8SO2(g)
2SO2 + O2(g) → 2SO3
H2SO4(aq) + nSO3(g) → H2SO4.nSO3(l)
H2SO4.nSO3 (l) + nH2O → (n+1) H2SO4
II. Muối sulfate
1. Một số muối sulfate
- Muối sulfate đa số đều tan trong nước, CaSO4 rất ít tan, BaSO4 không tan trong nước.
- Ứng dụng của một số muối:
+ (NH4)2SO4: dùng làm phân bón cung cấp đạm.
+ MgSO4: Chủ yếu dùng làm phân bón.
+ CaSO4.2H2O (thạch cao tự nhiên); CaSO4.0,5H2O (thạch cao nung): hút nước, sử dụng trong vật liệu xây dựng, đúc tượng …
+ BaSO4: Sơn, mực in, nhựa, lớp phủ, men, …
2. Nhận biết ion SO42- trong dung dịch
Ba2+ + SO42- → BaSO4
Xuất hiện kết tủa trắng (BaSO4)
Sơ đồ tư duy Sulfuric acid và muối sulfate
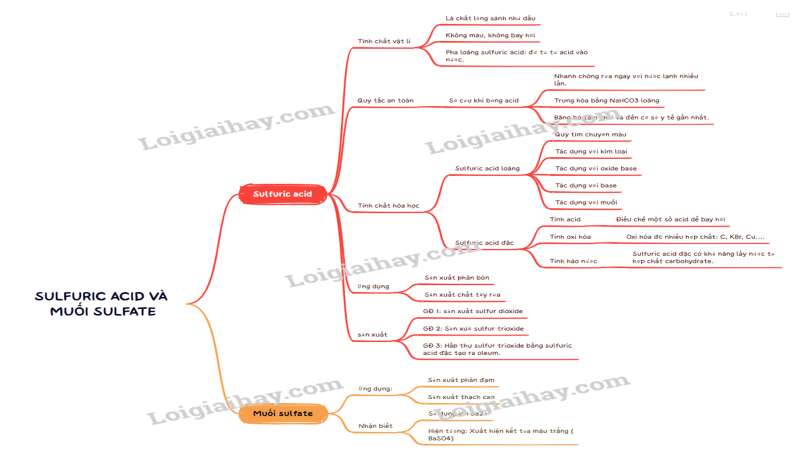
B. Bài tập Sulfuric acid và muối sulfate
Đang cập nhật ...
Xem thêm Lý thuyết các bài Hoá học 11 Cánh Diều hay, chi tiết khác:
Lý thuyết Bài 6: Sulfur và sulfur dioxide
Lý thuyết Bài 8: Hợp chất hữu cơ và hoá học hữu cơ
Lý thuyết Bài 9: Phương pháp tách biệt và tinh chế hợp chất hữu cơ
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.