Toptailieu.vn xin giới thiệu Lý thuyết Hợp chất carbonyl (Cánh diều) hay, chi tiết | Lý thuyết Hóa học 11. Bài viết gồm phần lý thuyết trọng tâm nhất được trình bày một cách dễ hiểu, dễ nhớ bên cạnh đó là bộ câu hỏi trắc nghiệm có hướng dẫn giải chi tiết để học sinh có thể vận dụng ngay lý thuyết, nắm bài một cách hiệu quả nhất. Mời các bạn đón xem:
Nội dung bài viết
Lý thuyết Hợp chất carbonyl (Cánh diều) hay, chi tiết | Lý thuyết Hóa học 11
A. Lý thuyết Hợp chất carbonyl
I. Khái niệm và danh pháp
1. Khái niệm
- Nhóm ![]() trong phân tử hợp chất hữu cơ được gọi là nhóm carbonyl.
trong phân tử hợp chất hữu cơ được gọi là nhóm carbonyl.
- Aldehyde, ketone thuộc loại hợp chất carbonyl.
- Aldehyde là hợp chất hữu cơ trong phân tử có nhóm –CHO liên kết trực tiếp với nguyên tử carbon hoặc nguyên tử hydrogen.
- Ketone là hợp chất hữu cơ có nhóm carbonyl liên kết với hai gốc hydrocarbon.
2. Danh pháp
a) Tên thay thế
- Tên aldehyde = Tên hydrocarbon (bỏ e) + al
- Tên ketone = Tên hydrocarbon (bỏ e)-vị trí nhóm carbonyl-one
b) Tên thông thường
- Tên thông thường của aldehyde: các aldehyde mà acid tương ứng của chúng có tên thông thường thì có thể được gọi tên thông thường bằng cách thay “…ic acid” bằng “…ic aldehyde” hoặc “…aldehyde”.
- Tên thông thường của ketone: một số ketone có tên thông thường.
II. Tính chất vật lý
-Nhiệt độ sôi cao hơn hydrocarbon nhưng thấp hơn alcohol có phân tử khối tương đương.
-Tính tan: mạch ngắn tan tốt, mạch dài không tan hoặc ít tan.
III. Tính chất hóa học
1. Phản ứng khử hợp chất carbonyl
- Với chất khử là LiAlH4 hoặc NaBH4 thì
+ Aldehyde bị khử tạo thành alcohol bậc 1
+ Ketone bị khử tạo thành alcohol bậc 2
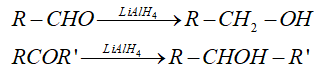
2. Phản ứng oxi hóa aldehyde
a) Phản ứng với nước bromie
- Khi tác dụng với nước bromine, aldehyde bị oxi hóa tạo thành acid.
![]()
b) Phản ứng với thuốc thử Tollens
- Thuốc thử Tollens là dung dịch AgNO3 trong NH3 dư:
AgNO3 + 3NH3 + H2O → [Ag(NH3)2]OH + NH4NO3
- Phản ứng tổng quát giữa thuốc thử Tollens với aldehyde sau:
R-CH=O + 2[Ag(NH3)2]OH → R-COONH4 + 2Ag + 3NH3 + H2O
c) Phản ứng với Cu(OH)2
- Trong môi trường kiềm, Cu(OH)2 oxi hóa hầu hết các aldehyde thành muối carboxylate và sinh ra kết tủa Cu2O có màu đỏ gạch.
- Ketone không có phản ứng với thuốc thử Tollens hoặc với Cu(OH)2 (trong môi trường kiềm) => có thể dung thuốc thử Tollens hoặc Cu(OH)2 để phan biệt aldehyde hoặc ketone.
3. Phản ứng với hydrogen cyanide: tạo sản phẩm cyanohydrin (hydroxynitrile)
CH3-CH=O + H-C≡C → CH3-CH(OH)-CN
CH3-CO-CH3 + H-C≡C → (CH3)2C(OH)-CN
4. Phản ứng tạo iodoform
- Các aldehyde, ketone có nhóm methyl cạnh nhóm carbonyl (CH3CO-) tham gia được phản ứng iodoform.
CH3-CH=O + I2 + 4NaOH → CHI3 +H-COONa + 3NaI + 3H2O
CH3-CO-CH3 + 3I2 + 4NaOH → CHI3 + CH3COONa + 3NaI + 3H2O
IV. Ứng dụng và điều chế
1. Ứng dụng
- Formaldehyde dùng làm dung môi, sản xuất nhựa,…
- Acetaldehyde dùng làm nguyên liệu.
- Acetone làm dung môi, nguyên liệu.
2. Điều chế
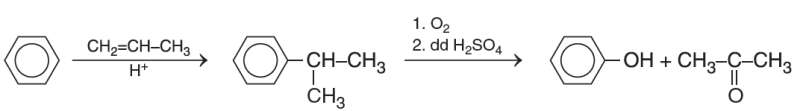
a) Điều chế acetaldehyde
![]()
b) Điều chế acetone:
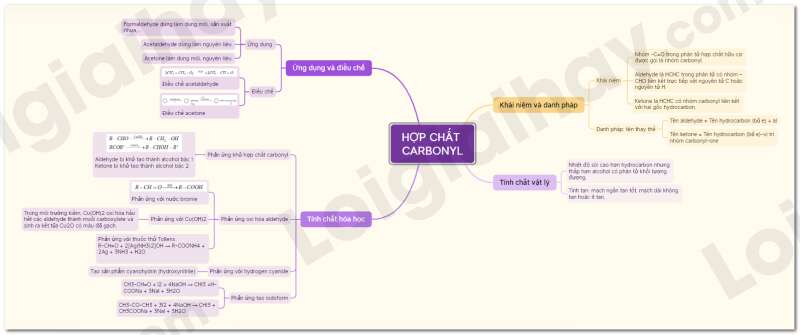
Sơ đồ tư duy Hợp chất carbonyl
B. Bài tập Hợp chất carbonyl
Đang cập nhật ...
Xem thêm Lý thuyết các bài Hoá học 11 Cánh Diều hay, chi tiết khác:
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.