Toptailieu.vn xin giới thiệu Lý thuyết KHTH 8 (Chân trời sáng tạo) Bài 13: Muối . Bài viết gồm phần lý thuyết trọng tâm nhất được trình bày một cách dễ hiểu, dễ nhớ bên cạnh đó là bộ câu hỏi trắc nghiệm có hướng dẫn giải chi tiết để học sinh có thể vận dụng ngay lý thuyết, nắm bài một cách hiệu quả nhất. Mời các bạn đón xem:
Lý thuyết KHTH 8 (Chân trời sáng tạo) Bài 13: Muối
A. Kiến thức trọng tâm KHTN 8 Bài 13: Muối
I. Khái niệm muối
Muối là hợp chất được tạo ra khi thay thế ion H+ trong acid bằng ion kim loại hoặc ion ammonium (NH4+).
Ví dụ: Na2SO4 là muối có thành phần sau:
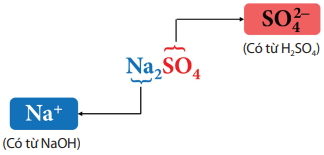
Cách gọi tên muối:
- Cách gọi tên muối của kim loại:
Tên kim loại + hoá trị (kim loại nhiều hoá trị) + tên gốc acid
- Cách gọi tên muối của ammonium (NH4+):
Ammonium + tên gốc acid
Ví dụ một số muối và tên gọi tương ứng:
|
Tên muối |
Công thức hoá học |
|
Potassium carbonate |
K2CO3 |
|
Iron(III) sulfate |
Fe2(SO4)3 |
|
Copper(II) chloride |
CuCl2 |
|
Ammonium nitrate |
NH4NO3 |
|
Sodium acetate |
CH3COONa |
|
Calcium phosphate |
Ca3(PO4)2 |
II. Tính tan của muối
Tuỳ thuộc vào khả năng tan trong nước của muối, ta có: muối tan, muối không tan hoặc ít tan.
- Một số muối tan được trong nước:
+ Tất cả các muối của kim loại nhóm IA (Li, Na, K, …)
+ Tất cả các muối ammonium.
+ Tất cả các muối nitrate.
+ Các muối sulfate ngoại trừ BaSO4, PbSO4.
+ Các muối chloride ngoại trừ AgCl, PbCl2.
- Một số muối không tan trong nước:
+ Các muối carbonate ngoại trừ Na2CO3, K2CO3, (NH4)2CO3 …
+ BaSO4, PbSO4 …
+ AgCl, PbCl2 …
III. Điều chế muối
Các phương pháp điều chế muối từ:
- Oxide acid:
Oxide acid + Base → Muối + H2O
Ví dụ: SO2 + Ba(OH)2 → BaSO3 + H2O.
- Oxide base:
Oxide base + Acid → Muối + H2O
Ví dụ: FeO + 2HCl → FeCl2 + H2O
- Dung dịch acid và base:
Acid + Base → Muối + H2O
Ví dụ: HCl + NaOH → NaCl + H2O
- Kim loại và acid:
M + (HCl, H2SO4 loãng, …) → Muối + H2↑
M là một số kim loại như Mg, Al, Zn, Fe, …
Ví dụ: Fe + 2HCl → FeCl2 + H2↑
Ngoài ra, đa số kim loại tác dụng với phi kim thu được muối. Ví dụ đốt dây sắt trong bình khí chlorine thu được muối FeCl3.
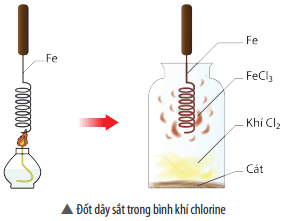
IV. Tính chất hoá học của muối
Một số tính chất hoá học của muối:
- Dung dịch muối phản ứng với kim loại (KL):
Muối KL(A) + KL(B) → Muối KL(B) + KL(A)
Ví dụ: Fe + CuSO4 → FeSO4 + Cu.
- Dung dịch muối phản ứng với dung dịch base:
Muối + Base → Muối mới + Base mới
Ví dụ: 2NaOH + CuCl2 → Cu(OH)2↓ + 2NaCl.
- Dung dịch muối phản ứng với dung dịch acid:
Muối + Acid → Muối mới + Acid mới
Ví dụ: Na2CO3 + 2HCl → 2NaCl + CO2↑ + H2O.
- Dung dịch muối phản ứng với dung dịch muối:
Muối (A) + Muối (B) → Muối (C) + Muối (D)
Ví dụ: K2CO3 + CaCl2 → CaCO3↓ + 2KCl.
V. Mối quan hệ giữa acid, base, oxide và muối
Các hợp chất acid, base, oxide, muối có quan hệ với nhau theo sơ đồ sau:
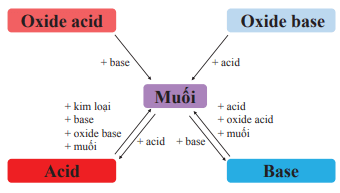
B. Bài tập KHTN 8 Bài 13: Muối
Đang cập nhật
Xem thêm các bài lý thuyết Khoa học tự nhiên 8 Chân trời sáng tạo hay, chi tiết khác:
Bài 1: Sử dụng hoá chất, dụng cụ và các thiết bị điện an toàn
Bài 2: Biến đổi vật lí và biến đổi hoá học
Bài 3: Phản ứng hoá học và năng lượng trong các phản ứng hoá học
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.