Toptailieu.vn xin giới thiệu sơ lược Lý thuyết Benzen và đồng đẳng benzen. Một số hidrocacbon thơm khác (Lý thuyết + 35 bài tập có lời giải)Hóa học11 chọn lọc, hay nhất giúp học sinh lớp 11ôn luyện để nắm chắc kiến thức cơ bản và đạt kết quả cao trong các bài thi môn Hóa học.
Mời các bạn đón xem:
Benzen và đồng đẳng benzen. Một số hidrocacbon thơm khác (Lý thuyết + 35 bài tập có lời giải)
Lí thuyết Benzen và đồng đẳng benzen. Một số hidrocacbon thơm khác
A - Benzen và đồng đẳng
I - Đồng đẳng, đồng phân, danh pháp, cấu tạo
1. Dãy đồng đẳng của benzen
- Dãy đồng đẳng của benzen có công thức chung là CnH2n – 6 (n ≥ 6).
2. Đồng phân, danh pháp
- Cách đọc tên theo danh pháp hệ thống:
Tên = số chỉ vị trí nhánh + tên nhánh + benzen
Lưu ý:
+ Đánh số trên vòng sao cho tổng vị trí nhánh trên vòng là nhỏ nhất.
+ Nếu 2 nhóm thế trên vòng benzen ở vị trí: 1,2 – ortho; 1,3 – meta; 1,4 – para.
Thí dụ:
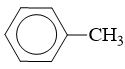 : có tên thông thường là toluen, tên thay thế là metylbenzen.
: có tên thông thường là toluen, tên thay thế là metylbenzen.
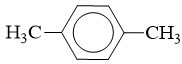 : có tên thông thường là p-xilen, tên thay thế là 1,4-đimetylbenzen (p-đimetylbenzen).
: có tên thông thường là p-xilen, tên thay thế là 1,4-đimetylbenzen (p-đimetylbenzen).
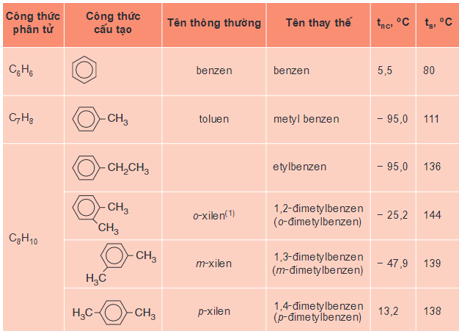
Bảng 1: Tên và hằng số vật lí của một số hiđrocacbon thơm đầu dãy đồng đẳng
- Từ C8H10 trở đi có các đổng phân về vị trí tương đối của các nhóm ankyl xung quanh vòng benzen và về cấu tạo mạch cacbon của mạch nhánh.
3. Cấu tạo
- Công thức cấu tạo của benzen (C6H6) là:
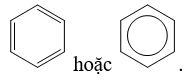
II. TÍNH CHẤT VẬT LÍ
- Các hiđrocacbon thơm đều là chất lỏng hoặc rắn ở điều kiện thường, chúng có nhiệt độ sôi tăng theo chiều tăng của phân tử khối.
- Các hiđrocacbon thơm ở thể lỏng có mùi đặc trưng, không tan trong nước và nhẹ hơn nước, có khả năng hoà tan nhiều chất hữu cơ.
III. TÍNH CHẤT HOÁ HỌC
Các đồng đẳng của benzen có tính chất của vòng benzen và có tính chất của mạch nhánh ankyl.
1. Phản ứng thế
a) Thế nguyên tử H của vòng benzen
* Phản ứng với halogen

- Nếu cho các ankylbenzen phản ứng với brom trong điều kiện có bột sắt sẽ thu được hỗn hợp sản phẩm thế brom chủ yếu vào vị trí para và ortho so với nhóm ankyl:
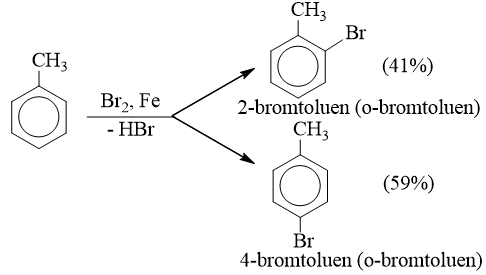
* Phản ứng với axit nitric
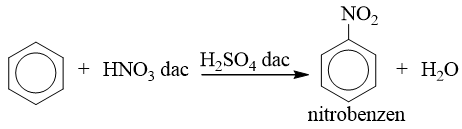
* Quy tắc thế: Các ankylbenzen dễ tham gia phản ứng thế nguyên tử H của vòng benzen hơn benzen và sự thế ưu tiên ở vị trí ortho và para so với nhóm ankyl.
b) Thế nguyên tử H của mạch nhánh
- Nếu đun toluen hoặc các ankylbenzen với brom, sẽ xảy ra phản ứng thế nguyên tử H của mạch nhánh tương tự ankan.
Thí dụ:
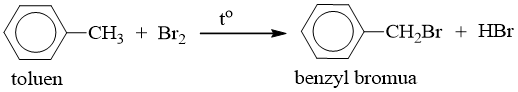
2. Phản ứng cộng
a) Cộng hiđro
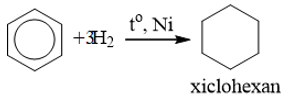
b) Cộng clo
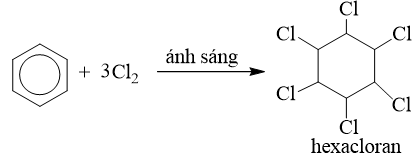
3. Phản ứng oxi hoá
a) Phản ứng oxi hoá không hoàn toàn
- Benzen và các ankylbenzen không làm mất màu dung dịch thuốc tím ở nhiệt độ thường.
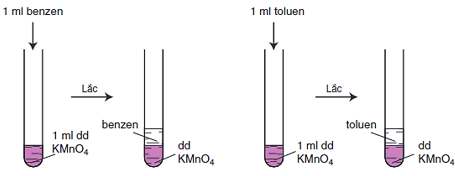
Hình 1: Benzen và toluen không làm mất màu dung dịch KMnO4 ở nhiệt độ thường
- Khi đun nóng, benzen không làm mất màu dung dịch thuốc tím nhưng ankylbenzen làm mất màu dung dịch thuốc tím
Thí dụ: Toluen làm mất màu dung dịch kali pemanganat.
Phương trình hóa học:
C6H5 – CH3 + 2KMnO4 C6H5 – COOK + 2MnO2↓ + KOH + H2O
b) Phản ứng oxi hoá hoàn toàn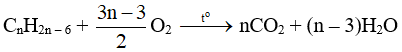
B - Một vài hiđrocacbon thơm khác
I. Stiren
1. Cấu tạo và tính chất vật lí
- Công thức phân tử: C8H8
- Công thức cấu tạo:
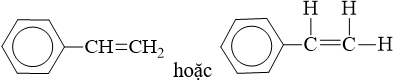
- Stiren (còn gọi là vinylbenzen) là chất lỏng không màu, sôi ở 146oC, tan nhiều trong dung môi hữu cơ.
2. Tính chất hoá học
a) Phản ứng với dung dịch brom
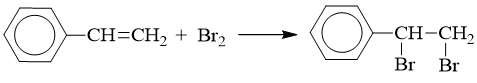
b) Phản ứng với hiđro
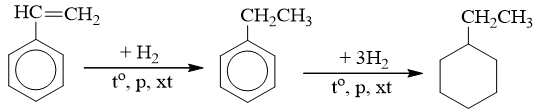
c) Phản ứng trùng hợp
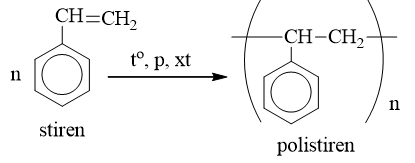
II. Naphtalen
1. Cấu tạo và tính chất vật lí
- Công thức phân tử: C10H8
- Phân tử naphtalen có cấu tạo phẳng:
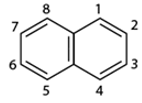
- Naphtalen (băng phiến) là chất rắn, nóng chảy ở 80oC, tan trong benzen, ete,... và có tính thăng hoa.
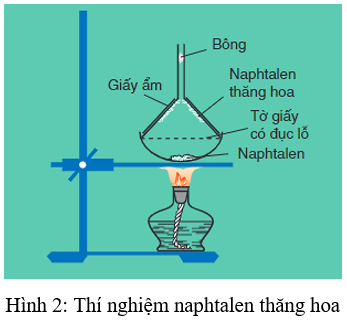
2. Tính chất hóa học
- Naphtalen không làm mất màu dung dịch KMnO4 ở điều kiện thường.
- Naphtalen có tính chất hóa học tương tự benzen.
a) Phản ứng thế
- Naphtalen tham gia phản ứng thế tương tự benzen, nhưng phản ứng xảy ra dễ dàng hơn và thường ưu tiên thế vào vị trí số 1.
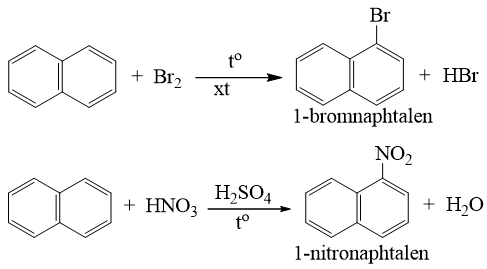
b) Phản ứng cộng
- Khi có chất xúc tác, naphtalen cộng hiđro tạo ra đecalin:
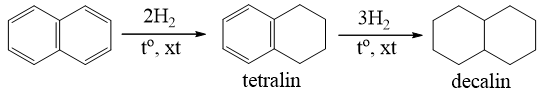
C - Ứng dụng của một số hiđrocacbon thơm
- Benzen và toluen là nguyên liệu rất quan trọng cho công nghiệp hoá học.
- Nguồn cung cấp benzen, toluen chủ yếu là từ nhựa than đá và từ sản phẩm đề hiđro đóng vòng hexan, heptan tương ứng.

Bài tập Benzen và đồng đẳng. Một số hidrocacbon thơm khác
Câu 1: Trong phân tử X có vòng benzen. X không tác dụng với brom khi có mặt bột Fe, còn khi tác dụng với brom đun nóng tỉ lệ 1:1 tạo thành dẫn xuất monobrom duy nhất nên tên của X là
A. Benzen
B. Hexametyl benzen
C. Toluen
D. o - Xilen
Đáp án: B
Câu 2: Để phân biệt benzen, toluen, stiren ta chỉ dùng 1 thuốc thử duy nhất là:
A. Brom (dd).
B. Br2 (Fe).
C. KMnO4 (dd).
D. Br2 (dd) hoặc KMnO4(dd).
Đáp án: C
Câu 3: A có công thức phân tử là C8H8, tác dụng với dung dịch KMnO4 ở nhiệt độ thường tạo ra ancol 2 chức. 1 mol A cộng tối đa với bao nhiêu mol H2 (Ni, to) và bao nhiêu mol Br2 trong dung dịch?
A. 4 mol H2; 1 mol brom.
B. 3 mol H2; 1 mol brom.
C. 3 mol H2; 3 mol brom.
D. 4 mol H2; 4 mol brom.
Đáp án: A
Câu 4: Một hỗn hợp X gồm 2 aren A, R đều có M < 120, tỉ khối của X đối với C2H6 là 3,067. CTPT và số đồng phân của A và R là
A. C6H6 (1 đồng phân); C7H8 (1 đồng phân).
B. C7H8 (1 đồng phân); C8H10 (4 đồng phân).
C. C6H6 (1 đồng phân); C8H10 (2 đồng phân).
D. C6H6 (1 đồng phân); C8H10 (4 đồng phân).
Đáp án: D
Câu 5: Cho 100 ml benzen (D = 0,879 g/ml) tác dụng với một lượng vừa đủ brom lỏng (có mặt bột sắt, đun nóng) thu được 80 ml brombenzen (D = 1,495 g/ml). Hiệu suất brom hóa đạt là
A. 67,6%.
B. 73,49%.
C. 85,3%.
D. 65,35%
Đáp án: A
Câu 6: Đề hiđro hoá etylbenzen ta được stiren; trùng hợp stiren ta được polistiren với hiệu suất chung 80%. Khối lượng etylbenzen cần dùng để sản xuất 10,4 tấn polisitren là:
A. 13,52 tấn.
B. 10,6 tấn.
C. 13,25 tấn.
D. 8,48 tấn.
Đáp án: C
Câu 7: Đốt cháy hoàn toàn x mol hỗn hợp A gồm benzen, toluen, etyl benzen thu được 0,15 mol CO2 và 0,12 mol H2O. Tìm x ?
A. 0,01
B. 0,05
C. 0,06
D. 0,02
Đáp án: A
Câu 8: Lượng clobenzen thu được khi cho 15,6 gam C6H6 tác dụng hết với Cl2 (có mặt bột Fe) với hiệu suất phản ứng đạt 80% là :
A. 14 gam.
B. 16 gam.
C. 18 gam.
D. 20 gam.
Đáp án: C
Câu 9: Hỗn hợp gồm 1 mol C6H6 và 1,5 mol Cl2. Trong điều kiện có mặt bột Fe, to, hiệu suất 100%. Sau phản ứng thu được chất gì ? bao nhiêu mol ?
A. 1 mol C6H5Cl; 1 mol HCl; 1 mol C6H4Cl2.
B. 1,5 mol C6H5Cl; 1,5 mol HCl; 0,5 mol C6H4Cl2.
C. 1 mol C6H5Cl; 1,5 mol HCl; 0,5 mol C6H4Cl2.
D. 0,5 mol C6H5Cl; 1,5 mol HCl; 0,5 mol C6H4Cl2.
Đáp án: D
Câu 10: Một hợp chất hữu cơ X có vòng benzen có CTĐGN là C3H2Br và M = 236. Gọi tên hợp chất này biết rằng hợp chất này là sản phẩm chính trong phản ứng giữa C6H6 và Br2 (xúc tác Fe).
A. o- hoặc p-đibrombenzen.
B. o- hoặc p-đibromuabenzen.
C. m-đibromuabenzen.
D. m-đibromben
Đáp án: A
Câu 11: Hiđrocacbon X là đồng đẳng của benzen có phần trăm khối lượng cacbon bằng 90,56%. Biết khi X tác dụng với brom có hoặc không có mặt bột sắt trong mỗi trường hợp chỉ thu được một dẫn xuất monobrom duy nhất. Tên của X là
A. Toluen.
B. 1,3,5-trimetyl benzen.
C. 1,4-đimetylbenzen.
D. 1,2,5-trimetyl benzen.
Đáp án: C
Câu 12: Đốt cháy hoàn toàn a gam hiđrocacbon X thu được a gam H2O. Trong phân tử X có vòng benzen. X không tác dụng với brom khi có mặt bột Fe, còn khi tác dụng với brom đun nóng tạo thành dẫn xuất chứa 1 nguyên tử brom duy nhất. Tỉ khối hơi của X so với không khí có giá trị trong khoảng từ 5 đến 6. X là
A. Hexan.
B. Hexametyl benzen.
C. Toluen.
D. Hex-2-en.
Đáp án: B
Câu 13: TNT (2,4,6- trinitrotoluen) được điều chế bằng phản ứng của toluen với hỗn hợp gồm HNO3 đặc và H2SO4 đặc, trong điều kiện đun nóng. Biết hiệu suất của toàn bộ quá trình tổng hợp là 80%. Lượng TNT (2,4,6-trinitrotoluen) tạo thành từ 230 gam toluen là
A. 550,0 gam.
B. 687,5 gam.
C. 454,0 gam.
D. 567,5 gam.
Đáp án: C
Câu 14: Nitro hóa benzen được 14,1 gam hỗn hợp hai chất nitro có khối lượng phân tử hơn kém nhau 45 đvC. Đốt cháy hoàn toàn hỗn hợp hai chất nitro này được 0,07 mol N2. Hai chất nitro đó là:
A. C6H5NO2 và C6H4(NO2)2.
B. C6H4(NO2)2 và C6H3(NO2)3.
C. C6H3(NO2)3 và C6H2(NO2)4.
D. C6H2(NO2)4 và C6H(NO2)5.
Đáp án: A
Câu 15: Đốt cháy hoàn toàn hiđrocacbon A, sau phản ứng thu được 15,68 lít CO2 (đktc) và 7,2 gam H2O. Tìm công thức cấu tạo của A.
A. C6H5 – CH3
B. C6H6
C. C6H5 – C2H5
D. C6H5 – C2H3
Đáp án: A
Câu 16: Đốt cháy hoàn toàn a g hỗn hợp X gồm 2 hiđrocacbon thơm A và B là 2 đồng đẳng kế tiếp nhau thuộc dãy đồng đẳng của benzen. Sau phản ứng thu được 7,84 lít CO2 (đktc)và 3,33 g H2O. Xác định CTCT của A và B.
A. C6H6 và C8H8
B. C6H6 và C6H5 – C2H3
C. C6H6 và C6H5 – C2H5
D. C6H6 và C6H5 – CH3
Đáp án: D
Câu 17: Tiến hành trùng hợp 10,4 gam stiren được hỗn hợp X gồm polistiren và stiren (dư). Cho X tác dụng với 200 ml dung dịch Br2 0,15M, sau đó cho dung KI dư vào thấy xuất hiện 1,27 gam iot. Hiệu suất trùng hợp stiren là
A. 60%.
B. 75%.
C. 80%.
D. 83,33%.
Đáp án: B
Câu 18: Đốt cháy hoàn toàn hiđrocacbon X cho CO2 và H2O theo tỉ lệ mol 1,75 : 1 về thể tích. Cho bay hơi hoàn toàn 5,06 gam X thu được một thể tích hơi đúng bằng thể tích của 1,76 gam oxi trong cùng điều kiện. Nhận xét nào sau đây là đúng đối với X ?
A. X không làm mất màu dung dịch Br2 nhưng làm mất màu dung dịch KMnO4 đun nóng.
B. X tác dụng với dung dịch Br2 tạo kết tủa trắng.
C. X có thể trùng hợp thành PS.
D. X tan tốt trong nước.
Đáp án: A
Câu 19: Đốt cháy hết 9,18 gam 2 đồng đẳng của benzen A, B thu được 8,1 gam H2O và V lít CO2 (đktc). Giá trị của V là:
A. 15,654.
B. 15,465.
C. 15,546.
D. 15,456.
Đáp án: D
Câu 20: Cho 21 g hỗn hợp axetilen và toluen phản ứng với dung dịch KMnO4/H2SO4 loãng. Sau phản ứng thu được 33,4 g hỗn hợp hai axit. Tính thành phần phần trăm khối lượng của mỗi chất trong hỗn hợp ban đầu.
A. %C2H2 = 45%, %C6H5CH3 = 55%
B. %C2H2 = 60%, %C6H5CH3 = 40%
C. %C2H2 = 35%, %C6H5CH3 = 65%
D. %C2H2 = 12,38%, %C6H5CH3 = 87,62%
Đáp án: D
Câu 21: Khi cho toluen phản ứng với Br2 (xúc tác Fe, toC) theo tỉ lệ 1:1 về số mol, sản phẩm chính thu được có tên là
A. benzyl clorua
B. 2,4-đibromtoluen
C. p-bromtoluen
D. m-bromtoluen
Đáp án: C
Câu 22: Cho các hidrocacbon: eten; axetilen; benzen; toluen; isopentan; stiren. Số chất làm mất màu dung dịch KMnO4 là:
A. 4
B. 5
C. 6
D. 3
Đáp án: A
Câu 23: Cứ 49,125 gam cao su buna-S phản ứng vừa hết với 30 gam brom trong CCl4. Tỉ lệ số mắt xích stiren và butađien trong loại cao su trên tương ứng là
A. 1 : 2.
B. 2 : 3.
C. 2 : 1.
D. 1 : 3.
Đáp án: C
Câu 24: Công thức tổng quát hidrocacbon thơm là
A. CnH2n-6
B. CnH2n
C, CnH2n-4
D. C2H2n-2
Đáp án: A
Câu 25: Ankylbenzen là hiđrocacbon có chứa :
A. vòng benzen.
B. gốc ankyl và vòng benzen.
C. gốc ankyl và 1 benzen.
D. gốc ankyl và 1 vòng benzen.
Đáp án: D
Câu 26: Trong vòng benzen có chứa mấy liên kết
A.1
B. 2
C. 3
D. 4
Đáp án: C
Câu 27: Nhận xét nào sau đây đúng khi nói về tính chất vật lí của hidrocacbon thơm
(1) Các hidrocacbon thơm thường là chất lỏng
(2) Các hidrocacbon không tan trong nước, tan nhiều trong dung môi hữu cơ
(3) Các hidrocacbon dễ tan trong nước
(4)Các hidrocacbon có tính độc
(5) Các hidrocacbon đều là chất khí.
A. 1, 2, 4
B.1, 2, 5
C.1, 3, 4
D.1, 2, 4, 5
Đáp án: A
Câu 28: Giả sử số nguyên tử cacbon trong phân tử hidrocacbon thơm là n. Điều kiện của n
A.
B. n > 6
C. n 4
D. n >1
Đáp án: A
Câu 29: Chất A có công thức cấu tạo
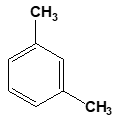
Tên gọi của chất A là
A. 1,3-đimetylbenzen
B. m-xilen
C. toluen
D. cả A,B
Đáp án: D
Câu 30: Tính chất hóa học đặc trưng của benzen và đồng đẳng của nó là
A. Dễ thế, khó cộng
B. Dễ cộng, khó thế
C. Dễ trùng hợp
D. Dễ bị oxi hóa bằng dung dịch thuốc tím
Đáp án: A
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.