Toptailieu biên soạn và sưu tầm lời giải bài tập Hóa học lớp 10 Bài 7: Xu hướng biến đổi một số tính chất của đơn chất, biến đổi thành phần và tính chất của hợp chất trong một chu kì và trong một nhóm sách Cánh Diều hay, chi tiết sẽ giúp học sinh dễ dàng trả lời câu hỏi Hóa học 10 Bài 7 từ đó học tốt môn Hóa học 10.
Nội dung bài viết
Hoá học 10 Cánh Diều Bài 7: Xu hướng biến đổi một số tính chất của đơn chất, biến đổi thành phần và tính chất của hợp chất trong một chu kì và trong một nhóm
a) Điện tích hạt nhân càng lớn thì lực hút electron càng mạnh hay càng yếu?
b) Khoảng cách giữa electron và hạt nhân càng lớn thì electron bị hạt nhân hút càng mạnh hay càng yếu?
Lời giải:
a) Dựa vào biểu thức F = aZr2 , điện tích hạt nhân càng lớn (tức Z càng lớn) thì lực hút electron càng mạnh (tức F càng lớn).
b) Dựa vào biểu thức F = aZr2 , khoảng cách giữa electron và hạt nhân càng lớn (tức r càng lớn) thì electron bị hạt nhân hút càng yếu (tức F càng nhỏ).
I. Xu hướng biến đổi bán kính nguyên tử
Lời giải:
- Các nguyên tố chu kì 2 có 2 lớp electron.
- Mô hình nguyên tử của Li (Z = 3) và F (Z = 9) theo Rutherford – Bohr như sau:
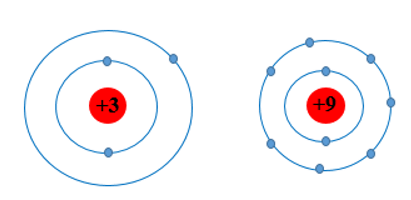
Li và F đều cùng có 2 lớp electron, tuy nhiên điện tích hạt nhân của F lớn hơn Li nên hạt nhân của F sẽ hút electron lớp ngoài cùng mạnh hơn làm cho bán kính nguyên tử F nhỏ hơn Li.
Lời giải:
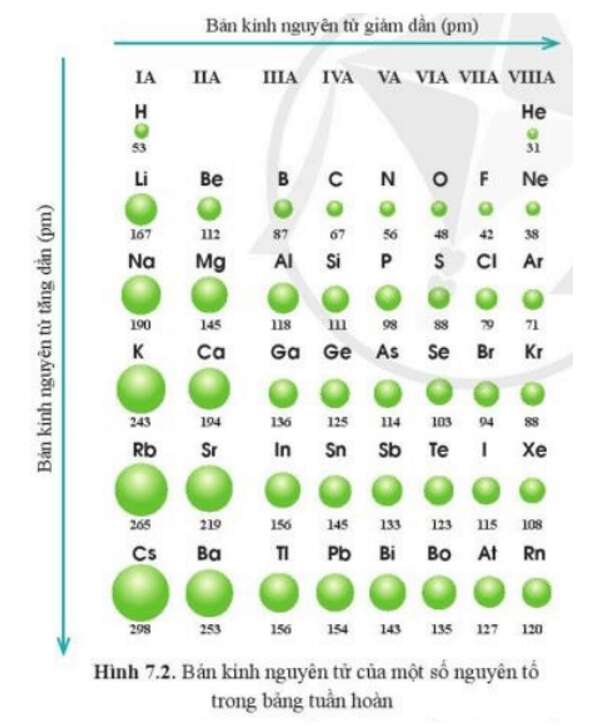
Trong các chu kì 3, 4, 5 theo chiều tăng dần điện tích hạt nhân bán kính nguyên tử của các nguyên tố giảm dần.
Lời giải:
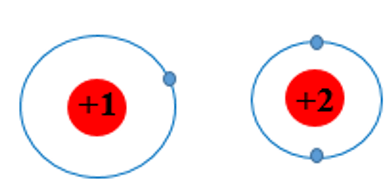
Đều có 1 lớp electron nhưng nguyên tử He có điện tích hạt nhân +2 lớn hơn nguyên tử H (điện tích hạt nhân là +1) nên hút electron lớp ngoài cùng mạnh hơn, làm cho bán kính của He nhỏ hơn bán kính của H.
Mặt khác, nguyên tử He chỉ có 1 lớp electron nên bán kính là nhỏ nhất trong bảng tuần hoàn.
II. Xu hướng biến đổi độ âm điện, tính kim loại và tính phi kim

Lời giải:
Quy luật chung về sự biến đổi độ âm điện của các nguyên tử nguyên tố nhóm A trong một chu kì, trong một nhóm:
- Trong một chu kì, theo chiều tăng điện tích hạt nhân, độ âm điện của các nguyên tử nguyên tố có xu hướng tăng dần (ngoại lệ ở chu kì 6).
- Trong một nhóm, theo chiều tăng điện tích hạt nhân, độ âm điện của các nguyên tử nguyên tố có xu hướng giảm dần (ngoại lệ ở nhóm IIA).
Lời giải:
Trong phân tử H2 có hai nguyên tử H liên kết với nhau.
⇒ Độ âm điện của hai nguyên tử bằng nhau.
⇒ Lực hút electron liên kết giữa hai nguyên tử bằng nhau.
⇒ Cặp electron liên kết của phân tử H2 không bị lệch về nguyên tử nào
Lời giải:
- Độ âm điện của H và N lần lượt là 2,2 và 3,0. Vậy nguyên tử N hút electron liên kết mạnh hơn nguyên tử H, gấp 3,0 : 2,2 = 1,36 lần.
- Độ âm điện của H và O lần lượt là 2,2 và 3,4. Vậy nguyên tử N hút electron liên kết mạnh hơn nguyên tử H, gấp 3,4 : 2,2 = 1,54 lần.
Ta thấy 1,54 > 1,36 nên cặp electron liên kết bị lệch nhiều hơn trong phân tử H2O.
Lời giải:
Cấu hình electron của nguyên tố X (Z = 14) là: 1s22s22p63s23p2
Cấu hình electron của nguyên tố Y (Z = 16) là: 1s22s22p63s23p4
Dựa vào cấu hình electron ta thấy X và Y đều thuộc chu kì 3 tuy nhiên điện tích hạt nhân của Y lớn hơn X nên độ âm điện của Y lớn hơn độ âm điện của X.
Chú ý: Trong một chu kì, theo chiều tăng điện tích hạt nhân, độ âm điện của các nguyên tử nguyên tố có xu hướng tăng dần.
Lời giải:
Trong một chu kì, từ trái sang phải, điện tích hạt nhân tăng dần, bán kính nguyên tử giảm dần nên lực hút của hạt nhân tới electron hóa trị tăng, làm tăng khả năng nhận electron, do đó, tính phi kim của nguyên tố tăng dần.
Trong một nhóm A, mặc dù điện tích hạt nhân tăng dần nhưng do bán kính nguyên tử của các nguyên tố tăng nhanh, nên lực hút của hạt nhân tới electron hóa trị giảm dần, làm giảm khả năng nhận thêm electron, do đó tính phi kim giảm.
Lời giải:
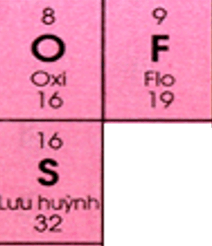
O (Z = 8) và F (Z = 9) thuộc cùng một chu kì. Theo chiều điện tích hạt nhân tăng dần ta được tính phi kim F > O (1).
O và S thuộc cùng một nhóm A. Theo chiều điện tích hạt nhân tăng dần ta được tính phi kim O > S (2)
Từ (1) và (2) ⇒ Tính phi kim F > O > S.
III. Xu hướng biến đổi thành phần và tính acid, tính base của các oxide và các hydroxide theo chu kì
Lời giải:
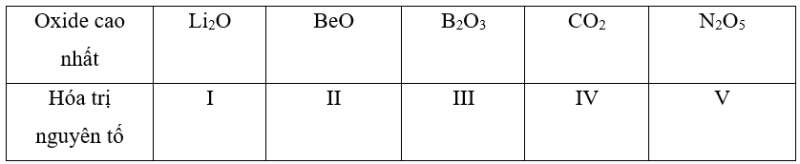
Công thức oxide cao nhất và hóa trị tương ứng của các nguyên tố chu kì 2, từ Li đến N được thể hiện trong bảng sau:
Vận dụng trang 43 Hóa học 10: Giải thích vì sao không dùng chậu nhôm để đựng nước vôi tôi.
Lời giải:
Không dùng chậu nhôm để đựng nước vôi tôi vì nước vôi tôi (Ca(OH)2) sẽ làm thủng chậu nhôm do có phản ứng:
Al2O3 + Ca(OH)2 + 3H2O → Ca[Al(OH)4]2
2Al + Ca(OH)2 + 6H2O → Ca[Al(OH)4]2 + 3H2
Lời giải:
Al(OH)3 thể hiện tính acid trong phản ứng:
Al(OH)3 + NaOH → Na[Al(OH)4]
Al(OH)3 thể hiện tính base trong phản ứng:
Al(OH)3 + 3HCl → AlCl3 + 3H2O
Lời giải:
- Trong một chu kì, theo chiều tăng điện tích hạt nhân tính kim loại của các nguyên tố có xu hướng giảm dần ⇒ Các nguyên tố đầu mỗi chu kì (các nguyên tố nhóm IA (trừ H)) có tính kim loại mạnh nhất.
Xét trong cùng một nhóm (nhóm IA), theo chiều tăng điện tích hạt nhân tính kim loại của các nguyên tố có xu hướng tăng dần ⇒ Fr có tính kim loại mạnh nhất.
- Trong một chu kì, theo chiều tăng điện tích hạt nhân tính phi kim của các nguyên tố có xu hướng tăng dần ⇒ Các nguyên tố cuối mỗi chu kì (các nguyên tố nhóm VIIA) có tính phi kim mạnh nhất.
Xét trong cùng một nhóm (nhóm VIIA), theo chiều tăng điện tích hạt nhân tính phi kim của các nguyên tố có xu hướng giảm dần ⇒ F có tính phi kim mạnh nhất
Lời giải:
Công thức các hydroxide và hóa trị tương ứng của những nguyên tố chu kì 2:
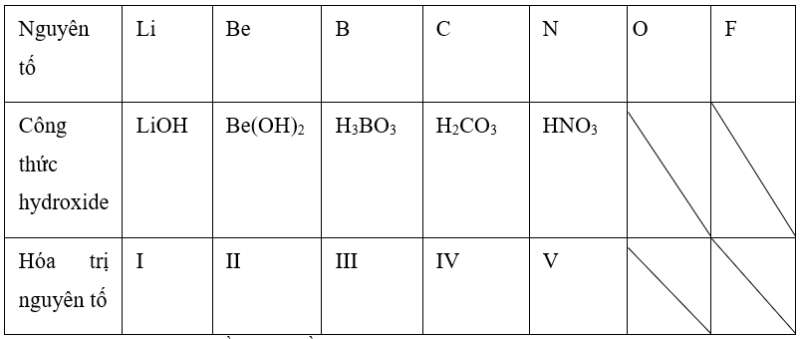
Trong chu kì 2, theo chiều tăng dần điện tích hạt nhân, tính acid của các hydroxide tăng dần, đồng thời tính base giảm dần.
LiOH là một base mạnh.
2LiOH + CO2 → Li2CO3 + H2O
Be(OH)2 có cả tính acid và tính base:
Be(OH)2 + 2NaOH → Na2BeO2 + 2H2O
Be(OH)2 + 2HCl → BeCl2 + 2H2O
H3BO3 là acid rất yếu, H2CO3 là acid yếu, HNO3 là acid mạnh.
Bài 1 trang 45 Hóa học 10: Hoàn thành chỗ trống trong các câu sau:
a) Trong một chu kì, theo chiều ...(1)... điện tích hạt nhân, độ âm điện của các nguyên tố có xu hướng tăng dần, tính base của các hydroxide của các nguyên tố có xu hướng ...(2)... dần.
c) Nhóm ...(3)... là nhóm chứa các nguyên tố đứng đầu mỗi chu kì trong bảng tuần hoàn. Trong nhóm này, nguyên tử nguyên tố ...(4)... có bán kính lớn nhất. Số lượng các nguyên tố là kim loại của nhóm này là ...(5)...
Lời giải:
(1) tăng
(2) giảm
(3) kim loại kiềm (kim loại điển hình)
(4) Francium (Fr)
(5) 6
(1) Dễ nhường electron
(2) Dễ nhận electron
(3) Oxide cao nhất có tính base
(4) Oxide cao nhất có tính acid
Lời giải:
Đặc trưng thuộc về kim loại nhóm A là:
(1) Dễ nhường electron
(3) Oxide cao nhất có tính base
Đặc trưng thuộc về phi kim là:
(2) Dễ nhận electron
(4) Oxide cao nhất có tính acid
a) H3PO4 + Na2SO4 → ?
b) HNO3 + Na2CO3 → ?
Lời giải:
Trong hai phản ứng trên, phản ứng (b) xảy ra còn phản ứng (a) không xảy ra.
Giải thích:
Phản ứng a) không xảy ra do H3PO4 là acid trung bình nên không đẩy được H2SO4 là acid mạnh ra khỏi muối.
Phản ứng b) xảy ra do HNO3 là acid mạnh nên đẩy được H2CO3 là acid rất yếu ra khỏi muối.
Bài 4 trang 45 Hóa học 10: Cấu hình electron lớp ngoài cùng của các nguyên tố chu kì 2 và 3 như sau:
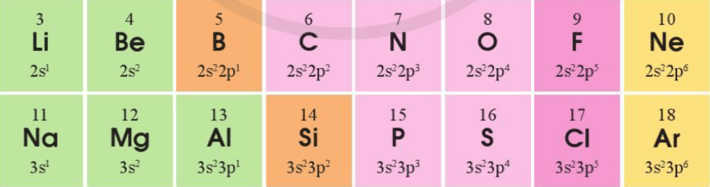
a) Sự lặp lại tuần hoàn về cấu hình electron lớp ngoài cùng của các nguyên tố chu kì 2 và 3 thể hiện như thế nào?
b*) Giải thích vì sao sự biến đổi tuần hoàn về cấu hình electron lớp ngoài cùng là nguyên nhân quyết định đến sự biến đổi tính tuần hoàn về tính chất hóa học của các đơn chất và hợp chất các nguyên tố chu kì 2 và 3. Lấy một số ví dụ để minh họa sự biến đổi đó.
Lời giải:
a) Sự lặp lại tuần hoàn về cấu hình electron lớp ngoài cùng của các nguyên tố chu kì 2 và 3 thể hiện như sau: Đi từ trái qua phải theo chiều tăng dần điện tích hạt nhân nguyên tử, số electron lớp ngoài cùng tăng dần từ 1 đến 8.
b*) Vì với các nguyên tố chu kỳ 2 và 3 electron hóa trị tham gia vào việc hình thành liên kết hóa học cũng là electron ở lớp ngoài cùng. Do đó, sự biến đổi tuần hoàn về cấu hình electron lớp ngoài cùng là nguyên nhân quyết định đến sự biến đổi tính tuần hoàn về tính chất hóa học của các đơn chất và hợp chất các nguyên tố chu kì 2 và 3
Một số ví dụ để minh họa sự biến đổi tính chất hóa học của đơn chất và hợp chất:
+ Trong chu kì 2, theo chiều từ trái sang phải (chiều tăng của điện tích hạt nhân), tính kim loại của các nguyên tố giảm dần, đồng thời tính phi kim tăng dần. Điều này cũng được lặp lại ở các chu kì khác.
+ Trong chu kì 2, theo chiều tăng của điện tích hạt nhân, tính acid của oxide cao nhất có xu hướng tăng dần, tính base của chúng có xu hướng giảm dần. Điều này cũng được lặp lại ở các chu kì khác.
Xem thêm các bài giải Hoá học lớp 10 Cánh Diều hay, chi tiết khác:
Bài 6: Cấu tạo bảng tuần hoàn các nguyên tố hoá học
Bài 8: Định luật tuần hoàn và ý nghĩa của bảng tuần hoàn các nguyên tố hóa học
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.