Với giải Câu hỏi trang 91 SGK Hoá học10 Cánh Diều Bài 16: Tốc độ phản ứng giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Hoá học 10. Mời các bạn đón xem:
Nội dung bài viết
Hoá học 10 Cánh Diều trang 91 Bài 16: Tốc độ phản ứng
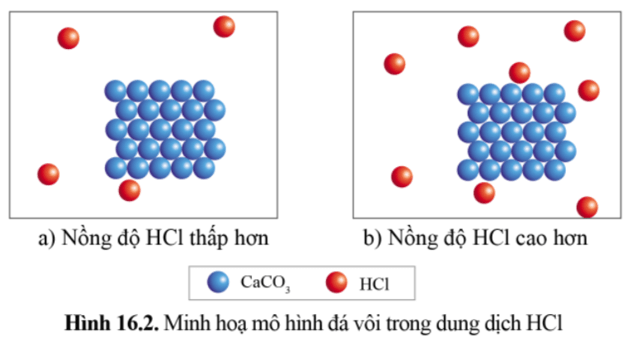
Thực hành trang 91 Hóa học 10: Cho hai mẩu đá vôi từ cùng một mẫu có kích thước xấp xỉ nhau vào hai ống nghiệm chứa cùng một thể tích dung dịch HCl (khoảng 13 ống nghiệm) có nồng độ khác nhau lần lượt là: 0,1M (ống nghiệm (a)) và 0,2M (ống nghiệm (b)). Quan sát hiện tượng phản ứng và nhận xét về mối liên hệ giữa tốc độ phản ứng và nồng độ HCl.
Lời giải:
Hiện tượng:
Mẩu đá vôi tan nhanh hơn trong dung dịch HCl 0,2M (ống nghiệm (b)) đồng thời khí thoát ra ở ống nghiệm (b) cũng nhanh hơn khí thoát ra ở ống nghiệm (a).
Phương trình hóa học của phản ứng:
CaCO3 + 2HCl → CaCl2 + H2O + CO2↑
Nhận xét:
Nồng độ HCl càng lớn thì tốc độ của phản ứng càng lớn.
Vận dụng 2 trang 91 Hóa học 10: Thực phẩm bị ôi thiu do các phản ứng oxi hóa của oxygen cũng như sự hoạt động của vi khuẩn. Giải thích vì sao để hạn chế sự ôi thiu, người ta lại bơm N2 hoặc CO2 vào túi đựng thực phẩm trước khi đóng gói. Biết rằng nồng độ oxygen trong túi thực phẩm sau khi bơm N2 hoặc CO2 chỉ còn khoảng 2 – 5%.
Lời giải:
Bơm N2 hoặc CO2 vào túi để đẩy bớt oxygen ra ngoài
⇒ Giảm nồng độ oxygen trong túi
⇒ Giảm tốc độ phản ứng oxi hóa của oxygen
⇒ Hạn chế sự ôi thiu thực phẩm
Xem thêm lời giải bài tập Hóa học lớp 10 Cánh diều hay, chi tiết khác:
Vận dụng 4 trang 94 Hóa học 10: Giải thích vì sao thanh củi chẻ nhỏ hơn thì sẽ cháy nhanh hơn...
Xem thêm các bài giải Hoá học lớp 10 Cánh Diều hay, chi tiết khác:
Bài 15: Ý nghĩa và cách tính biến thiên enthalpy phản ứng hoá học
Bài 17: Nguyên tố đơn chất halogen
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.