Toptailieu.vn xin giới thiệu Lý thuyết Ammonia. Muối ammonium (Kết nối tri thức) hay, chi tiết | Lý thuyết Hóa học 11. Bài viết gồm phần lý thuyết trọng tâm nhất được trình bày một cách dễ hiểu, dễ nhớ bên cạnh đó là bộ câu hỏi trắc nghiệm có hướng dẫn giải chi tiết để học sinh có thể vận dụng ngay lý thuyết, nắm bài một cách hiệu quả nhất. Mời các bạn đón xem:
Lý thuyết Ammonia. Muối ammonium (Kết nối tri thức) hay, chi tiết | Lý thuyết Hóa học 11
Bài giải Bài 5: Ammonia. Muối ammonium
A. Lý thuyết Ammonia. Muối ammonium
1. Ammonia
a. Cấu tạo phân tử
Phân tử ammonia được tạo bởi một nguyên tử nitrogen liên kết với ba nguyên tử hydrogen và có dạng hình học là chóp tam giác:
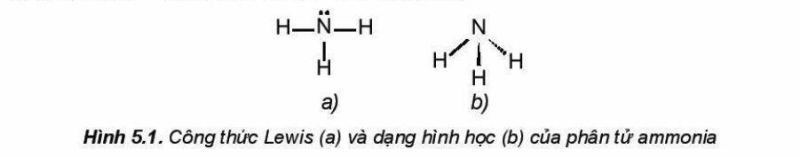
Đặc điểm cấu tạo của phân tử ammonia:
- Nguyên tử nitrogen còn một cặp electron không liên kết, tạo ra vùng có mật độ điện tích âm trên nguyên tử nitrogen
- Liên kết N-H phân cực, cặp electron dùng chung lệch về nguyên tử nitrogen làm cho nguyên tử hydrogen mang một phần đến Tịch Dương.
- Liên kết N-H tương đối bền với năng lượng liên kết là386 kJ/mol.
b. Tính chất vật lí
Ammonia tồn tại ở cả trong môi trường đất, nước, không khi. Trong cơ thể người. ammonia được tạo ra trong quá trình chuyển hoá thức ăn chứa protein.
Ở điều kiện thường, ammonia tồn tại ở thể khí, không màu, nhẹ hơn không khí, mùi khai và xốc. Ammonia tan nhiều trong nước. Ở điều kiện thường, 1 lít nước hoà tan được khoảng 700 lit khi ammonia. Ammonia dễ hoá lỏng (hoá lỏng ở -33,3 °C) và dễ hoá rắn (hóa rắn ở –77,7 °C).
c. Tính chất hoá học
* Tính base:
Dung dịch ammonia có môi trường base yếu, làm quỳ tím chuyển màu xanh, phenolphthalein chuyển màu hồng.
Ở thể khí, ammonia cũng có khả năng nhận proton, thể hiện tính chất của một base Bronsted-Lowry.
Ví dụ: NH3(g) + HCl(g) → NH4Cl(s)
* Tính khử
Trong phân tử ammonia, nguyên tử nitrogen có số oxi hoá −3 (số oxi hóa thấp nhất của nitrogen) nên ammonia thể hiện tính khử.
d. Ứng dụng
- Tác nhân làm lạnh.
- Sản xuất nitric acid.
- Dung môi.
- Sản xuất phân đạm.
e. Sản xuất
Trong công nghiệp, quá trình sản xuất ammonia thường được thực hiện ở nhiệt độ 400 °C – 450 °C, áp suất 150 – 200 bar, xúc tác Fe.
2. Muối Ammonium
a. Tính tan, sự điện li
Hầu hết các muối ammonium đều dễ tan trong nước và phân li hoàn toàn ra ion.
Ví dụ: NH4Cl → NH4+ + Cl-
b. Tác dụng với kiềm
Khi đun nóng hỗn hợp muối ammonium với dung dịch kiềm, sinh ra khí ammunia với mùi khai.
Ví dụ: (NH4)2SO4 +2NaOH → Na2SO4 +2NH3 + 2H2O
c. Tinh chất kém bền nhiệt
Các muối ammonium đều kém bền nhiệt và dễ bị phân huỷ khi nung nóng.
d. Ứng dụng
- Thuốc long đờm
- Phân bón hóa học
- Chất phụ gia thực phẩm
- Chất đánh sạch bề mặt kim loại
- Thuốc bổ sung chất điện giải
Sơ đồ tư duy Ammonia. Muối ammonium

B. Trắc nghiệm Ammonia. Muối ammonium
Đang cập nhật ...
Xem thêm Lý thuyết các bài Hoá học 11 Kết nối tri thức hay, chi tiết khác:
Lý thuyết Bài 6: Một số hợp chất của nitrogen với oxygen
Lý thuyết Bài 7: Sulfur và sulfur dioxide
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.