Toptailieu.vn xin giới thiệu Lý thuyết pH của dung dịch. Chuẩn độ acid – base (Cánh diều) hay, chi tiết | Lý thuyết Hóa học 11. Bài viết gồm phần lý thuyết trọng tâm nhất được trình bày một cách dễ hiểu, dễ nhớ bên cạnh đó là bộ câu hỏi trắc nghiệm có hướng dẫn giải chi tiết để học sinh có thể vận dụng ngay lý thuyết, nắm bài một cách hiệu quả nhất. Mời các bạn đón xem:
Nội dung bài viết
Lý thuyết pH của dung dịch. Chuẩn độ acid – base (Cánh diều) hay, chi tiết | Lý thuyết Hóa học 11
Bài giải Bài 3: pH của dung dịch. Chuẩn độ acid – base
A. Lý thuyết pH của dung dịch. Chuẩn độ acid – base
I. pH của dung dịch, chất chỉ thị
1. pH của dung dịch
|
pH = -lg[H+] hoặc [H+] = 10-pH |
với [H+] là nồng độ mol của ion H+.
- Môi trường acid có pH < 7.
- Môi trường base có pH > 7.
- Môi trường trung tính có pH = 7.
2. Ý nghĩa của pH trong thực tiễn
- pH có ý nghĩa trong tự nhiên, trong sản xuất và trong cơ thể sống xảy ra trong dung dịch nước với sự có mặt của các acid – base.
3. Xác định pH bằng chất chỉ thị
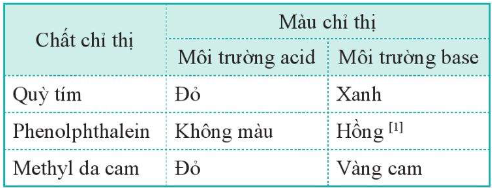
II. Chuẩn độ dung dịch acid và base
Nguyên tắc: Chuẩn độ là phương pháp xác định nồng độ của một chất bằng một dung dịch chuẩn đã biết nồng độ.
Sơ đồ tư duy pH của dung dịch. Chuẩn độ acid – base
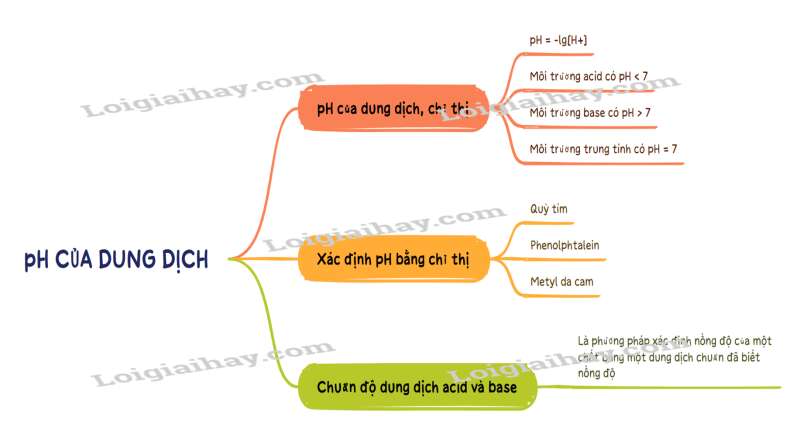 B. Bài tập pH của dung dịch. Chuẩn độ acid – base
B. Bài tập pH của dung dịch. Chuẩn độ acid – base
Đang cập nhật ...
Xem thêm Lý thuyết các bài Hoá học 11 Cánh Diều hay, chi tiết khác:
Lý thuyết Bài 2: Sự điện li trong dung dịch nước. Thuyết Br∅nsted – Lowry về acid - base
Lý thuyết Bài 4: Đơn chất nitrogen
Lý thuyết Bài 5: Một số hợp chất quan trọng của nitrogen
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.