Toptailieu.vn biên soạn và giới thiệu các kiến thức lý thuyết trọng tâm bao gồm định nghĩa, tính chất, ứng dụng và cách điều chế của ankan trong bài viết dưới đây, giúp học sinh ôn tập và bổ sung kiến thức cũng như hoàn thành tốt các bài kiểm tra môn Hóa học. Mời các bạn đón xem:
Nội dung bài viết
1. Định nghĩa Benzen là gì?
Benzen là chất lỏng, không màu, không tan trong nước, nhẹ hơn nước, hòa tan nhiều chất như: dầu ăn, nến, cao su, iot....Benzen có mùi thơm nhẹ nhưng có hại cho sức khỏe.
- Công thức phân tử: C6H6.
- Công thức cấu tạo:
2. Dãy đồng đẳng benzen
Benzen C6H6 và hidrocacbon thơm khác có công thức phân tử là C7H8 (toluen), C8H10,... lập thành dãy đồng đẳng có công thức phân tử chung CnH2n-6 với n≥6
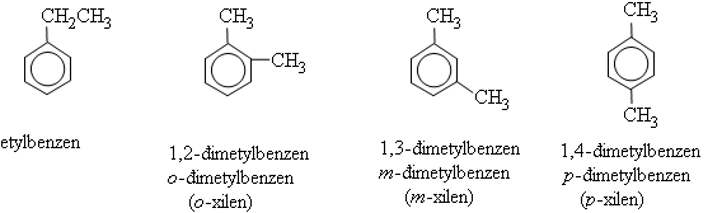
Dãy đồng đẳng của benzen bao gồm:
3. Đồng phân
Trừ C6H6 ( benzen ) là chất duy nhất không có đồng phân thì tất cả các chất còn lại trong dãy đồng đẳng benzen đều có đồng phân. Đặc biệt, từ công thức phân tử C8H10 trở đi đều tồn tại 2 dạng đồng phân là đồng phân mạch cacbon và đồng phân về vị trí của các nhóm ankyl xung quanh vòng benzen.
4. Danh pháp của benzen
- Khi coi vòng benzen là mạch chính thì các nhóm ankyl đính với nó là mạch nhánh (còn gọi là nhóm thế).
- Tên gọi: Tên vị trí – tên nhánh + benzen
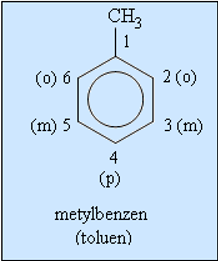
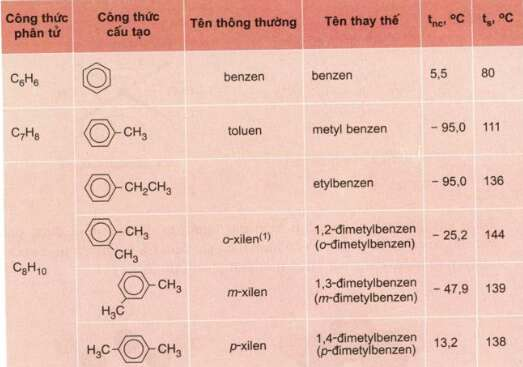
Tên và hằng số vật lí của một số hidrocacbon thơm đầu dãy đồng đẳng
 5. Tính chất vật lý của benzen
5. Tính chất vật lý của benzen
Benzen là chất lỏng, không màu, không tan trong nước, nhẹ hơn nước, hòa tan nhiều chất như: dầu ăn, nến, cao su, iot....Benzen độc.
6. Tính chất hóa học của benzen
Phản ứng thế
a) Phản ứng halogen hóa
• Khi có bột sắt, benzen tác dụng với brom khan tạo thành brombenzen và khí hiđro bromua.
• Nếu không dùng sắt mà chiếu sáng (as) thì Brom thế cho hiđro ở nhánh.
b) Phản ứng nitro hóa
Benzen tác dụng với hỗn hợp HNO3 đặc và H2SO4 đậm đặc tạo thành nitrobenzen:
Nitro benzen tác dụng với hỗn hợp axit HNO3 bốc khói và H2SO4 đậm đặc đồng thời đun nóng thì tạo thành m-đinitrobenzen.
c) Quy tắc thế ở vòng benzen
Khi vòng benzen đã có sắn nhóm ankyl (hay các nhóm –OH, -NH2, -OCH3,...
Phản ứng thế vào vòng sẽ dễ dàng hơn và ưu tiên xảy ra ở vị trí nhóm ortho và para. Ngược lại, nếu ở vòng benzen đã có sẵn nhóm –NO2 (hoặc các nhóm –COOH, -SO3H, ...) phản ứng thế vào vòng sẽ khó hơn và ưu tiên xảy ra ở vị trí meta.
d) Cơ chế phản ứng thế ở vòng benzen
Phân tử halogen hoặc phân tử axit nitric không trực tiếp tấn công. Các tiểu phân mag điện tích dương tạo thành do tác dụng của chúng với xúc tác mới là tác nhân tấn công trực tiếp vào vòng benzen. Thí dụ:
Phản ứng cộng
- Benzen không tác dụng được với brom trong dung dịch, chứng tỏ benzen khó tham gia phản ứng cộng hơn etilen và axetilen. Tuy nhiên, trong điều kiện thích hợp, benzen có phản ứng cộng với một số chất:
Do phân tử có cấu tạo đặc biệt nên benzen vừa có phản ứng thế vừa có phản ứng cộng. Tuy nhiên phản ứng cộng của benzen xảy ra khó hơn so với etilen và axetilen.
Phản ứng oxi hóa
• Benzen không tác dụng với KMnO4 (không làm mất màu dung dịch KMnO4).
• Cũng như các hiđrocacbon khác, benzen cháy dễ tạo ra khí cacbon đioxit và hơi nước.
C6H6 + O2 → 6CO2 + 3H2O
Tuy nhiên, khi benzen cháy trong không khí, ngoài cacbon đioxit và hơi nước còn sinh ra muội than.
Benzen tương đối dễ tham gia phản ứng thế, khó tham gia phản ứng cộng và bền vững các chất oxi hóa. Đây cũng là tính chất hóa học đặc trưng của hiđrocacbon thơm nên được gọi là tính thơm.
Benzen thường được tách bằng cách chưng cất dầu mỏ và nhựa than đá. Chúng còn được điều chế từ ankan hoặc xicloankan
CH3[CH2]4CH3 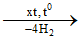
Benzen là nguyên liệu quan trọng nhất của công nghiệp hóa hữu cơ.
Benzen được dùng nhiều chất để tổng hợp các monome trong sản xuất polime làm chất dẻo, cao su, tơ sợi (chẳng hạn poli stiren, cao su buna – stiren, tơ capron). Từ benzen người ta điều chế ra nitrobenzen, anilin, phenol để dùng tổng hợp phẩm nhuộm, dược phẩm, thuốc trừ dịch hại,...
Benzen được sử dụng làm dung môi trong công nghiệp và trong phòng thí nghiệm.
Xem thêm các chất hữu cơ chi tiết khác:
Ancol: Tính chất vật lý, tính chất hóa học, ứng dụng và cách điều chế
Stiren: Tính chất vật lý, tính chất hóa học, ứng dụng và cách điều chế
Phenol: Tính chất vật lý, tính chất hóa học, ứng dụng và cách điều chế
Andehit: Tính chất vật lý, tính chất hóa học, ứng dụng và cách điều chế
Xeton: Tính chất vật lý, tính chất hóa học, ứng dụng và cách điều chế
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.