Toptailieu.vn biên soạn và giới thiệu Top 30 Đề thi Giữa học kì 1 Hóa học 10 (Kết nối tri thức 2023) tải nhiều nhất gồm các đề thi được tuyển chọn và tổng hợp từ các đề thi môn Hóa học THPT trên cả nước có hướng dẫn giải chi tiết giúp học sinh làm quen với các dạng đề, ôn luyện để đạt kết quả cao trong kì thi sắp tới. Mời các bạn đón xem:
Nội dung bài viết
Top 30 Đề thi Giữa học kì 1 Hóa học 10 (Kết nối tri thức 2023) tải nhiều nhất
Đề thi Giữa học kì 1 Hóa học 10 Kết nối tri thức - Đề số 1
Phòng Giáo dục và Đào tạo ...
Đề thi Giữa kì 1 - Kết nối tri thức
Năm học 2022 - 2023
Môn: Hóa học lớp 10
Thời gian làm bài: phút
(không kể thời gian phát đề)
(Đề số 1)
Phần I: Trắc nghiệm (7 điểm)
Câu 1: Nội dung nào dưới đây thuộc đối tượng nghiên cứu của hóa học?
A. Tốc độ ánh sáng trong chân không.
B. Cấu tạo của chất và sự biến đổi của chất.
C. Quá trình phân chia tế bào.
D. Sự hình thành hệ Mặt Trời.
Câu 2: Trong thành phần nguyên tử, những hạt mang điện tích là
A. proton và alpha.
B. proton và neutron.
C. proton và electron.
D. electron và neutron.
Câu 3: Nguyên tử không mang điện vì
A. có tổng số hạt proton bằng tổng số hạt electron.
B. có tổng số hạt electron bằng tổng số hạt neutron.
C. tổng số hạt neutron bằng tổng số hạt proton.
D. được tạo nên bởi các hạt không mang điện.
Câu 4: Nếu đường kính của hạt nhân nguyên tử khoảng 10-2 pm thì đường kính của nguyên tử khoảng
A. 102 pm.
B. 10-4 pm.
C. 10-2 pm.
D. 104 pm.
Câu 5: Trong tự nhiên, argon có các đồng vị 40Ar, 38Ar, 36Ar chiếm tương ứng khoảng 99,604%, 0,063% và 0,333% số nguyên tử. Nguyên tử khối trung bình của Ar gần nhất với đáp án là
A. 36,99.
B. 38,99.
C. 39,66.
D. 39,99.
Câu 6: Nguyên tử potassium (K) có 19 electron; 19 proton và 20 neutron. Số khối của nguyên tử potassium là
A.20. B.19. C.39. D.58.
Câu 7: Dãy nào sau đây gồm các đồng vị của cùng một nguyên tố hóa học?
Câu 8: Tất cả các nguyên tử có số đơn vị điện tích hạt nhân là 8 đều thuộc nguyên tố nào sau đây?
A. Hydrogen.
B. Helium.
C. Carbon.
D. Oxygen.
Câu 9: Orbital nguyên tử (kí hiệu là AO) là
A.khu vực không gian xung quanh hạt nhân nguyên tử mà xác suất tìm thấy proton trong khu vực đó là lớn nhất (khoảng 90%).
B.khu vực không gian trong hạt nhân nguyên tử mà xác suất tìm thấy electron trong khu vực đó là lớn nhất (khoảng 90%).
C.khu vực không gian xung quanh hạt nhân nguyên tử mà xác suất tìm thấy electron trong khu vực đó là nhỏ nhất (khoảng 10%).
D.khu vực không gian xung quanh hạt nhân nguyên tử mà xác suất tìm thấy electron trong khu vực đó là lớn nhất (khoảng 90%).
Câu 10: Mỗi orbital nguyên tử chứa tối đa bao nhiêu electron?
A. 1 electron.
B. 2 electron.
C. 3 electron.
D. 4 electron.
Câu 11: Lớp M có số phân lớp electron là
A. 1. B. 2. C. 3. D. 4.
Câu 12: Orbital p có dạng hình gì?
A. Hình cầu.
B. Hình tròn.
C. Hình bầu dục.
D. Hình số tám nổi.
Câu 13: Nguyên tử của nguyên tố neon (Z = 10) có cấu hình electron là
A. 1s22s22p63s2.
B. 1s22s22p6.
C. 1s22s22p63s1.
D. 1s22s22p43s2.
Câu 14: Nguyên tử của nguyên tố potassium có 19 electron. Ở trạng thái cơ bản, potassium có số electron độc thân là
A. 1. B. 2. C. 0. D. 3.
Câu 15: Mendeleev sắp xếp các nguyên tố hóa học vào bảng tuần hoàn dựa theo quy luật về
A. số hiệu nguyên tử.
B. số khối.
C. khối lượng nguyên tử.
D. cấu hình electron.
Câu 16: Các nguyên tố có cùng số lớp electron trong nguyên tử được xếp thành một hàng, gọi là
A.chu kì.
B.ô nguyên tố.
C.nhóm.
D.bảng tuần hoàn.
Câu 17: Nguyên tố Mg thuộc chu kì 3 của bảng tuần hoàn. Nguyên tử nguyên tố Mg có số lớp electron là
A. 1. B. 2. C. 3. D. 4.
Câu 18: Bảng tuần hoàn hiện nay có bao nhiêu cột?
A. 2. B. 8. C. 18. D. 32.
Câu 19: Trong các nguyên tố O, F, Cl, Se, nguyên tố có tính phi kim mạnh nhất là
A. O. B. F. C. Se. D. Cl.
Câu 20: Xét ba nguyên tử nguyên tố có cấu hình electron lần lượt là
X: 1s22s22p63s1
Q: 1s22s22p63s2
Z: 1s22s22p63s23p1
Tính base tăng dần của các hydroxide là
A. XOH < Q(OH)2 < Z (OH)3.
B. Z(OH)3 < XOH < Q (OH)2.
C. Z(OH)3 < Q(OH)2 < XOH.
D. XOH < Z(OH)2 < Q(OH)2.
Câu 21: Phát biểu nào sau đây là sai?
A.Tính kim loại là tính chất của một nguyên tố mà nguyên tử dễ nhường electron.
B. Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân tính kim loại của các nguyên tố giảm dần, tính phi kim tăng dần.
C. Trong một nhóm, theo chiều tăng dần của điện tích hạt nhân tính kim loại của các nguyên tố giảm dần, tính phi kim tăng dần.
D. Tính phi kim là tính chất của một nguyên tố mà nguyên tử dễ nhận electron
Câu 22: Trong các hydroxide dưới đây. Hydroxide lưỡng tính là
A.Al(OH)3.
B.Mg(OH)2.
C.NaOH.
D.LiOH.
Câu 23: X là nguyên tố nhóm IIA. Công thức oxide ứng với hóa trị cao nhất của X là
A. XO. B. XO2. C. X2O. D. X2O2.
Câu 24: Nguyên tố X thuộc chu kì 3 nhóm VIIA. Công thức hóa học của hydroxide (ứng với hóa trị cao nhất) của X là
A. H2XO3.
B. HX.
C. H2XO4.
D. HXO4.
Câu 25: Nguyên tử X có 15 electron ở lớp vỏ. Trong bảng tuần hoàn, nguyên tố X thuộc chu kì nào?
A. 4. B. 2. C. 5. D. 3.
Câu 26: Yếu tố nào của nguyên tố hóa học cho dưới đây không biến đổi tuần hoàn theo chiều tăng của điện tích hạt nhân nguyên tử?
A. Tính kim loại.
B. Tính acid – base của các hydroxide.
C. Khối lượng nguyên tử.
D. Tính phi kim.
Câu 27: Nguyên tố Ca có số hiệu nguyên tử là 20. Phát biểu nào sau đây về Ca là không đúng?
A. Số electron ở vỏ nguyên tử của nguyên tố Ca là 20.
B. Vỏ của nguyên tử Ca có 4 lớp electron và lớp ngoài cùng có 2 electron.
C. Hạt nhân của nguyên tử Ca có 20 proton
D. Nguyên tố Ca là một nguyên tố phi kim.
Câu 28: Đại lượng đặc trưng cho khả năng hút electron của một nguyên tử khi tạo thành liên kết hóa học là
A.bán kính nguyên tử.
B.độ âm điện.
C.năng lượng ion hóa.
D.điện tích hạt nhân.
Phần II: Tự luận (3 điểm)
Câu 1 (1 điểm): Nguyên tử X có tổng số các loại hạt bằng 52, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 16 hạt. Xác định thành phần các hạt cấu tạo nên nguyên tử X.
Câu 2 (1 điểm): Xác định vị trí (ô, chu kì và nhóm) của các nguyên tố sau (có giải thích ngắn gọn cách xác định):
a. Nguyên tố A có số hiệu nguyên tử là 20.
b. Nguyên tố B có số đơn vị điện tích hạt nhân là 9.
Câu 3 (1 điểm): Sắp xếp các nguyên tố sau: O (Z = 8), S (Z = 16), F (Z = 9) theo chiều tăng dần tính phi kim (có giải thích ngắn gọn).
Hướng dẫn giải:
Phần I: Trắc nghiệm
|
1-B |
2-C |
3-A |
4-A |
5-D |
6-C |
7-C |
8-D |
9-D |
10-B |
|
11-C |
12-D |
13-B |
14-A |
15-C |
16-A |
17-C |
18-C |
19-B |
20-C |
|
21-C |
22-A |
23-A |
24-D |
25-D |
26-C |
27-D |
28-B |
Câu 1:
Đáp án đúng là: B
Hóa học nghiên cứu về thành phần, cấu trúc, tính chất, sự biến đổi của các chất và các hiện tượng kèm theo.
Vậy nội dung thuộc đối tượng nghiên cứu của hóa học là: Cấu tạo của chất và sự biến đổi của chất.
Câu 2:
Đáp án đúng là: C
Trong nguyên tử:
- Hạt proton mang điện tích dương;
- Hạt electron mang điện tích âm;
- Hạt neutron không mang điện.
Câu 3:
Đáp án đúng là: A
Nguyên tử không mang điện (trung hòa về điện) vì có tổng số hạt proton (mang điện tích dương) bằng tổng số hạt electron (mang điện tích âm).
Câu 4:
Đáp án đúng là: A
Kích thước của nguyên tử lớn hơn khoảng 10 000 lần kích thước của hạt nhân nguyên tử.
Nếu đường kính của hạt nhân nguyên tử khoảng 10-2 pm thì đường kính của nguyên tử khoảng10-2.10 000 = 102pm.
Câu 5:
Đáp án đúng là: D
Nguyên tử khối trung bình của argon là:
ˉAAr=40×99,604+38×0,063+36×0,33399,604+0,063+0,333≈39,99.
Câu 6:
Đáp án đúng là: C
Nguyên tử potassium có số khối (A) = số proton + số neutron = 19 + 20 = 39.
Câu 7:
Đáp án đúng là: C
Dãy 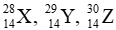
Câu 8:
Đáp án đúng là: D
Tất cả nguyên tử có số đơn vị điện tích hạt nhân là 8 thuộc nguyên tố oxygen dù chúng có thể có số neutron khác nhau.
Câu 9:
Đáp án đúng là: D
Orbital nguyên tử (kí hiệu là AO) là khu vực không gian xung quanh hạt nhân nguyên tử mà xác suất tìm thấy electron trong khu vực đó là lớn nhất (khoảng 90%).
Câu 10:
Đáp án đúng là: B
Mỗi orbital nguyên tử chứa tối đa 2 electron có chiều tự quay ngược nhau (nguyên lí loại trừ Pauli).
Câu 11:
Đáp án đúng là: C
Phân lớp M (n = 3) có 3 phân lớp là 3s, 3p và 3d.
Câu 12:
Đáp án đúng là: D
Orbital p có dạng hình số tám nổi.
Câu 13:
Đáp án đúng là: B
Neon có số electron bằng số hiệu nguyên tử = 10.
⇒ Cấu hình electron của nguyên tử neon là 1s22s22p6.
Câu 14:
Đáp án đúng là: A
Cấu hình electron của potassium là 1s22s22p63s23p64s1 có thể được biểu diễn theo ô orbital như sau:
⇒ Ở trạng thái cơ bản potassium có 1 electron độc thân.
Câu 15:
Đáp án đúng là: C
Mendeleevsắp xếp các nguyên tố hóa học vào bảng tuần hoàn dựa theo quy luật về khối lượng nguyên tử.
Câu 16:
Đáp án đúng là: A
Các nguyên tố có cùng số lớp electron trong nguyên tử được xếp thành một hàng, gọi là chu kì.
Câu 17:
Đáp án đúng là: C
Chú ý: Số lớp electron = số thứ tự chu kì
Nguyên tố Mg thuộc chu kì 3, có số lớp electron là 3.
Câu 18:
Đáp án đúng là: C
Bảng tuần hoàn hiện nay có 18 cột, chia thành 8 nhóm A (IA đến VIIIA) và 8 nhóm B (IB đến VIIIB), riêng nhóm VIIIB có 3 cột.
Câu 19:
Đáp án đúng là: B
Fluorine (F) là nguyên tố có độ âm điện lớn nhất trong bảng tuần hoàn nên có tính phi kim mạnh nhất.
Câu 20:
Đáp án đúng là: C
Ta thấy các nguyên tố trên đều thuộc chu kì 3 trong bảng tuần hoàn.
Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân, tính base của hydroxide tương ứng giảm dần.
⇒ Sắp xếp theo chiều tính base tăng dần: Z(OH)3 < Q(OH)2 < XOH.
Câu 21:
Đáp án đúng là: C
Phát biểu C sai vì: Trong một nhóm, theo chiều tăng dần của điện tích hạt nhân, lực hút giữa hạt nhân với các electron lớp ngoài cùng giảm. Do đó, tính kim loại của các nguyên tố tăng dần, tính phi kim giảm dần.
Câu 22:
Đáp án đúng là: A
Al(OH)3 là hydroxide lưỡng tính
Al(OH)3 thể hiện tính acid khi tác dụng với base:
Al(OH)3 + NaOH ⟶ Na[Al(OH)4]
Al(OH)3 thể hiện tính base khi tác dụng với acid:
Al(OH)3 + 3HCl ⟶ AlCl3 + 3H2O.
Câu 23:
Đáp án đúng là: A
X là nguyên tố nhóm IIA nên hóa trị của X trong oxide cao nhất là II. Công thức oxide ứng với hóa trị cao nhất của X là: XO.
Câu 24:
Đáp án đúng là: D
Nguyên tố X thuộc chu kì 3, nhóm VIIA. Công thức hóa học của hydroxide (ứng với hóa trị cao nhất) của X là HXO4.
Câu 25:
Đáp án đúng là: D
Cấu hình electron nguyên tử của X là 1s22s22p63s23p3
Dựa vào cấu hình electron nguyên tử ta thấy X có 3 lớp electron, vậy X thuộc chu kì 3.
Câu 26:
Đáp án đúng là: C
Khối lượng nguyên tử không biến đổi tuần hoàn theo chiều tăng của điện tích hạt nhân nguyên tử.
Câu 27:
Đáp án đúng là: D
Nguyên tố Ca có số hiệu nguyên tử là 20
⇒ Số hiệu nguyên tử (Z) = số proton = số electron = 20.
Cấu hình electron nguyên tử: 1s22s22p63s23p64s2
⇒ Vỏ của nguyên tử Ca có 4 lớp electron và lớp ngoài cùng có 2 electron.
⇒ Nguyên tố Ca là một nguyên tố kim loại.
Câu 28:
Đáp án đúng là: B
Đại lượng đặc trưng cho khả năng hút electron của một nguyên tử khi tạo thành liên kết hóa học là độ âm điện.
Phần II: Tự luận
Câu 1:
Gọi P, N và E lần lượt là số proton, neutron và electron của X. Trong đó P = E.
Nguyên tử X có tổng số các loại hạt bằng 52 nên:
P + N + E = 52 hay 2P + N = 52 (1)
Trong nguyên tử X, số hạt mang điện nhiều hơn số hạt không mang điện là 16 hạt nên:
(P + E) – N = 16 hay 2P – N = 16 (2)
Từ (1) và (2) ta có hệ phương trình:
Vậy trong X có 17 proton; 17 electron và 18 neutron.
Câu 2:
a) Nguyên tố A (Z = 20), cấu hình electron: 1s22s22p63s23p64s2
Nguyên tố A thuộc ô 20 (do Z = 20); chu kì 4 (do có 4 lớp electron); nhóm IIA (do nguyên tố s, 2 electron hóa trị).
b) Nguyên tố B (Z = 9), cấu hình electron: 1s22s22p5
Nguyên tố B thuộc ô 9 (do Z = 9); chu kì 2 (do có 2 lớp electron); nhóm VIIA (do nguyên tố p, 7 electron hóa trị).
Câu 3:
O (Z = 8): 1s22s22p4, suy ra O thuộc chu kì 2, nhóm VIA.
S (Z = 16): [Ne]3s23p4, suy ra S thuộc chu kì 3, nhóm VIA.
F (Z = 9): 1s22s22p5, suy ra F thuộc chu kì 2, nhóm VIIA.
Ta có:
O và F thuộc cùng một chu kì 2. Theo chiều điện tích hạt nhân tăng dần ta được tính phi kim F > O (1).
O và S thuộc cùng một nhóm VIA. Theo chiều điện tích hạt nhân tăng dần ta được tính phi kim O > S (2)
Từ (1) và (2) ⇒ Tính phi kim: S < O < F.
Ma trận đề kiểm tra giữa kì I – Hóa học 10 – bộ sách KNTT
|
TT |
Chủ đề |
Nội dung/đơn vị kiến thức |
Mức độ nhận thức |
Tổng số câu |
Tổng % điểm |
||||||||
|
Nhận biết |
Thông hiểu |
Vận dụng |
Vận dụng cao |
||||||||||
|
Số câu TN |
Số câu TL |
Số câu TN |
Số câu TL |
Số câu TN |
Số câu TL |
Số câu TN |
Số câu TL |
TN |
TL |
||||
|
(1) |
(2) |
(3) |
(4) |
(5) |
(6) |
(7) |
(8) |
(9) |
(10) |
(11) |
(12) |
(13) |
(14) |
|
1 |
Mở đầu |
1 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
1 (0,25đ) |
0 |
2,5% |
|
|
2 |
Cấu tạo nguyên tử |
Thành phần của nguyên tử |
2 |
0 |
1 |
0 |
0 |
1 |
0 |
0 |
3 (0,75đ) |
1 (1đ) |
17,5% |
|
Nguyên tố hóa học |
2 |
0 |
2 |
0 |
0 |
0 |
0 |
0 |
4 (1đ) |
0 |
10% |
||
|
Cấu trúc lớp vỏ electron nguyên tử |
3 |
0 |
3 |
0 |
0 |
0 |
0 |
0 |
6 (1,5đ) |
0 |
15% |
||
|
3 |
Bảng tuần hoàn các nguyên tố hóa học và định luật tuần hoàn |
Cấu tạo của bảng tuần hoàn các nguyên tố hóa học |
2 |
0 |
2 |
0 |
0 |
1 |
0 |
0 |
4 (1đ) |
1 (1đ) |
20% |
|
Xu hướng biến đổi một số tính chất của nguyên tử các nguyên tố trong một chu kì và nhóm |
2 |
0 |
2 |
0 |
0 |
0 |
0 |
1 |
4 (1đ) |
1 (1đ) |
20% |
||
|
Xu hướng biến đổi thành phần và một số tính chất của hợp chất trong một chu kì |
2 |
0 |
1 |
0 |
0 |
0 |
0 |
0 |
3 (0,75đ) |
0 |
7,5% |
||
|
Định luật tuần hoàn. Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học |
2 |
0 |
1 |
0 |
0 |
0 |
0 |
0 |
3 (0,75đ) |
0 |
7,5% |
||
|
Tổng (câu/ điểm) |
16 (4đ) |
0 |
12 (3đ) |
0 |
0 |
2 (2đ) |
0 |
1 (1đ) |
31 (10đ) |
||||
|
Tỉ lệ % điểm |
40 |
0 |
30 |
0 |
0 |
20 |
0 |
10 |
100% |
||||
|
Tổng hợp chung |
40% |
30% |
20% |
10% |
100% |
||||||||
Lưu ý:
- Hình thức kiểm tra: Kết hợp giữa trắc nghiệm và tự luận (tỉ lệ 70% trắc nghiệm, 30% tự luận).
- Cấu trúc:
+ Mức độ đề: 40% Nhận biết; 30% Thông hiểu; 20% Vận dụng; 10% Vận dụng cao.
+ Phần trắc nghiệm: 28 câu, 7,0 điểm (gồm 16 câu ở mức độ nhận biết;12 câu ở mức độ thông hiểu), mỗi câu 0,25 điểm;
+ Phần tự luận: 3,0 điểm (Vận dụng: 02 câu, 2,0 điểm; Vận dụng cao: 1-2 câu, 1,0 điểm).
- Các câu hỏi ở mức độ nhận biết và thông hiểu là các câu hỏi trắc nghiệm khách quan 4 lựa chọn, trong đó có duy nhất 1 lựa chọn đúng; các câu hỏi ở mức độ vận dụng và vận dụng cao là các câu hỏi tự luận.
- Với các câu hỏi TNKQ ở mức độ nhận biết và mức độ thông hiểu, mỗi câu hỏi kiểm tra, đánh giá 01 yêu cầu cần đạt của chương trình.
- Không chọn câu ở mức độ vận dụng và câu ở mức độ vận dụng cao trong cùng một đơn vị kiến thức.
Đề thi Giữa học kì 1 Hóa học 10 Kết nối tri thức - Đề số 2
Phòng Giáo dục và Đào tạo ...
Đề thi Giữa kì 1 - Kết nối tri thức
Năm học 2022 - 2023
Môn: Hóa học lớp 10
Thời gian làm bài: phút
(không kể thời gian phát đề)
(Đề số 2)
Phần I: Trắc nghiệm (7 điểm)
Câu 1: Hóa học là ngành khoa học thuộc lĩnh vực nào sau đây?
A.Khoa học hình thức.
B.Khoa học xã hội.
C.Khoa học tự nhiên.
D.Khoa học ứng dụng.
Câu 2: Hầu hết hạt nhân các nguyên tử được cấu tạo bởi các loại hạt nào sau đây?
A. Proton và electron.
B. Proton, electron và neutron.
C. Proton và neutron.
D. Electron và neutron.
Câu 3: Trường hợp nào sau đây có sự tương ứng giữa hạt cơ bản với khối lượng và điện tích của chúng?
A. Electron, m ≈ 1 amu, q = -1.
B. Proton, m≈ 1 amu, q = -1.
C. Proton, m ≈ 0,00055 amu, q = +1.
D. Neutron, m ≈ 1 amu, q = 0.
Câu 4: Nguyên tử fluorine chứa 9 electron và có số khối là19. Tổng số hạt proton, electron và neutron trong nguyên tử fluorine là
A. 30. B. 32. C. 19. D. 28.
Câu 5: Số hiệu nguyên tử cho biết thông tin nào sau đây?
A. Số khối.
B. Nguyên tử khối trung bình.
C. Số proton.
D. Số neutron.
Câu 6: Cho kí hiệu nguyên tử sau: 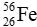
A. Số đơn vị điện tích hạt nhân là 26.
B. Tổng số proton và số neutron là 26.
C. Số neutron là 30.
D. Số khối là 56.
Câu 7: Nguyên tử magnesium có 12 electron. Điện tích hạt nhân của nguyên tử này là
A.12+. B.12. C.+12. D.-12.
Câu 8: Trong tự nhiên, nguyên tố bromine có 2 đồng vị. Trong đó 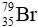
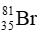
A.79,5.
B.79,1.
C.80,01.
D.35.
Câu 9: Số orbital trong các phân lớp s, p, d lần lượt là
A. 3, 5, 7.
B. 1, 2, 3.
C. 1, 3, 5.
D. 1, 2, 4.
Câu 10: Số electron tối đa trong lớp M là
A. 8. B. 18. C. 32. D. 2.
Câu 11: Ở trạng thái cơ bản, số electron độc thân trong nguyên tử O (Z = 8) là
A.0. B.1. C.3. D.2.
Câu 12: Nguyên tử X có 3 lớp electron, lớp thứ ba có 2 electron. Số hiệu nguyên tử X là
A.12. B.13. C.14. D.15.
Câu 13: Cấu hình electron nguyên tử chlorine (Z = 17) là
A. 1s22s22p63s23p2.
B. 1s22s22p63s23p5.
C. 1s22s22p63s23p3.
D. 1s22s22p63s23p4.
Câu 14: Cho biết nguyên tố A có 15 proton trong hạt nhân. A là
A.kim loại.
B.phi kim.
C.khí hiếm.
D.khí trơ.
Câu 15: Nguyên tử các nguyên tố thuộc cùng một chu kì có cùng đặc điểm nào sau đây?
A.Số electron.
B.Số lớp electron.
C.Số electron hóa trị.
D. Số electron ở lớp ngoài cùng.
Câu 16: Bảng tuần hoàn hiện nay gồm
A. 18 chu kì, trong đó 8 chu kì nhỏ và 10 chu kì lớn.
B. 7 chu kì, trong đó 3 chu kì nhỏ và 4 chu kì lớn.
C. 7 chu kì, trong đó 4 chu kì nhỏ và 3 chu kì lớn.
D. 8 chu kì, trong đó 4 chu kì nhỏ và 4 chu kì lớn.
Câu 17: Nguyên tố Cl (Z = 17) thuộc nhóm nào trong bảng tuần hoàn các nguyên tố hóa học?
A. IA. B. IIA. C. VA. D. VIIA.
Câu 18: Chu kì 2 trong bảng tuần hoàn gồm bao nhiêu nguyên tố?
A. 2 nguyên tố.
B. 8 nguyên tố.
C. 18 nguyên tố.
D. 32 nguyên tố.
Câu 19: Đại lượng nào sau đây trong nguyên tử của các nguyên tố biến đổi tuần hoàn theo chiều tăng của điện tích hạt nhân nguyên tử?
A. Số lớp electron.
B. Số electron ở lớp ngoài cùng.
C. Nguyên tử khối.
D. Số electron trong nguyên tử.
Câu 20: Cấu hình electron hóa trị của nguyên tử các nguyên tố nhóm IIIA trong bảng tuần hoàn các nguyên tố hóa học đều là
A. np3.
B. ns3.
C. ns2np1.
D. ns2np4.
Câu 21: Theo độ âm điện của Pauling, nguyên tố có độ âm điện lớn nhất trong bảng tuần hoàn là
A.Fluorine.
B.Hydrogen.
C.Helium.
D.Oxygen.
Câu 22: Dãy nguyên tố nào sau đây sắp xếp theo chiều tăng dần độ âm điện?
A. Rb, K, Na, Li.
B. Na, Li, K, Rb.
C. Na, K, Rb, Li.
D. Li, Rb, Na, K.
Câu 23: X là nguyên tố thuộc nhóm VIA trong bảng tuần hoàn. Công thức oxide ứng với hóa trị cao nhất của X là
A. X2O3. B. X2O6. C. X3O. D. XO3.
Câu 24: Trong các chất dưới đây, chất nào có tính acid mạnh nhất?
A. H2SO4.
B. HClO4.
C. H3PO4.
D. H2SiO3.
Câu 25: Khi xếp theo chiều tăng dần của điện tích hạt nhân, đại lượng nào sau đây không biến đổi tuần hoàn?
A. Bán kính nguyên tử.
B. Số neutron.
C. Tính kim loại, tính phi kim.
D. Độ âm điện.
Câu 26: Nguyên tố X ở chu kì 3, nhóm IIA của bảng tuần hoàn. Cấu hình electron của nguyên tử nguyên tố X là
A. 1s22s22p6.
B. 1s22s22p63s23p1.
C. 1s22s22p63s3.
D. 1s22s22p63s2.
Câu 27: Nguyên tử nguyên tố G có cấu hình electron là [Ne]3s23p4. Vị trí của G trong bảng tuần hoàn là
A.ô thứ 16, chu kì 3, nhóm VIA.
B.ô thứ 26, chu kì 3, nhóm IVB.
C.ô thứ 16, chu kì 2, nhóm IVA.
D.ô thứ 26, chu kì 3, nhóm VIA.
Câu 28: Cho X (Z = 9), Y (Z = 17) và T (Z = 16). Các nguyên tố được sắp xếp theo thứ tự bán kính nguyên tử tăng dần là
A.X, Y, T.
B.T, Y, X.
C.X, T, Y.
D.Y, T, X.
Phần II. Tự luận (3 điểm)
Câu 1 (1 điểm): Chlorine có hai đồng vị bền là 35Cl và 37Cl. Nguyên tử khối trung bình của chlorine là 35,45. Tính tỉ lệ phần trăm số nguyên tử mỗi đồng vị của chlorine trong tự nhiên.
Câu 2 (1 điểm): Cation M+ và anion Y2- đều có cấu hình electron lớp ngoài cùng là 3s23p6. Hãy xác định vị trí của các nguyên tố M, Y trong bảng tuần hoàn, có giải thích ngắn gọn.
Câu 3 (1 điểm): Sắp xếp các nguyên tố sau: 3Li, 8O, 9F, 11Na theo chiều tăng dần bán kính nguyên tử, có giải thích ngắn gọn.
Đề thi Giữa học kì 1 Hóa học 10 Kết nối tri thức - Đề số 3
Phòng Giáo dục và Đào tạo ...
Đề thi Giữa kì 1 - Kết nối tri thức
Năm học 2022 - 2023
Môn: Hóa học lớp 10
Thời gian làm bài: phút
(không kể thời gian phát đề)
(Đề số 3)
Phần I: Trắc nghiệm (7 điểm)
Câu 1: Nội dung thuộc đối tượng nghiên cứu của hóa học là
A.quỹ đạo chuyển động của Trái đất.
B.tốc độ ánh sáng trong chân không.
C. sựtiến hóa của loài người.
D. sự biến đổi của các chất.
Câu 2: Một loại nguyên tử hydrogen có cấu tạo đơn giản nhất, chỉ tạo nên từ 1 electron và 1 proton (không chứa neutron). Phát biểu nào sau đây là đúng khi nói về nguyên tử hydrogen này?
A. Đây là nguyên tử nặng nhất trong số các nguyên tử được biết cho đến nay.
B. Khối lượng nguyên tử xấp xỉ 2 amu.
C. Hạt nhân nguyên tử có khối lượng gấp khoảng 1818 lần khối lượng lớp vỏ.
D. Kích thước của nguyên tử bằng kích thước của hạt nhân.
Câu 3: Nguyên tử gồm
A.hạt nhân chứa proton, neutron và vỏ nguyên tử chứa electron.
B.hạt nhân chứa proton, electron.
C.hạt nhân chứa proton, electron và vỏ nguyên tử chứa neutron.
D.hạt nhân và vỏ nguyên tử chứa proton.
Câu 4: Hạt nhân nguyên tử X có chứa 15 proton và 16 neutron. Số khối của hạt nhân nguyên tử X là
A. 30. B. 31. C. 32. D. 46.
Câu 5: Cho các nguyên tử sau: A (Z = 8, A = 16), B (Z = 9, A = 19), C (Z = 8, A = 17), D (Z = 7, A = 17). Trong các nguyên tử trên, các nguyên tử thuộc cùng một nguyên tố hóa học là
A. nguyên tử A và nguyên tử B.
B. nguyên tử C và nguyên tử D.
C. nguyên tử A và nguyên tử C.
D. nguyên tử B và nguyên tử C.
Câu 6: Nguyên tử nitrogen có 7 electron. Điện tích hạt nhân của nguyên tử này là
A.+7. B.-7. C.7+. D.7.
Câu 7: Một nguyên tử có chứa 11 electron và 12 neutron. Kí hiệu nguyên tử này là
Câu 8: Trong tự nhiên, lithium có 2 đồng vị là 7Li và 6Li. Nguyên tử khối trung bình của Li là 6,93. Phần trăm số nguyên tử của đồng vị 7Li là
A.93%. B.7%. C.78%. D.22%.
Câu 9: Hình ảnh dưới đây chỉ hình dạng của orbital nào?
A.Orbital s.
B.Orbital p.
C.Orbital d.
D.Orbital f.
Câu 10: Sự phân bố electron vào các lớp và phân lớp căn cứ vào
A. số khối.
B. điện tích hạt nhân.
C. nguyên tử khối.
D. mức năng lượng electron.
Câu 11: Lớp M chứa số electron tối đa là
A. 3. B.6. C. 9. D. 18.
Câu 12: Lớp electron thứ 4 còn được gọi là
A. Lớp K.
B. Lớp M.
C. Lớp N.
D. Lớp L.
Câu 13: Cấu hình electron của nguyên tử sulfur (Z = 16) là
A. 1s22s22p63s23p3.
B. 1s22s22p63s23p5.
C. 1s22s22p63s23p4.
D. 1s22s22p63s23p6.
Câu 14: Ở trạng thái cơ bản, nguyên tử của nguyên tố phosphorus (Z = 15) có số electron độc thân là
A. 1. B. 2. C. 3. D. 4.
Câu 15: Ở trạng thái cơ bản, cấu hình electron lớp ngoài cùng của nguyên tử X là 3s2. Số hiệu nguyên tử của nguyên tố X là
A. 12. B. 13. C. 11. D. 14.
Câu 16: Số hiệu nguyên tử của nguyên tố hoá học bằng
A. số thứ tự của nhóm.
B. số thứ tự của chu kì.
C. số thứ tự của ô nguyên tố.
D. số electron lớp ngoài cùng của nguyên tử.
Câu 17: Cấu hình electron của nguyên tử oxygen là 1s22s22p4. Vị trí của oxygen trong bảng tuần hoàn là
A. ô số 6, chu kì 2, nhóm VIA.
B. ô số 6, chu kì 3, nhóm VIB.
C. ô số 8, chu kì 2, nhóm VIB.
D. ô số 8, chu kì 2, nhóm VIA.
Câu 18: Nguyên tố aluminium (Al) có số hiệu nguyên tử là 13. Al thuộc khối nguyên tố
A.s. B.p. C.d. D.f.
Câu 19: Nguyên tử của nguyên tố nào sau đây có tính phi kim mạnh nhất?
A. Fluorine.
B. Bromine.
C. Phosphorus.
D. Iodine.
Câu 20: Phát biểu nào sau đây là đúng về xu hướng biến đổi tính kim loại trong bảng tuần hoàn các nguyên tố hóa học?
A. Tính kim loại của các nguyên tố tăng theo chiều từ trái sang phải trong một chu kì và từ trên xuống dưới trong một nhóm.
B. Tính kim loại giảm dần theo chiều từ trái sang phải trong một chu kì và tăng dần từ trên xuống dưới trong một nhóm.
C. Tính kim loại giảm dần theo chiều từ trái sang phải trong một chu kì và từ trên xuống dưới trong một nhóm.
D. Tính kim loại tăng dần theo chiều từ trái sang phải trong một chu kì và giảm dần từ trên xuống dưới trong một nhóm.
Câu 21: Độ âm điện là
A. đại lượng đặc trưng cho khả năng nhường electron của nguyên tử một nguyên tố khi tạo thành liên kết hóa học.
B. đại lượng đặc trưng cho khả năng tạo thành phân tử.
C. đại lượng đặc trưng cho khả năng tạo thành nguyên tử.
D. đại lượng đặc trưng cho khả năng hút electron của nguyên tử một nguyên tố khi tạo thành liên kết hóa học.
Câu 22: Sulfur là nguyên tố hóa học thuộc nhóm VIA của bảng tuần hoàn. Công thức oxide cao nhất của sulfur là
A. S2O6. B. SO3. C. SO6. D. SO2.
Câu 23: Oxide nào sau đây có tính base mạnh nhất?
A. MgO.
B. Cl2O7.
C. SO3.
D. Na2O.
Câu 24: Trong các chất dưới đây, chất nào có tính acid yếu nhất?
A. H3PO4.
B. H2SiO3.
C. H2SO4.
D. HClO4.
Câu 25: Các nguyên tố kim loại thuộc nhóm IA còn được gọi là
A. nhóm kim loại kiềm.
B. nhóm kim loại kiềm thổ.
C. nhóm halogen.
D. nhóm nguyên tố khí hiếm.
Câu 26: Nguyên tố M thuộc chu kì 3, nhóm VA của bảng tuần hoàn. Số hiệu nguyên tử của nguyên tố M là
A. 16. B. 14. C. 15. D. 13.
Câu 27: Cấu hình eletron lớp ngoài cùng của nguyên tố X là 3s1. Oxide cao nhất của X có tính chất nào sau đây?
A. Tính kim loại.
B. Tính phi kim.
C. Tính acid.
D. Tính base.
Câu 28: Sắp xếp tính base của NaOH, Mg(OH)2, Al(OH)3 theo chiều giảm dần là
A.NaOH, Mg(OH)2, Al(OH)3.
B.Al(OH)3, Mg(OH)2, NaOH.
C.Mg(OH)2, Al(OH)3, NaOH.
D.Mg(OH)2, NaOH, Al(OH)3.
Phần II: Tự luận (3 điểm)
Câu 1 (1 điểm): Hai nguyên tố A, B đứng kế tiếp nhau trong cùng một chu kì của bảng tuần hoàn và có tổng số đơn vị điện tích hạt nhân là 25. Xác định vị trí (ô, chu kì, nhóm) của hai nguyên tố A và B trong bảng tuần hoàn (có giải thích ngắn gọn cách xác định).
Câu 2 (1 điểm): Nguyên tử của nguyên tố X có tổng số hạt (proton, electron, neutron) là 40. Tổng số hạt mang điện nhiều hơn tổng số hạt không mang điện là 12.
Tính số hạt mỗi loại (proton, electron, neutron) trong nguyên tử X.
Câu 3 (1 điểm): Cho các nguyên tố sau: Li (Z = 3), O (Z = 8), F (Z = 9), Na (Z = 11).
Sắp xếp các nguyên tố trên theo chiều tăng dần bán kính nguyên tử, có giải thích ngắn gọn cách sắp xếp.
Hướng dẫn giải:
Phần I: Trắc nghiệm
|
1-D |
2-C |
3-A |
4-B |
5-C |
6-A |
7-D |
8-A |
9-A |
10-D |
|
11-D |
12-C |
13-C |
14-C |
15-A |
16-C |
17-D |
18-B |
19-A |
20-B |
|
21-D |
22-B |
23-D |
24-B |
25-B |
26-C |
27-D |
28-A |
Câu 1:
Đáp án đúng là: D
Hóa học nghiên cứu về thành phần, cấu trúc, tính chất, sự biến đổi của các chất và các hiện tượng kèm theo.
Câu 2:
Đáp án đúng là: C
Nguyên tử hydrogen này có:
Khối lượng hạt nhân = khối lượng hạt proton ≈ 1 amu
Khối lượng lớp vỏ = khối lượng hạt electron ≈ 0,00055 amu
⇒ Khối lượng hạt nhân nguyên tử lớn hơn khối lượng lớp vỏ là 10,00055 ≈ 1818 lần.
Phát biểu Asai vì:Khối lượng nguyên tử xấp xỉ 1 amu, là nguyên tử nhẹ nhất trong số các nguyên tử được biết cho đến nay.
Phát biểu B sai vì:Khối lượng nguyên tử xấp xỉ 1 amu.
Phát biểu D sai vì: Kích thước của hạt nhân rất nhỏ so với kích thước của nguyên tử.
Câu 3:
Đáp án đúng là: A
Nguyên tử gồm hạt nhân chứa proton, neutron và vỏ nguyên tử chứa electron.
Câu 4:
Đáp án đúng là: B
Số khối của hạt nhân nguyên tử X là: A = Z + N = 15 + 16 = 31.
Câu 5:
Đáp án đúng là: C
Các nguyên tử thuộc cùng một nguyên tử hóa học khi có cùng số đơn vị điện tích hạt nhân (Z) ⇒ Các nguyên tử A và C thuộc cùng một nguyên tố hóa học (đều có Z = 8).
Câu 6:
Đáp án đúng là: A
Nguyên tử nitrogen có số proton = số electron = 7.
Điện tích hạt nhân nguyên tử là: +7.
Câu 7:
Đáp án đúng là: D
Số hiệu nguyên tử (Z) = số proton = số electron = 11.
Số khối (A) = Z + N = 11 + 12 = 23.
Vậy kí hiệu của nguyên tử X là
Câu 8:
Đáp án đúng là: A
Gọi phần trăm số nguyên tử của đồng vị 7Li là x% ⇒ phần trăm số nguyên tử của đồng vị 6Li là (100 − x)%
Ta có: ¯ALi=7x+6(100−x)100=6,93⇒ x = 93
Phần trăm số nguyên tử của đồng vị 7Li là 93%.
Câu 9:
Đáp án đúng là: A
AO s là orbital có dạng hình cầu.
Câu 10:
Đáp án đúng là: D
Sự phân bố electron vào các lớp và phân lớp căn cứ vàomức năng lượng electron.
Câu 11:
Đáp án đúng là: D
Lớp M (n = 3) chứa số electron tối đa là: 2.32 =18 electron.
Câu 12:
Đáp án đúng là: C
Số thứ tự lớp và tên gọi là các chữ cái in hoa như bảng sau:
|
n |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
|
Tên lớp |
K |
L |
M |
N |
O |
P |
Q |
Câu 13:
Đáp án đúng là: C
Nguyên tử sulfur có Z = 16 nên nguyên tử có 16 electron.
⇒ Cấu hình electron là 1s22s22p63s23p4.
Câu 14:
Đáp án đúng là: C
Cấu hình electron nguyên tử P (Z = 15): 1s22s22p63s23p3.
Sự phân bố các electron vào AO:
Nguyên tử của nguyên tố phosphorus (Z = 15) có số electron độc thân là 3.
Câu 15:
Đáp án đúng là: A
Cấu hình electron của X là: 1s22s22p63s2.
Vậy số hiệu nguyên tử X = số electron = 12.
Câu 16:
Đáp án đúng là: C
Số hiệu nguyên tử của nguyên tố hoá học bằng số thứ tự của ô nguyên tố.
Câu 17:
Đáp án đúng là: D
Oxygen có 8 electron nên số hiệu nguyên tử là 8, oxygen ở ô số 8 trong bảng tuần hoàn.
Oxygen ở chu kì 2 (do có 2 lớp electron); nhóm VIA (do 6 electron hóa trị, nguyên tố p).
Câu 18:
Đáp án đúng là: B
Cấu hình electron nguyên tử của Al là: 1s22s22p63s23p1 ⇒ Al thuộc khối nguyên tố p.
Câu 19:
Đáp án đúng là: A
Trong bảng tuần hoàn, fluorine có độ âm điện lớn nhất nên có tính phi kim mạnh nhất.
Câu 20:
Đáp án đúng là: B
Tính kim loại giảm dần theo chiều từ trái sang phải trong một chu kì và tăng dần từ trên xuống dưới trong một nhóm.
Câu 21:
Đáp án đúng là: D
Độ âm điện là đại lượng đặc trưng cho khả năng hút electron của nguyên tử một nguyên tố khi tạo thành liên kết hóa học.
Câu 22:
Đáp án đúng là: B
Sulfur là nguyên tố nhóm VIA nên có hóa trị cao nhất trong hợp chất là VI.
Công thức oxide cao nhất của sulfur là SO3.
Câu 23:
Đáp án đúng là: D
Na, Cl, S, Mg đều thuộc chu kì 3 trong bảng tuần hoàn. Na thuộc nhóm IA (hay kim loại ở đầu chu kì 3) nên Na2O có tính base mạnh nhất trong số các oxide đề bài cho.
Câu 24:
Đáp án đúng là: B
|
Nhóm |
IVA |
VA |
VIA |
VIIA |
|
Nguyên tố |
Si |
P |
S |
Cl |
|
Công thức hydroxide |
H2SiO3 |
H3PO4 |
H2SO4 |
HClO4 |
Theo quy luật biến đổi tính chất trong một chu kì ta có acid H2SiO3 có tính acid yếu nhất.
Câu 25:
Đáp án đúng là: B
Các nguyên tố kim loại thuộc nhóm IA còn được gọi là nhóm kim loại kiềm.
Câu 26:
Đáp án đúng là: C
Nguyên tố M thuộc chu kì 3, nhóm VA.
Cấu hình electron của nguyên tố M là: 1s22s22p63s23p3
Vậy số hiệu nguyên tử của nguyên tố M là: Z = 15.
Câu 27:
Đáp án đúng là: D
Cấu hình eletron lớp ngoài cùng của nguyên tố X là 3s1 suy ra X ở nhóm IA trong bảng tuần hoàn.
Oxide cao nhất của X là Na2O, có tính base mạnh.
Câu 28:
Đáp án đúng là: A
Na, Mg, Al cùng thuộc chu kì 3 trong bảng tuần hoàn, theo chiều tăng dần của điện tích hạt nhân, tính base của hydroxide có xu hướng giảm dần theo thứ tự NaOH, Mg(OH)2, Al(OH)3.
Phần II: Tự luận
Câu 1:
a) Gọi số đơn vị điện tích hạt nhân nguyên tử của nguyên tố A là Z.
Hai nguyên tố A, B đứng kế tiếp nhau trong cùng một chu kì của bảng tuần hoàn nên số đơn vị điện tích hạt nhân của nguyên tố B là Z + 1.
Theo bài: Z + (Z + 1) = 25 ⇒ Z = 12
⇒ Nguyên tử A có 12 electron, nguyên tử B có 13 electron.
+ Cấu hình electron của A là 1s22s22p63s2.
Nguyên tố A thuộc ô số 12 (do Z = 12), chu kì 3 (do có 3 lớp electron), nhóm IIA (do 2 electron hóa trị, nguyên tố s).
+ Cấu hình electron của B là 1s22s22p63s23p1.
Nguyên tố B thuộc ô số 13 (do Z =13), chu kì 3 (do có 3 lớp electron), nhóm IIIA (do 3 electron hóa trị, nguyên tố p).
Câu 2:
Gọi số hạt proton, neutron và electron trong X lần lượt là P, N và E.
Nguyên tử trung hòa về điện nên P = E.
Theo bài ra ta có hệ phương trình:
Giải hệ phương trình được:
P = E = 13 và N = 14.
Câu 3:
Ta có:
+ Li, O, F cùng thuộc chu kì 2 trong bảng tuần hoàn. Trong một chu kì theo chiều tăng dần điện tích hạt nhân nguyên tử, bán kính nguyên tử giảm dần ⇒ bán kính nguyên tử:
F < O < Li (1)
+ Li và Na cùng thuộc nhóm IA. Trong một nhóm, theo chiều tăng dần điện tích hạt nhân nguyên tử, bán kính nguyên tử tăng dần ⇒ bán kính nguyên tử: Li < Na (2)
Vậy dãy gồm các nguyên tố được sắp xếp theo chiều tăng dần bán kính nguyên tử là:
F, O, Li, Na.
Đề thi Giữa học kì 1 Hóa học 10 Kết nối tri thức - Đề số 4
Phòng Giáo dục và Đào tạo ...
Đề thi Giữa kì 1 - Kết nối tri thức
Năm học 2022 - 2023
Môn: Hóa học lớp 10
Thời gian làm bài: phút
(không kể thời gian phát đề)
(Đề số 4)
Phần I: Trắc nghiệm (7 điểm)
Câu 1:Nội dung nào dưới đây không phải đối tượng nghiên cứu của hóa học?
A. Ứng dụng của chất.
B. Sự lớn lên và sinh sản của tế bào.
C. Thành phần, cấu trúc của chất.
D. Tính chất và sự biến đổi của chất.
Câu 2: Trong nguyên tử, hạt mang điện tích dương là
A. neutron và proton.
B. proton.
C. electron.
D. neutron.
Câu 3: Phát biểu nào dưới đây không đúng?
A. Khối lượng nguyên tử tập trung chủ yếu ở hạt nhân.
B. Hạt nhân của tất cả các nguyên tử đều có 2 loại hạt: proton và neutron.
C. Thí nghiệm bắn phá lá vàng của Rutherford cho thấy nguyên tử có cấu tạo rỗng.
D. Nguyên tử là trung hòa về điện.
Câu 4: Tổng số hạt proton, electron, neutron trong nguyên tử của nguyên tố A là 28, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 8. Nguyên tố A là
A. oxygen (Z = 8).
B. fluorine (Z = 9).
C. argon (Z = 18).
D. potassium (Z = 19).
Câu 5: Chọn phát biểu đúng khi nói về nguyên tử 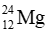
A. Mg có 12 electron.
B. Mg có 24 proton.
C. Mg có 24 electron.
D.Mg có 24 neutron.
Câu 6: Trong tự nhiên hydrogen có 3 đồng vị: 1H, 2H, 3H. Oxygen có 3 đồng vị 16O, 17O, 18O. Hỏi có bao nhiêu loại phân tử H2O được tạo thành từ các loại đồng vị trên?
A. 3. B. 16. C. 18. D. 9.
Câu 7: Nguyên tử khối trung bình của nguyên tố R là 35,5; biết R có 2 đồng vị, trong đó đồng vị 37R chiếm 25% số nguyên tử. Số khối của đồng vị thứ 2 là
A. 38. B. 35. C. 36. D. 34.
Câu 8: X và Y là đồng vị của cùng một nguyên tố hóa học. Phát biểu nào sau đây đúng?
A. X và Y có cùng số hạt neutron và khác số hạt proton.
B. X và Y có cùng số hạt electron và khác số hạt neutron.
C. X và Y có cùng số hạt proton và khác số hạt electron.
D. X và Y có cùng số hạt proton và khác số hạt neutron.
Câu 9: Số electron tối đa của lớp K là
A. 2. B. 18. C. 19. D. 8.
Câu 10: Phân lớp 3d có số electron tối đa là
A. 6. B. 18. C. 10. D. 14.
Câu 11:Nguyên tử sulfur (Z=16) có cấu hình electron nguyên tử là
A. 1s22s22p63s23p2.
B. 1s22s22p6.
C. 1s22s22p63s3 .
D. 1s22s22p63s23p4.
Câu 12: Cấu hình electron của nguyên tử nguyên tố X có tổng số electron ở các phân lớp p là 9. Số electron lớp ngoài cùng của X là
A. 4. B. 5. C. 3. D. 6.
Câu 13: Nguyên tố X có số hiệu nguyên tử là 17. Ở trạng thái cơ bản, X có số electron độc thân là
A. 1. B. 3. C. 2. D. 4.
Câu 14: Kí hiệu phân lớp nào sau đây là sai?
A. 2p. B. 3f. C. 3d. D. 4f.
Câu 15: Theo bảng tuần hoàn của Mendeleev, các nguyên tố được sắp xếp theo thứ tự tăng dần của
A.khối lượng nguyên tử.
B.cấu hình electron.
C.số hiệu nguyên tử.
D.số khối.
Câu 16: Các nguyên tố có cùng số lớp electron trong nguyên tử được xếp thành một hàng, gọi là
A.bảng tuần hoàn.
B.ô nguyên tố.
C.nhóm.
D.chu kì.
Câu 17: Nguyên tố magnesium (kí hiệu: Mg) có số hiệu nguyên tử là 12. Magnesium thuộc loại nguyên tố nào sau đây?
A.Nguyên tố s.
B.Nguyên tố p.
C.Nguyên tố d.
D.Nguyên tố f.
Câu 18: Biết nguyên tử nguyên tố X có 19 proton trong hạt nhân. Vị trí của X trong bảng tuần hoàn là
A.ô số 19, chu kì 4, nhóm IA.
B.ô số 19, chu kì 4, nhóm IB.
C.ô số 19, chu kì 3, nhóm IIIA.
D.ô số 19, chu kì 4, nhóm VB.
Câu 19: Trong bảng tuần hoàn các nguyên tố hóa học, nguyên tố có tính phi kim mạnh nhất là
A. oxygen.
B. fluorine.
C. iodine.
D. hydogen.
Câu 20: Đại lượng đặc trưng cho khả năng hút electron của một nguyên tử khi tạo thành liên kết hóa học là
A.năng lượng ion hóa.
B.điện tích hạt nhân.
C.bán kính nguyên tử.
D.độ âm điện.
Câu 21: Trong một chu kì, theo chiều tăng của điện tích hạt nhân nguyên tử
A. bán kính nguyên tử tăng, độ âm điện giảm.
B. bán kính nguyên tử giảm, độ âm điện tăng.
C. bán kính nguyên tử và độ âm điện đều giảm
D. bán kính nguyên tử và độ âm điện đều tăng.
Câu 22: Cho các nguyên tố sau: Be, Mg, Ca, Ba. Nguyên tử của nguyên tố có bán kính bé nhất là
A. Be. B. Mg. C. Ca. D. Ba.
Câu 23: Nguyên tử nguyên tố sulfur (S) có 16 proton. Công thức oxide cao nhất và tính chất của oxide đó là
A. SO2, basic oxide.
B. SO3, basic oxide.
C. SO2, acidic oxide.
C. SO3, acidic oxide.
Câu 24: X là nguyên tố nhóm A có công thức oxide cao nhất là XO3. Trong bảng tuần hoàn, X thuộc nhóm
A.IIIA. B.VA. C.IA. D.VIA.
Câu 25: Nguyên tố X thuộc chu kì 3 nhóm VIIA. Công thức hóa học của hydroxide (ứng với hóa trị cao nhất) của X là
A. H2XO3.
B. HX.
C. H2XO4.
D. HXO4.
Câu 26: Cho các nguyên tố sau: K (Z = 19), N (Z = 7), Si (Z = 14), Mg (Z = 12). Dãy gồm các nguyên tố được sắp xếp theo chiều giảm dần bán kính nguyên tử từ trái sang phải là
A. N, Si, Mg, K.
B. Mg, K, Si, N.
C. K, Mg, N, Si.
D. K, Mg, Si, N.
Câu 27: Nguyên tố Y ở chu kì 3, nhóm IA trong bảng tuần hoàn. Tính chất hóa học cơ bản của Y là
A. lưỡng tính.
B. khí hiếm.
C. phi kim.
D. kim loại.
Câu 28: Trong các chất dưới đây, chất nào có tính acid yếu nhất?
A. H3PO4.
B. H2SiO3.
C. H2SO4.
D. HClO4.
Phần II: Tự luận (3 điểm)
Câu 1 (1 điểm): Trong tự nhiên, đồng (copper) có hai đồng vị bền là 63Cu và 65Cu. Nguyên tử khối trung bình của đồng là 63,54. Tính số mol mỗi loại đồng vị có trong 6,354 gam đồng.
Câu 2 (1 điểm): Nguyên tố X và Y có số hiệu nguyên tử lần lượt là 12 và 18. Viết cấu hình electron, từ đó xác định vị trí của X, Y (số thứ tự của ô nguyên tố, chu kì và nhóm) trong bảng tuần hoàn, có giải thích ngắn gọn cách xác định.
Câu 3 (1 điểm): Chu kì 2 trong bảng tuần hoàn gồm các nguyên tố: Li, Be, B, C, N, O, F, Ne. Viết công thức các hydroxide (nếu có) của những nguyên tố chu kì 2. So sánh tính acid, tính base của chúng.
Xem thêm các đề thi giữa học kì 1 Hóa học 10 hay, chi tiết khác:
Đề thi Giữa học kì 1 Hóa học 10 Chân trời sáng tạo (Có đáp án)...
Đề thi Giữa học kì 1 Hóa học 10 Cánh diều (Có đáp án)...
Xem thêm các đề thi Học kì 1 Hóa học 10 hay, chi tiết khác:
Đề thi Học kì 1 Hóa học 10 Kết nối tri thức (Có đáp án)...
Đề thi Học kì 1 Hóa học 10 Chân trời sáng tạo (Có đáp án)...
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.