Toptailieu.vn xin giới thiệu 15 câu trắc nghiệm Liên kết hydrogen và tương tác van der waals Chân trời sáng tạo (có đáp án 2023) CHỌN LỌC, hay nhất giúp học sinh lớp 10 ôn luyện kiến thức để đạt kết quả cao trong các bài thi môn Hóa học.
Mời các bạn đón xem:
15 câu trắc nghiệm Liên kết hydrogen và tương tác van der waals Chân trời sáng tạo (có đáp án 2023) CHỌN LỌC
Lý thuyết
I. Liên kết hydrogen
1. Tìm hiểu về liên kết hydrogen
- Liên kết hydrogen là một loại liên kết yếu, được hình thành giữa nguyên tử H (đã liên kết với một nguyên tử có độ âm điện lớn, thường là F, O, N) với một nguyên tử khác có độ âm điện lớn (thường là F, O, N) còn cặp electron hóa trị chưa tham gia liên kết
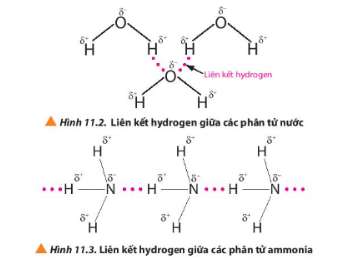
- Điều kiện cần và đủ để tạo thành liên kết hydrogen:
+ Nguyên tử hydrogen liên kết với các nguyên tử có độ âm điện lớn như F, O, N,…
+ Nguyên tử F, O, N,… liên kết với hydrogen phải có ít nhất một cặp electron hóa trị chưa liên kết
2. Tìm hiểu vai trò, ảnh hưởng của liên kết hydrogen tới tính chất vật lí của nước
- Liên kết hydrogen làm tăng nhiệt độ nóng chảy, nhiệt độ sôi của nước
II. Tương tác van der Waals
1. Giới thiệu về tương tác van der Waals (van đơ Van)
- Tương tác van der Waals là tương tác tĩnh điện lưỡng cực – lưỡng cực giữa các nguyên tử hay phân tử
- Bản chất:
+ Trong phân tử, các electron không ngừng chuyển động. Khi các electron di chuyển tập trung về một phía bất kì của phân tử sẽ hình thành nên các lưỡng cực tạm thời:
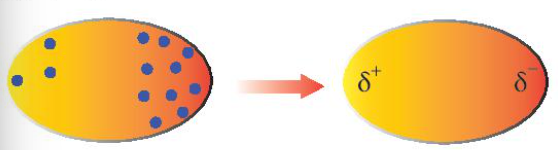
+ Các phân tử có lưỡng cực tạm thời cũng có thể làm các phần tử lân cận xuất hiện các lưỡng cực cảm ứng. Do đó, các phân tử có thể tập hợp thành một mạng lưới với tương tác lưỡng cực cảm ứng, được gọi là tương tác van der Waals
2. Ảnh hưởng của tương tác van der Waals đến nhiệt độ nóng chảy, nhiệt độ sôi của các chất
- Tương tác van der Waals tăng theo sự tăng của số electron trong phân tử. Làm tăng nhiệt độ nóng chảy, nhiệt độ sôi của các chất
Bài tập
Câu 1. Các tính chất vật lý của các chất có liên kết cộng hóa trị được quyết định bởi các yếu tố nào?
A. Lực tương tác giữa các phân tử;
B. Hình dạng của phân tử;
C. Mức độ phân cực của liên kết cộng hóa trị trong phân tử;
D. Cả A, B, C đều đúng.
Đáp án: D
Các tính chất vật lý của các chất có liên kết cộng hóa trị được quyết định bởi lực tương tác giữa các phân tử, hình dạng của phân tử và mức độ phân cực của liên kết cộng hóa trị trong phân tử.
Câu 2. Liên kết hydrogen được hình thành như thế nào?
A. Giữa nguyên tử H (đã liên kết với một nguyên tử có độ âm điện lớn) với một nguyên tử khác (có độ âm điện lớn) còn cặp electron hóa trị chưa tham gia vào liên kết;
B. Giữa nguyên tử H (đã liên kết với một nguyên tử có độ âm điện lớn) với một nguyên tử khác (có độ âm điện lớn);
C. Giữa nguyên tử H và nguyên tử O;
D. Giữa nguyên tử H và các phi kim.
Đáp án: A
Liên kết hydrogen được hình thành giữa nguyên tử H (đã liên kết với một nguyên tử có độ âm điện lớn) với một nguyên tử khác (có độ âm điện lớn) còn cặp electron hóa trị chưa tham gia vào liên kết.
Câu 3. Liên kết hydrogen có tính chất nào sau đây?
A. Không bền bằng liên kết ion;
B. Không bền bằng liên kết cộng hóa trị;
C. Không bền bằng liên kết cho – nhận;
D. Tất cả các tính chất A, B, C đều đúng.
Đáp án: D
Lực tương tác giữa các phân tử yếu hơn rất nhiều so với lực liên kết ion, liên kết cộng hóa trị hay liên kết kim loại.
Câu 4. Nguyên nhân làm cho các liên kết phân cực là?
A. Sự chênh lệch độ âm điện lớn;
B. Sự chênh lệch năng lượng liên kết;
C. Do liên kết hidro trong phân tử;
D. Do bán kính của nguyên tử.
Đáp án: A
Sự chênh lệch độ âm điện lớn làm cho các liên kết phân cực, cặp electron dùng chung trong liên kết cộng hóa trị bị hút lệch về phía các nguyên tử có độ âm điện lớn hơn.
Câu 5. Liên kết hydrogen có thể xuất hiện giữa những phân tử cùng loại nào sau đây?
A. C2H6
B. H2S
C. H3C-O-CH3
D. NH3
Đáp án: D
A. Loại vì C-H là liên kết cộng hóa trị không phân cực, nguyên tử C không còn electron hóa trị riêng.
B. Loại vì S-H là liên kết cộng hóa trị không phân cực.
C. Loại vì trong phân tử H3C-O-CH3 nguyên tử C và O đều không có cặp electron hóa trị riêng.
D. Chọn vì liên kết N-H phân cực. Liên kết hydrogen giữa hai phân tử NH3 được biểu diễn như sau:
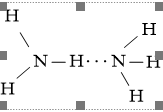
Câu 6. Số phát biểu sai về sự tạo thành liên kết hydrogen?
(1) Nguyên tử hydrogen liên kết với các nguyên tử có độ âm điện lớn như F, O, N,…;
(2) Nguyên tử liên kết với hydrogen phải có ít nhất một cặp electron hóa trị chưa liên kết;
(3) Nguyên tử hydrogen liên kết với các nguyên tử thuộc nhóm kim loại kiềm và kiềm thổ;
(4) Nguyên tử liên kết với hydrogen phải có cấu hình electron bền vững.
A. 1;
B. 2;
C. 3;
D. 4.
Đáp án: B
Phát biểu sai: (3), (4).
Câu 7. Liên kết hydrogen có ảnh hưởng như thế nào tới tính chất vật lý của nước?
A. Không có ảnh hưởng gì;
B. Làm tăng nhiệt độ nóng chảy;
C. Làm tăng nhiệt độ sôi;
D. Cả B và C đều đúng
Đáp án: D
Liên kết hydrogen làm tăng nhiệt độ nóng chảy và nhiệt độ sôi của nước.
Câu 8. Tương tác van der Waals là gì?
A. Là tương tác tĩnh điện giữa các phân tử;
B. Là tương tác tĩnh điện lưỡng cực - lưỡng cực các nguyên tử hay phân tử;
C. Là tương tác giữa các electron trong phân tử;
D. Là tương tác giữa các electron hóa trị trong phân tử.
Đáp án: B
Tương tác van der Waals là tương tác tĩnh điện lưỡng cực - lưỡng cực các nguyên tử hay phân tử.
Câu 9. Tương tác van der Waal có ảnh hưởng gì đến nhiệt độ nóng chảy và nhiệt độ sôi của các chất?
A. Không có ảnh hưởng gì;
B. Làm tăng nhiệt độ nóng chảy;
C. Làm tăng nhiệt độ sôi;
D. Cả B và C đều đúng
Đáp án: D
Tương tác van der Waal làm tăng nhiệt độ nóng chảy và nhiệt độ sôi của các chất.
Câu 10. Khi khối lượng phân tử tăng thì tương tác van der Waals như thế nào?
A. Giảm;
B. Tăng;
C. Tăng rồi giảm;
D. Giảm rồi tăng.
Đáp án: B
Khi khối lượng phân tử tăng thì tương tác van der Waals tăng.
Câu 11. Tại sao ở nhiệt độ phòng fluorine, chlorine là những chất khí, còn bromine là chất lỏng?
A. Do giữa các phân tử bromine có tương tác van der Waals;
B. Do độ âm điện của bromine thấp hơn fluorine, chlorine;
C. Do năng lượng liên kết của bromine lớn hơn fluorine, chlorine;
D. Do bán kính nguyên tử bromine lớn hơn fluorine, chlorine.
Đáp án: A
Cùng là phân tử không phân cực, ở nhiệt độ phòng, fluorine, chlorine là những chất khí, còn bromine là chất lỏng. Như vậy, ở trạng thái lỏng, các phân tử bromine tồn tại một tương tác yếu. Tương tác yếu đó gọi là tương tác van der Waals.
Câu 12. Nhiệt độ nóng chảy của các phân tử trong dãy halogen được sắp xếp theo thứ tự tăng dần là?
A. Cl2, Br2, F2, I2;
B. I2, Br2, Cl2, F2;
C. F2, Cl2, Br2, I2;
D. F2, Br2, Cl2, I2-.
Đáp án: C
Trong dãy halogen, tương tác van der Waals tăng theo sự tăng của số electron và proton trong phân tử, làm tăng nhiệt độ nóng chảy của các chất.
Câu 13. Liên kết hydrogen thường được biểu diễn như thế nào?
A. Biểu diễn bằng dấu ba chấm giữa các nguyên tử;
B. Biểu diễn bằng liên kết đôi giữa các nguyên tử;
C. Biểu diễn bằng liên kết ba giữa các nguyên tử;
D. Biểu diễn bằng mũi tên giữa các nguyên tử.
Đáp án: A
Liên kết hydrogen thường được biểu diễn bằng dấu ba chấm giữa các nguyên tử.
Câu 14. Nhiệt độ sôi của H2O cao hơn nhiều so với H2S và CH4 vì?
A. Nhiệt độ nóng chảy cao làm cho nhiệt độ sôi cao.
B. Liên kết O-H phân cực hơn liên kết S-H và C-H nên phân tử H2O khó bị phá vỡ hơn.
C. H2O là dung môi hòa tan được nhiều chất.
D. Giữa các phân tử nước có liên kết hydrogen còn H2S và CH4 thì không.
Đáp án: D
Giữa các phân tử nước có liên kết hydrogen còn H2S và CH4 thì không.
Liên kết hydrogen làm tăng nhiệt độ nóng chảy và nhiệt độ sôi của nước.
Câu 15. Tại sao khi chưng cất rượu, C2H5OH bay hơi trước H2O mà C2H5OH có khối lượng phân tử lớn hơn H2O?
A. Các phân tử nước liên kết chặt chẽ với nhau bằng liên kết hydrogen;
B. Nhiệt độ sôi của H2O cao hơn C2H5OH;
C. Khi chưng cất, C2H5OH ở điểm sôi thấp hơn nên bay hơi trước;
D. Cả A, B, C đều đúng.
Đáp án: D
Mặc dù C2H5OH có khối lượng phân tử lớn hơn H2O nhưng các phân tử nước liên kết chặt chẽ với nhau bằng liên kết hydrogen
Nhiệt độ sôi của H2O cao hơn C2H5OH.
Khi chưng cất, C2H5OH ở điểm sôi thấp hơn nên bay hơi trước.
Xem thêm các bài giải Trắc nghiệm Hóa lớp 10 Chân trời sáng tạo hay, chi tiết khác:
Bài 12: Phản ứng oxi hóa khử và ứng dụng trong cuộc sống
Bài 13: Enthalpy tạo thành và biến thiên enthalpy của phản ứng hóa học
Bài 14: Tính biến thiên enthalpy của phản ứng hóa học
Bài 15: Phương trình tốc độ phản ứng và hằng số tốc độ phản ứng
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.