Với giải Hoá học 11 trang 9 (Kết nối tri thức) chi tiết trong Bài 1: Khái niệm về cân bằng hoá học giúp học sinh dễ dàng xem và so sánh lời giải, từ đó biết cách làm bài tập Hoá học 11. Mời các bạn đón xem:
Hoá học 11 trang 9 (Kết nối tri thức)
Câu hỏi 4 trang 9 Hóa học 11: Cho phản ứng: 2HI(g) ⇌ H2(g) + I2(g)
a) Vẽ dạng đồ thị biểu diễn tốc độ của phản ứng thuận và phản ứng nghịch theo thời gian.
b) Xác định trên đồ thị thời điểm phản ứng trên bắt đầu đạt đến trạng thái cân bằng.
Lời giải:
a) Dạng đồ thị biểu diễn tốc độ của phản ứng thuận và phản ứng nghịch theo thời gian:
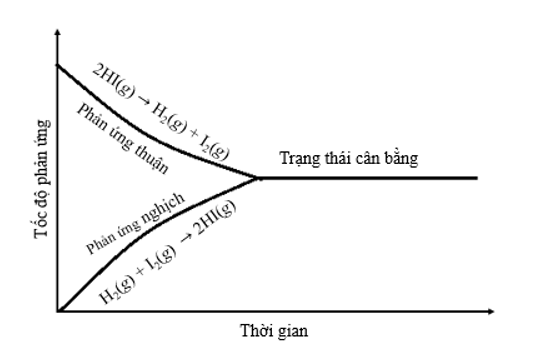
b) Tại thời điểm số mol của các chất hydrogen, iodine, hydrogen iodide không thay đổi nữa thì phản ứng đạt trạng thái cân bằng.
Câu hỏi 5 trang 9 Hóa học 11: Cho các nhận xét sau:
a) Ở trạng thái cân bằng, tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch.
b) Ở trạng thái cân bằng, các chất không phản ứng với nhau.
c) Ở trạng thái cân bằng, nồng độ các chất sản phẩm luôn lớn hơn nồng độ các chất đầu.
d) Ở trạng thái cân bằng, nồng độ các chất không thay đổi.
Lời giải:
Đáp án đúng là: D
- Trạng thái cân bằng của phản ứng thuận nghịch là trạng thái tại đó tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch.
- Ở trạng thái cân bằng, nồng độ các chất không thay đổi.
Câu hỏi 5 trang 9 Hóa học 11: Cho các nhận xét sau:
a) Ở trạng thái cân bằng, tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch.
b) Ở trạng thái cân bằng, các chất không phản ứng với nhau.
c) Ở trạng thái cân bằng, nồng độ các chất sản phẩm luôn lớn hơn nồng độ các chất đầu.
d) Ở trạng thái cân bằng, nồng độ các chất không thay đổi.
Các nhận xét đúng là
A. (a) và (b).
B. (b) và (c).
C. (a) và (c).
D. (a) và (d).
Lời giải:
Đáp án đúng là: D
- Trạng thái cân bằng của phản ứng thuận nghịch là trạng thái tại đó tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch.
- Ở trạng thái cân bằng, nồng độ các chất không thay đổi.
Hoạt động trang 9 Hóa học 11: Xét phản ứng thuận nghịch: H2(g) + I2(g) ⇌ 2HI(g)
Thực hiện phản ứng trên ở trong bình kín, ở nhiệt độ 445 oC với các nồng độ ban đầu khác nhau. Số liệu về nồng độ các chất ở thời điểm ban đầu và trạng thái cân bằng trong các thí nghiệm được trình bày trong Bảng 1.2.
Bảng 1.2. Nồng độ các chất của phản ứng H2(g) + I2(g) ⇌ 2HI(g) ở thời điểm ban đầu và ở trạng thái cân bằng.
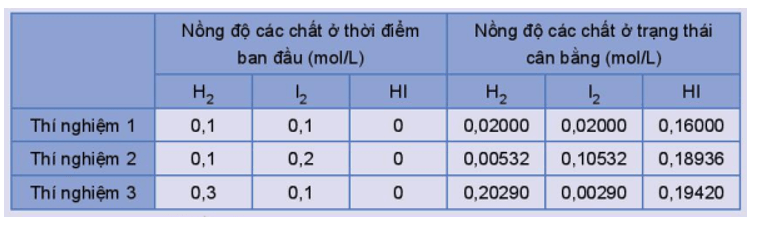
Tính giá trị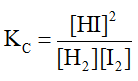
Lời giải:
Giá trị hằng số cân bằng ở mỗi thí nghiệm:
- Thí nghiệm 1:
- Thí nghiệm 2: 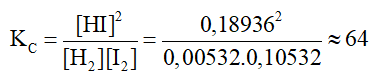
- Thí nghiệm 3: 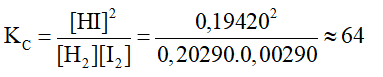
Nhận xét: Hằng số cân bằng KC của một phản ứng thuận nghịch chỉ phụ thuộc vào nhiệt độ và bản chất của phản ứng.
Xem thêm các bài giải Hoá học 11 Kết nối tri thức hay, chi tiết khác:
Hoá học 11 trang 6 ( Kết nối tri thức )
Hoá học 11 trang 8 ( Kết nối tri thức )
Hoá học 11 trang 10 ( Kết nối tri thức )
Hoá học 11 trang 13 ( Kết nối tri thức )
Hoá học 11 trang 14 ( Kết nối tri thức )
Xem thêm các bài giải Hoá học 11 Kết nối tri thức hay, chi tiết khác:
Mở đầu trang 6 Hóa học 11: Phản ứng hoá học là quá trình biến đổi các chất đầu thành sản phẩm....
Hoạt động trang 6 Hóa học 11: Hai thí nghiệm sau đều được thực hiện ở cùng một điều kiện...
Câu hỏi 2 trang 8 Hóa học 11: Phản ứng xảy ra khi cho khí Cl2 tác dụng với nước là một phản ứng....
Câu hỏi 3 trang 8 Hóa học 11: Nhận xét nào sau đây không đúng?
Hoạt động trang 8 Hóa học 11: Xét phản ứng thuận nghịch: H2(g) + I2(g) ⇌ 2HI(g).
Câu hỏi 4 trang 9 Hóa học 11: Cho phản ứng: 2HI(g) ⇌ H2(g) + I2(g)
Câu hỏi 5 trang 9 Hóa học 11: Cho các nhận xét sau:
Câu hỏi 5 trang 9 Hóa học 11: Cho các nhận xét sau:
Hoạt động trang 9 Hóa học 11: Xét phản ứng thuận nghịch: H2(g) + I2(g) ⇌ 2HI(g)
Câu hỏi 6 trang 10 Hóa học 11: Viết biểu thức hằng số cân bằng cho các phản ứng sau:
Câu hỏi 7 trang 10 Hóa học 11: Ammonia (NH3) được điều chế bằng phản ứng: N2(g) + 3H2(g) ⇌ 2NH3(g)
Thí nghiệm 1 trang 10 Hóa học 11: Ảnh hưởng của nhiệt độ đến sự chuyển dịch cân bằng:
Câu hỏi 8 trang 13 Hóa học 11: Cho các cân bằng sau:
Câu hỏi 9 trang 13 Hóa học 11: Ester là hợp chất hữu cơ dễ bay hơi, một số ester được...
Câu hỏi 10 trang 14 Hóa học 11: Cho các cân bằng sau:
Câu hỏi 11 trang 14 Hóa học 11: Trong công nghiệp, khí hydrogen được điều chế như sau:
Câu hỏi 12 trang 14 Hóa học 11: Trong cơ thể người, hemoglobin (Hb) kết hợp với oxygen...
Xem thêm các bài giải Hoá học 11 Kết nối tri thức hay, chi tiết khác:
Hoá học 11 (Kết nối tri thức) Bài 2: Cân bằng trong dung dịch nước
Hoá học 11 ( Kết nối tri thức ) Bài 3: Ôn tập chương 1
Hoá học 11 (Kết nối tri thức) Bài 4: Nitrogen
Hoá học 11 (Kết nối tri thức) Bài 5: Ammonia. Muối ammonium
Hoá học 11 (Kết nối tri thức) Bài 6: Một số hợp chất của nitrogen với oxygen
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.