Với giải Hoạt động trang 35 Hóa học 11 Kết nối tri thức chi tiết trong Bài 5: Ammonia. Muối ammonium giúp học sinh dễ dàng xem và so sánh lời giải, từ đó biết cách làm bài tập Hoá học 11. Mời các bạn đón xem:
Vận dụng kiến thức về cân bằng hoá học, tốc độ phản ứng, biến thiên enthalpy
Hoạt động trang 35 Hóa học 11: Vận dụng kiến thức về cân bằng hoá học, tốc độ phản ứng, biến thiên enthalpy để giải thích các điều kiện của phản ứng sản xuất ammonia, cụ thể:
1. Nếu tăng hoặc giảm nhiệt độ sẽ ảnh hưởng đến sự chuyển dịch cân bằng và tốc độ phản ứng như thế nào?
2. Nếu giảm áp suất, cân bằng chuyển dịch theo chiều nào? Tại sao không thực hiện ở áp suất cao hơn?
3. Vai trò của chất xúc tác trong phản ứng là gì?
Lời giải:
Trong công nghiệp, quá trình sản xuất ammonia thường được thực hiện ở nhiệt độ 400 oC – 450 oC,áp suất 150 – 200 bar, xúc tác Fe.
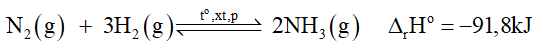
1) Vì DrHo = -91,8 kJ < 0 nên phản ứng thuận toả nhiệt. Vậy:
+ Nếu tăng nhiệt độ, cân bằng chuyển dịch theo chiều nghịch (tức chiều phản ứng thu nhiệt) làm giảm hiệu suất phản ứng.
+ Nếu giảm nhiệt độ, cân bằng chuyển dịch theo chiều thuận (tức chiều phản ứng toả nhiệt) làm tăng hiệu suất phản ứng.
Tuy nhiên, khi thực hiện phản ứng ở nhiệt độ quá thấp thì tốc độ của phản ứng nhỏ, phản ứng diễn ra chậm. Thực tế, người ta đã chọn nhiệt độ phù hợp, khoảng 400 oC - 450 oC.
2. Khi giảm áp suất, cân bằng chuyển dịch theo chiều làm tăng áp suất của hệ - tức chiều làm tăng số mol khí, hay chiều nghịch.
Quá trình sản xuất NH3 được thực hiện ở áp suất 150 – 200 bar mà không thực hiện ở áp suất cao hơn. Điều này được giải thích như sau: Khi thực hiện ở áp suất cao sẽ thu
được nồng độ NH3 tại thời điểm cân bằng lớn, tuy nhiên khi tăng áp suất thì
sự tăng nồng độ NH3 không tăng nhanh chỉ tăng chậm. Ngoài ra, khi tăng áp suất thì
tiêu tốn năng lượng và yêu cầu thiết bị phải chịu được áp suất cao, do đó phải
tính toán chính xác khi tăng áp suất để mang lại hiệu quả kinh tế cao nhất. Thực tế chứng minh quá trình sản xuất NH3 được thực hiện ở áp suất 150 – 200 bar đem lại hiệu quả cao nhất.
3. Việc sử dụng chất xúc tác là bột sắt có tác dụng làm cho phản ứng nhanh đạt tới trạng thái cân bằng.
Xem thêm các bài giải Hoá học 11 Kết nối tri thức hay, chi tiết khác:
Mở đầu trang 33 Hóa học 11: Từ ammonia, thông qua phản ứng nào có thể sản xuất...
Hoạt động 1 trang 33 Hóa học 11: Viết cấu hình electron của các nguyên tử H (Z = 1) và N (Z = 7).
Hoạt động 2 trang 33 Hóa học 11: Trình bày các bước lập công thức Lewis của phân tử ammonia.
Câu hỏi 1 trang 34 Hóa học 11: Từ đặc điểm cấu tạo của phân tử ammonia, hãy giải thích...
Câu hỏi 2 trang 34 Hóa học 11: Hãy giải thích tại sao ammonia tan tốt trong nước
Hoạt động trang 34 Hóa học 11: Trong công nghiệp, phản ứng giữa ammonia với acid...
Câu hỏi 3 trang 34 Hóa học 11: Trong hai phản ứng oxi hoá ammonia bằng oxygen ở trên, hãy:
Hoạt động trang 35 Hóa học 11: Sưu tầm một số hình ảnh để báo cáo, thuyết trình về...
Hoạt động trang 35 Hóa học 11: Vận dụng kiến thức về cân bằng hoá học,...
Thí nghiệm trang 36 Hóa học 11: Nhận biết ion ammonium trong phân đạm
Câu hỏi 4 trang 37 Hóa học 11: a) So sánh phân tử ammonia và ion ammonium về dạng hình học...
Em có thể trang 37 Hóa học 11: - Vận dụng được kiến thức về cân bằng hoá học, tốc độ phản ứng....
Xem thêm các bài giải Hoá học 11 Kết nối tri thức hay, chi tiết khác:
Hoá học 11 ( Kết nối tri thức ) Bài 3: Ôn tập chương 1
Hoá học 11 (Kết nối tri thức) Bài 4: Nitrogen
Hoá học 11 (Kết nối tri thức) Bài 6: Một số hợp chất của nitrogen với oxygen
Hoá học 11 (Kết nối tri thức) Bài 7: Sulfur và sulfur dioxide
Hoá học 11 (Kết nối tri thức) Bài 8: Sulfuric acid và muối sulfate
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.