Toptailieu.vn biên soạn và giới thiệu lời giải Hoá học 11 (Chân trời sáng tạo) Bài 19: Carboxylic acid hay, chi tiết sẽ giúp học sinh dễ dàng trả lời câu SGK Hóa học 11 Bài 19 từ đó học tốt môn Hóa học 11.
Hoá học 11 (Chân trời sáng tạo) Bài 19: Carboxylic acid
Lời giải:
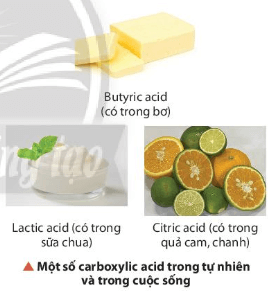
- Carboxylic acid là hợp chất hữu cơ mà phân tử có nhóm carboxyl (- COOH) liên kết trực tiếp với nguyên tử carbon (của gốc hydrocarbon hoặc của nhóm – COOH khác) hoặc của nguyên tử hydrogen.
- Tính chất đặc trưng của carboxylic acid:
+ Làm đổi màu giấy quỳ tím thành đỏ;
+ Phản ứng với một số kim loại, oxide base, base, muối, …
+ Phản ứng với alcohol tạo ester.
1. Khái niệm - cấu trúc - danh pháp
Lời giải:
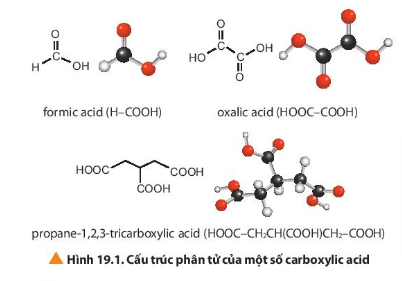
- Đặc điểm chung về cấu tạo của carboxylic acid: phân tử có nhóm – COOH. Nhóm – COOH gồm nhóm hydroxy (- OH) liên kết với nhóm carbonyl.
- Điểm khác về cấu tạo của carboxylic acid so với cấu tạo của aldehyde và ketone: có thêm nhóm hydroxy (- OH).
Lời giải:
Công thức cấu tạo của các carboxylic acid đơn chức có công thức phân tử C4H8O2:
CH3 – CH2 – CH2 – COOH;
Lời giải:
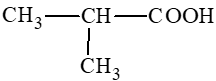
Các hợp chất carboxylic acid là: CH2 = CH – COOH (3), HOOC – COOH (4).
Lời giải:
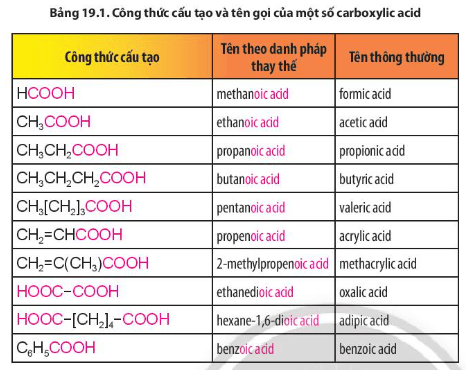
Tên theo danh pháp thay thế của carboxylic acid đơn chức, mạch hở:
Số chỉ vị trí nhánh + tên nhánh + tên hydrocarbon ứng với mạch chính (bỏ kí tự e ở cuối) + oic + acid.
Nếu carboxylic acid đa chức, mạch hở:
Số chỉ vị trí nhánh + tên nhánh + tên hydrocarbon ứng với mạch chính + số chỉ vị trí các nhóm COOH + tiền tố (di, tri, …) + oic + acid.
Luyện tập 1 trang 126 Hóa học 11: Gọi tên theo danh pháp thay thế của các carboxylic sau:
a) (CH3)2CH – COOH.
b) (CH3)3C – COOH.
c) CH3CH=CH-COOH.
d) CH3CH=C(CH3) – COOH.
Lời giải:
a) (CH3)2CH – COOH: 2 – methylpropanoic acid.
b) (CH3)3C – COOH: 2,2 – dimethylpropanoic acid.
c) CH3CH=CH-COOH: but – 2 – enoic acid.
d) CH3CH=C(CH3) – COOH: 2 – methylbut – 2 – enoic acid.
Luyện tập 2 trang 126 Hóa học 11: Viết công thức cấu tạo của các carboxylic acid có tên sau:
a) Propanoic acid.
b) Pent – 3 – enoic acid.
Lời giải:
a) Propanoic acid: CH3 – CH2 – COOH.
b) Pent – 3 – enoic acid: CH3 – CH = CH – CH2 – COOH.
Lời giải:
Công thức cấu tạo các đồng phân acid có công thức phân tử C5H10O2:
CH3 – CH2 – CH2 – CH2 – COOH: pentanoic acid;
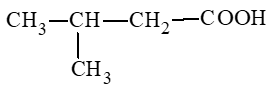 : 3 – methylbutanoic acid;
: 3 – methylbutanoic acid;
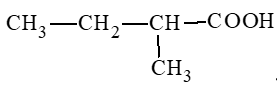 : 2 – methylbutanoic acid;
: 2 – methylbutanoic acid;
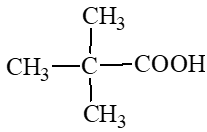 : 2,2 – dimethylpropanoic acid.
: 2,2 – dimethylpropanoic acid.
2. Tính chất vật lí
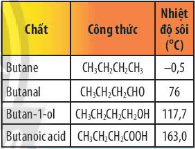
Lời giải:
Nhiệt độ sôi: butanoic acid > butan – 1 – ol > butanal > butane.
Giải thích:
+ Butanoic acid có nhiệt độ sôi cao nhất trong dãy do butanoic acid có khả năng tạo thành liên kết hydrogen bền vững hơn liên kết hydrogen trong phân tử butan – 1 – ol.
+ Butanal và butane không có liên kết hydrogen nhưng butanal phân cực nên có nhiệt độ sôi cao hơn butane.
Câu hỏi thảo luận 4 trang 127 Hóa học 11: Vì sao acetic acid tan vô hạn trong nước?
Lời giải:
Nhờ khả năng tạo liên kết hydrogen với nước nên acetic acid tan vô hạn trong nước.
(1) C3H8.
(2) C2H5COOH.
(3) C2H5CHO.
(4) C3H7OH.
Lời giải:
Chiều nhiệt độ sôi tăng dần: (1) C3H8 < (3) C2H5CHO < (4) C3H7OH < (2) C2H5COOH.
Giải thích:
+ C3H8 có nhiệt độ sôi thấp nhất do phân tử không phân cực; Tiếp theo là C2H5CHO do chất này phân cực nhưng không tạo được liên kết hydrogen liên phân tử.
+ C2H5COOH có nhiệt độ sôi cao nhất do liên kết hydrogen liên phân tử của chất này bền hơn liên kết hydrogen liên phân tử của C3H7OH.
3. Tính chất hóa học
Lời giải:
Nhóm carbonyl (>C = O) hút electron nên liên kết O – H trong carboxylic acid phân cực hơn so với alcohol, phenol.
Dự đoán tính chất hoá học đặc trưng của hợp chất carboxyl acid là tính acid.
Ka =
Dựa vào Bảng 19.3, nhận xét về tính acid của carboxylic acid. Nêu tính chất hoá học đặc trưng của chúng.
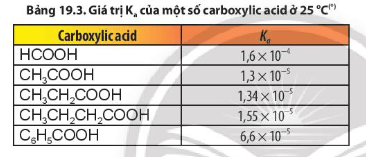
Lời giải:
Carboxylic acid có tính acid yếu. Cụ thể:
+ Làm đổi màu giấy quỳ tím thành màu đỏ;
+ Phản ứng được với các kim loại đứng trước hydrogen trong dãy hoạt động hoá học, giải phóng khí hydrogen.
+ Tác dụng được với oxide base, base.
+ Tác dụng được với một số muối…
Lời giải:
Hiện tượng:
+ Giấy quỳ tím chuyển sang màu đỏ, do trong dung dịch nước carboxylic acid phân li theo cân bằng: RCOOH ⇌ RCOO- + H+.
+ Ở ống nghiệm (1) mẩu Mg tan dần, có khí thoát ra, do CH3COOH tác dụng được với Mg, giải phóng H2. Phương trình hoá học:
2CH3COOH + 2Mg → (CH3COO)2Mg + H2↑.
+ Ở ống nghiệm (2), sodium carbonate tan dần, có khí thoát ra, do sodium carbonate tác dụng được với CH3COOH, giải phóng khí CO2. Phương trình hoá học:
2CH3COOH + Na2CO3 → 2CH3COONa + CO2↑ + H2O.
Lời giải:
Sử dụng giấm ăn, hoặc nước chanh….để làm sạch lớp cặn trong các dụng cụ đun và chứa nước nóng.
Do lớp cặn này có thành phần chính là MgCO3; CaCO3 có thể tác dụng được với các carboxylic acid có trong giấm ăn hoặc chanh … tạo thành muối tan, do đó lớp cặn được rửa trôi.
Luyện tập 1 trang 129 Hóa học 11: Hoàn thành các phương trình hoá học của các phản ứng sau:
a) (CH3)2CHCOOH + Ca →
b) HOOC – COOH + NaOH →
c) HCOOH + Na2CO3 →
d) C2H5COOH + CuO →
Lời giải:
a) 2(CH3)2CHCOOH + Ca → [(CH3)2CHCOO]2Ca + H2↑
b) HOOC – COOH + 2NaOH → NaOOC – COONa + 2H2O
c) 2HCOOH + Na2CO3 → 2HCOONa + CO2↑ + H2O
d) 2C2H5COOH + CuO → (C2H5COO)2Cu + H2O.
Lời giải:
Trích mẫu thử.
Cho lần lượt vào mỗi mẫu thử một mẩu giấy quỳ tím.
+ Giấy quỳ tím chuyển sang màu đỏ → mẫu thử là acetic acid và acrylic acid (nhóm I);
+ Giấy quỳ tím không đổi màu → mẫu thử là ethanol và acetaldehyde (nhóm II).
Phân biệt nhóm I: Dùng dung dịch bromine
+ Dung dịch bromine nhạt dần đến mất màu → mẫu thử là acrylic acid.
CH2 = CH – COOH + Br2 → CH2Br – CHBr – COOH.
+ Dung dịch bromine không bị mất màu → mẫu thử là acetic acid.
Phân biệt nhóm II: Dùng dung dịch bromine
+ Dung dịch bromine nhạt dần đến mất màu → mẫu thử là acetaldehyde
CH3CHO + Br2 + H2O → CH3COOH + 2HBr.
+ Dung dịch bromine không bị mất màu → mẫu thử là ethanol.
Dấu hiệu nào giúp nhận biết có sản phẩm mới được tạo thành? Giải thích.
Lời giải:
Hiện tượng: Phản ứng sinh ra chất lỏng, nhẹ hơn nước, có mùi thơm đặc trưng.
Dấu hiệu nhận ra có sản phẩm mới tạo thành: sản phẩm có chất lỏng, nhẹ hơn nước, mùi thơm đặc trưng.
Giải thích bằng phương trình hoá học:
CH3COOH + C2H5OH CH3COOC2H5 + H2O.
Lời giải:
- H2SO4 đặc: vừa là chất xúc tác, vừa có tác dụng hút nước, do đó góp phần làm tăng hiệu suất tạo ester.
- Đá bọt: điều hoà quá trình sôi, giúp hỗn hợp sôi đều.
- Dung dịch NaCl bão hoà: dùng để tách ethyl acetate.
Câu hỏi thảo luận 10 trang 129 Hóa học 11: Nêu một số biện pháp để nâng cao hiệu suất của phản ứng.
Lời giải:
Một số biện pháp dùng để tăng hiệu suất của phản ứng:
- Thêm chất xúc tác.
- Lấy dư một trong hai chất đầu.
- Giảm nồng độ các sản phẩm.
Lời giải:
CH3COOH + CH3OH CH3 – COO – CH3 + H2O
Ứng dụng của CH3 – COO – CH3: làm dung môi trong keo, sơn và tẩy sơn móng tay.
4. Ứng dụng của một số carboxylic acid thông dụng
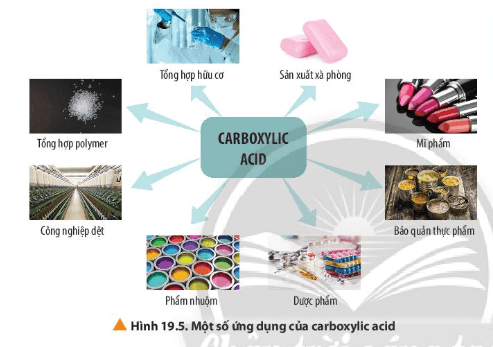
Lời giải:
Một số ứng dụng của carboxylic acid là: Tổng hợp hữu cơ; sản xuất xà phòng, mỹ phẩm, phẩm nhuộm, dược phẩm; tổng hợp polymer; bảo quản thực phẩm…
5. Điều chế
Lời giải:
Phương pháp lên men giấm được thực hiện trong điều kiện thoáng khí, nhiệt độ khoảng 20 oC – 30 oC. Do quá trình lên men giấm là lên men hiếu khí.
Phương trình hoá học: CH3CH2OH + O2 CH3COOH + H2O.
Ứng dụng trong thực tiễn của phương pháp này là để sản xuất giấm ăn do phương pháp này dễ thực hiện, sản phẩm có mùi thơm đặc trưng tuy nhiên thời gian thực hiện thường kéo dài và acetic acid thu được có nồng độ thấp.
Lời giải:
Phương pháp lên men giấm: đây là quá trình oxi hoá dung dịch ethyl alcohol loãng bằng oxygen không khí ở điều kiện thường, dưới tác dụng của men giấm. Phản ứng hoá học xảy ra như sau:
CH3CH2OH + O2 CH3COOH + H2O
Vận dụng làm giấm gạo tại nhà:
Nguyên liệu:
+ 1 kg gạo trắng;
+ 400 g men bia;
+ Đường trắng;
+ 2 quả trứng gà;
+ 1,5 lít nước sạch.
Cách tiến hành:
Bước 1: Vo sạch gạo nấu thành cơm rồi ngâm vào nước và để qua đêm. Sau đó dùng 1 mảnh vải sạch bọc cơm lại, vắt thật kỹ để lấy nước rồi bỏ đường vào theo tỉ lệ 4 : 2 (cứ 4 bát nước thì 2 bát đường). Đun nước vừa vắt trong vòng 30 phút.
Bước 2: Khi nước cơm và đường đã nguội thì cho men bia vào với tỉ lệ 1 : 1. Cho hỗn hợp vào bình thuỷ tinh và đậy kín, sau 4 tuần thu được thành phẩm.
Bước 3: Sau 4 tuần, đổ giấm ra nồi sạch, cho 2 quả trứng gà (chỉ lấy lòng trắng trứng) vào, đun sôi 1 lúc thì tắt bếp. Dùng rây lọc, lọc bỏ hết lòng trắng trứng gà rồi để giấm nguội. Giấm nguội thì cho vào lọ hoặc hũ thuỷ tinh có nắp đậy kín và để ở môi trường thoáng mát để dùng dần.
Bài tập (trang 132)
CH2 = CH2 → CH3CH2OH → CH3COOC2H5.
Lời giải:
CH2 = CH2 + H2O CH3CH2OH
CH3COOH + C2H5OH CH3COOC2H5 + H2O.
Bài 2 trang 132 Hóa học 11: Xác định các chất X, Y, Z và hoàn thành các phản ứng sau:
a) sodium hydroxide + X → sodium methanoate + nước
b) 3 – methylbutanoic acid + Mg → Y + Z
Lời giải:
a) X là HCOOH. Phương trình hoá học:
NaOH + HCOOH → HCOONa + H2O.
b) Y và Z là: [(CH3)2CH – CH2 – COO]2Mg và H2.
2(CH3)2CH – CH2 – COOH + Mg → [(CH3)2CH – CH2 – COO]2Mg + H2.
Bài 3 trang 132 Hóa học 11: Bằng kiến thức hoá học, em hãy giải thích các cách làm sau đây:
a) Khi đồ dùng có đốm gỉ, sử dụng giấm để lau chùi, vết gỉ sẽ hết.
b) Khi thực hiện lên men rượu cần ủ kín, còn khi lên men giấm cần để thoáng.
Lời giải:
a) Giấm ăn là dung dịch acetic acid có nồng độ 2 – 5%, nên có khả năng phản ứng với các vết gỉ để tạo thành muối tan. Do đó, vết gỉ bị rửa trôi khi lau, chùi bằng giấm ăn.
b) Khi thực hiện lên men rượu cần ủ kín do lên men rượu là lên men kị khí; khi thực hiện lên men giấm cần để thoáng do lên men giấm là lên men hiếu khí.
Lời giải:
Phương trình hoá học:
CH3COOH + C2H5OH CH3COOC2H5 + H2O
0,1 0,11 0,1 mol
Theo phương trình hoá học C2H5OH dư, nên số mol CH3COOC2H5 theo lí thuyết tính theo CH3COOH.
Khối lượng ester theo lí thuyết là: 0,1.88 = 8,8 gam.
Hiệu suất phản ứng là:
Xem thêm các bài giải SGK Hoá học 11 Chân trời sáng tạo hay, chi tiết khác:
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.