Toptailieu.vn biên soạn và giới thiệu lời giải SBT Hóa 11 (Chân trời sáng tạo) Ôn tập chương 2 hay, chi tiết sẽ giúp học sinh dễ dàng trả lời câu hỏi từ đó học tốt môn Hoá học 11.
Nội dung bài viết
SBT Hóa 11 (Chân trời sáng tạo) Ôn tập chương 2
Bài OT2.1 trang 31 SBT Hóa học 11: Điều nào sau đây đúng về tính chất hoá học của N2?
A. N2 chỉ có tính khử.
B. N2 chỉ có tính oxi hoá.
C. N2 vừa có tính khử, vừa có tính oxi hoá.
D. N2 có tính acid.
Lời giải:
Ta có, số oxi hóa của N2 là 0. Đây là số oxi hóa trung gian của N.
→ N2 vừa có tính khử, vừa có tính oxi hoá.
→ Chọn C.
Bài OT2.2 trang 31 SBT Hóa học 11: Điều nào sau đây đúng về tính chất hoá học của NH3?
A. NH3 chỉ có tính khử.
B. NH3 chỉ có tính oxi hoá.
C. NH3 vừa có tính khử, vừa có tính oxi hoá.
D. NH3 có tính acid.
Lời giải:
Ta có, số oxi hóa của NH3 là -3. Đây là số oxi hóa thấp nhất của N.
→ NH3 chỉ có tính khử.
→ Chọn A.
A. Dung dịch HNO3 có tính khử mạnh.
B. Dung dịch HNO3 có tính oxi hoá mạnh.
C. Dung dịch HNO3 đặc, nguội không phản ứng với Fe.
D. Dung dịch HNO3 có tính acid.
Lời giải:
Dung dịch HNO3 có không tính khử.
→ Chọn A.
Bài OT2.4 trang 31 SBT Hóa học 11: Phát biểu nào diễn tả đúng tính chất hoá học của SO2?
A. SO2 chỉ có tính khử.
B. SO2 chỉ có tính oxi hoá.
C. SO2 vừa có tính khử, vừa có tính oxi hoá.
D. SO2 không có tính khử và không có tính oxi hoá.
Lời giải:
Ta có, số oxi hóa của SO2 là +4. Đây là số oxi hóa trung gian của S.
→ . SO2 vừa có tính khử, vừa có tính oxi hoá.
→ Chọn C.
A. Dung dịch H2SO4 đặc có tính khử mạnh.
B. Dung dịch H2SO4 đặc có tính oxi hoá mạnh.
C. Dung dịch H2SO4 đặc vừa có tính khử, vừa có tính oxi hoá.
D. Dung dịch H2SO4 đặc không có tính khử, không có tính oxi hoá.
Lời giải:
Các số oxi hóa có thể có của sulfur: -2; 0; +2; +4; +6.
Vì +6 là số oxi hóa lớn nhất của sulfur, do đó trong các phản ứng oxi hóa khử, số oxi hóa của sulfur chỉ có thể giảm về +4 (hoặc +2; 0; -2). Vậy trong phản ứng oxi hóa khử H2SO4 đặc không có khả năng thể hiện tính khử, mà chỉ thể hiện tính oxi hóa.
→ Chọn B.
(A) Sự phân huỷ xác động thực vật bởi vi khuẩn sử dụng nhiều oxygen trong nước gây nên tình trạng thiếu oxygen nghiêm trọng, làm chết cả hệ sinh thái.
(B) Ánh sáng mặt trời bị cản trở làm ảnh hưởng đến quá trình quang hợp. gây thiếu oxygen làm cho thực vật và động vật chết.
(C) Chất dinh dưỡng giúp thực vật và tảo sống trong nước phát triển ồ ạt.
(D) Phân bón và chất dinh dưỡng bị rửa trôi xuống sông, ao, hồ, ...
Lời giải:
Quá trình hình thành sắp hiện tượng phú dưỡng: (D), (C), (B), (A).
Lời giải:
Sulfuric acid đặc ở nhiệt độ thường không tác dụng với Fe (do Fe bị thụ động hoá bởi H2SO4 đặc nguội) nên có thể chuyên chở được trong các toa thùng bằng thép. Khi vòi thoát không được đóng kín ngay, sulfuric acid đặc hấp thụ hơi nước trong không khí rất mạnh và trở thành acid loãng sẽ ăn mòn thành toa thùng rất nhanh.
Không khí → (A)
Methane → (X)
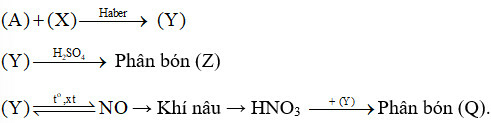
Lời giải:
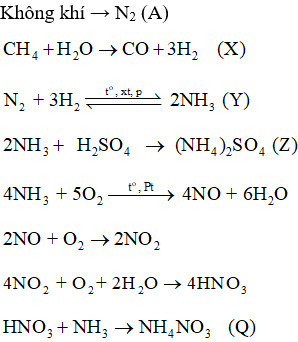
Lời giải:
- Xét cốc (A): Đặt công thức chung của KHCO3 và NaHCO3 là RHCO3.
Ta có:
nRHCO3(1)=nNaHCO3=12084≈1,4(mol)nRHCO3(2)=nKHCO3=120100=1,2(mol)
Đặt số mol của RHCO3 là x (1,2 < x < 1,4).
nH2SO4=100×19,6%100%=19,6(g)⇒mH2SO4=19,698=0,2(mol)
Ta có: 2RHCO3 + H2SO4 → R2SO4 + 2H2O + 2CO2
Vì nRHCO3(2)2>nH2SO41(1,22>0,21) nên RHCO3 dư, H2SO4 hết.
⇒nCO2=12nH2SO4=12×0,4=0,2(mol)⇒m(A)=mRHCO3+mddH2SO4−mCO2=120+100−0,2×44=211,2(g)
- Xét cốc (B): AgNO3 + HCl → AgCl + HNO3
Nước và hydrogen chloride không bay hơi
⇒m(B)=mAgNO3+mddHCl=85+100=185(g)
Để cân bằng, ta cần thêm dung dịch hydrochloric acid 36,5% vào cốc (B).
Khối lượng dung dịch hydrochloric acid 36,5% cho vào cốc (B):mddHCl=m(A)−m(B)=211,2−185=26,2(g)
Xem thêm lời giải Sách bài tập Hóa học lớp 11 bộ sách Chân trời sáng tạo hay, chi tiết khác:
Bài 7: Sulfuric acid và muối sulfate
Bài 8: Hợp chất hữu cơ và hóa học hữu cơ
Bài 9: Phương pháp tách và tinh chế hợp chất hữu cơ
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.