Toptailieu.vn xin giới thiệu 15 câu trắc nghiệm Liên kết hydrogen và tương tác van der waals Cánh diều (có đáp án 2023) CHỌN LỌC, hay nhất giúp học sinh lớp 10 ôn luyện kiến thức để đạt kết quả cao trong các bài thi môn Hóa học.
Mời các bạn đón xem:
15 câu trắc nghiệm Liên kết hydrogen và tương tác van der waals Cánh diều (có đáp án 2023) CHỌN LỌC
Lý thuyết
I. Mở đầu
- Các tính chất vật lí của các chất có liên kết cộng hóa trị được quyết định bởi:
+ Lực tương tác giữa các phân tử
+ Hình dạng của phân tử
+ Mức độ phân cực của liên kết cộng hóa trị trong phân tử
- Lực tương tác giữa các phân tử yếu hơn rất nhiều so với lực liên kết ion, liên kết CHT hay liên kết kim loại
- Một số tương tác điển hình giữa các phân tử
+ Liên kết hydrogen
+ Tương tác van der Waals
II. Liên kết hydrogen
1. Bản chất của liên kết hydrogen
- Bản chất: Nguyên tử hydrogen trong phân tử HF, H2O, NH3 rất linh động, có điện tích dương đủ lớn để hút cặp electron hóa trị chưa liên kết trên nguyên tử F, O hoặc N (của phân tử khác) có độ âm điện lớn tạo thành liên kết hydrogen
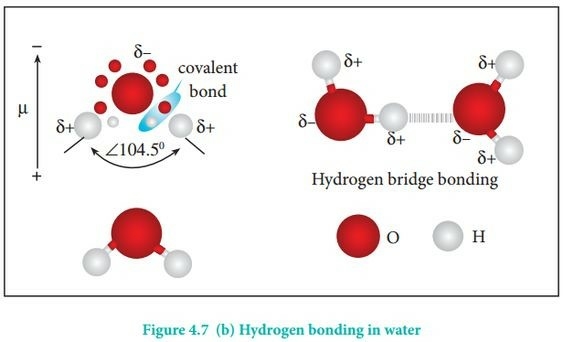
- Điều kiện cần và đủ để tạo thành liên kết hydrogen:
+ Nguyên tử hydrogen liên kết với các nguyên tử có độ âm điện lớn như F, O, N,…
+ Nguyên tử F, O, N,… liên kết với hydrogen phải có ít nhất một cặp electron hóa trị chưa liên kết
- Ví dụ: 1 số kiểu tọa thành liên kết hydrogen
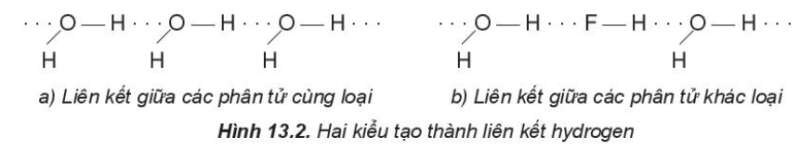
2. Vai trò và ảnh hưởng của liên kết hydrogen tới tính chất vật lí của nước
- Liên kết hydrogen làm tăng nhiệt độ nóng chảy, nhiệt độ sôi của nước
III. Tương tác van der Waals
1. Khái niệm tương tác van der Waals
- Tương tác van der Waals là tương tác tĩnh điện lưỡng cực – lưỡng cực giữa các nguyên tử hay phân tử
- Bản chất:
+ Trong phân tử, các electron không ngừng chuyển động. Khi các electron di chuyển tập trung về một phía bất kì của phân tử sẽ hình thành nên các lưỡng cực tạm thời:
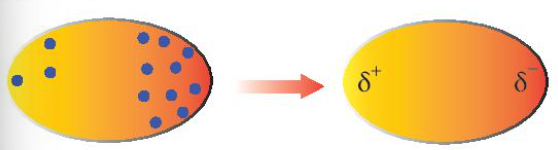
+ Các phân tử có lưỡng cực tạm thời cũng có thể làm các phân tử lân cận xuất hiện các lưỡng cực cảm ứng. Do đó, các phân tử có thể tập hợp thành một mạng lưới với tương tác lưỡng cực cảm ứng, được gọi là tương tác van der Waals
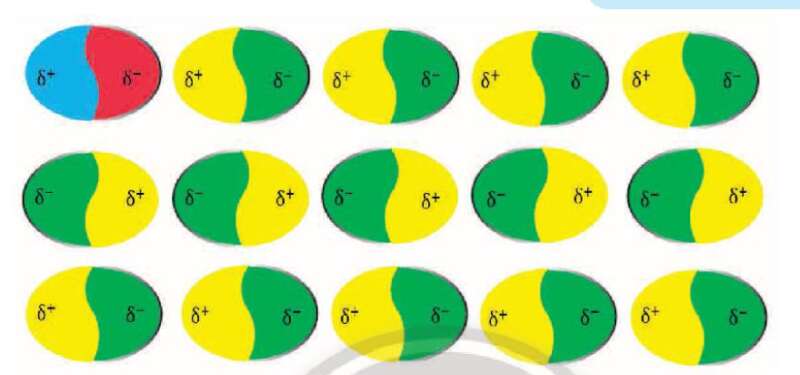
2. Ảnh hưởng của tương tác van der Waals đến nhiệt độ nóng chảy, nhiệt độ sôi của các chất
- Tương tác van der Waals tăng theo sự tăng của số electron trong phân tử. Làm tăng nhiệt độ nóng chảy, nhiệt độ sôi của các chất
Bài tập
Câu 1. Loại liên kết yếu được hình thành giữa nguyên tử H (đã liên kết với một nguyên tử có độ âm điện lớn, thường là F, O, N) với một nguyên tử khác (có độ âm điện lớn thường là F, O, N) còn cặp electron hóa trị chưa tham gia liên kết là
A. liên kết ion
B. liên kết cộng hóa trị có cực
C. liên kết cộng hóa trị không cực
D. liên kết hydrogen
Đáp án: D
Liên kết hydrogen là loại liên kết yếu được hình thành giữa nguyên tử H (đã liên kết với một nguyên tử có độ âm điện lớn, thường là F, O, N) với một nguyên tử khác (có độ âm điện lớn thường là F, O, N) còn cặp electron hóa trị chưa tham gia liên kết.
Câu 2. H2O có nhiệt độ sôi cao hơn H2S là vì
A. H2O có kích thước phân tử nhỏ hơn H2S
B. H2O có khối lượng phân tử nhỏ hơn H2S
C. Giữa các phân tử H2O có liên kết hydrogen
D. Cả A, B và C đều sai
Đáp án: C
H2O có nhiệt độ sôi cao hơn H2S là vì giữa các phân tử H2O có liên kết hydrogen.
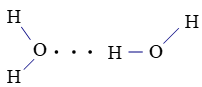
Câu 3. Một phân tử nước có thể tạo liên kết hydrogen tối đa với bao nhiêu phân tử nước khác?
A. 1
B. 2
C. 3
D. 4
Đáp án: D
Trong một phân tử nước, nguyên tử O mang phần điện tích âm còn 2 electron hóa trị chưa tham gia liên kết. Hai nguyên tử H mỗi nguyên tử mang một phần điện tích dương.
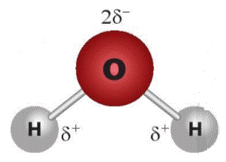
Như vậy:
+ Nguyên tử O có thể tạo liên kết hydrogen với tối đa 2 nguyên tử H ở các phân tử nước khác.
+ 2 nguyên tử H, mỗi nguyên tử H liên kết tối đa được với một nguyên tử O của phân tử nước khác.
Vậy một phân tử nước có thể tạo liên kết hydrogen tối đa với 4 phân tử nước khác.
Câu 4. Giữa các phân tử C2H5OH
A. không tồn tại liên kết hydrogen
B. tồn tại liên kết hydrogen giữa nguyên tử H (liên kết với C) và nguyên tử O
C. tồn tại liên kết hydrogen giữa nguyên tử H (liên kết với O) và nguyên tử O
D. tồn tại liên kết hydrogen giữa nguyên tử H (liên kết với O) và nguyên tử C
Đáp án: C
Giữa các phân tử C2H5OH tồn tại liên kết hydrogen giữa nguyên tử H (liên kết với O có độ âm điện lớn) và nguyên tử O còn cặp electron hóa trị chưa tham gia liên kết.
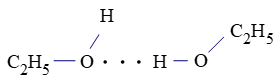
Câu 5. Trong dung dịch NH3 (hỗn hợp NH3 và H2O) tồn tại số loại liên kết hydrogen là
A. 1
B. 2
C. 3
D. 4
Đáp án: D
Liên kết hydrogen giữa nguyên tử H (liên kết với nguyên tử N có độ âm điện lớn) với nguyên tử N còn cặp electron hóa trị riêng.
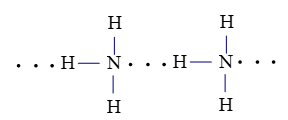
Liên kết hydrogen giữa nguyên tử H (liên kết với nguyên tử N có độ âm điện lớn) với nguyên tử O còn cặp electron hóa trị riêng.
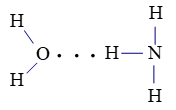
Liên kết hydrogen giữa nguyên tử H (liên kết với nguyên tử O có độ âm điện lớn) với nguyên tử O còn cặp electron hóa trị riêng.
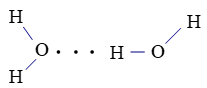
Liên kết hydrogen giữa nguyên tử H (liên kết với nguyên tử O có độ âm điện lớn) với nguyên tử N còn cặp electron hóa trị riêng.
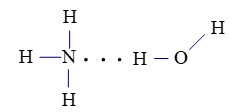
Câu 6. Hợp chất nào dưới đây tạo được liên kết hydrogen liên phân tử?
A. CH4
B. NH3
C. PH3
D. H2S
Đáp án: B
Hợp chất nào dưới đây tạo được liên kết hydrogen liên phân tử là NH3.
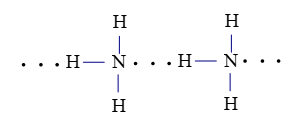
Liên kết hydrogen giữa nguyên tử H (liên kết với nguyên tử N có độ âm điện lớn) với nguyên tử N còn cặp electron hóa trị chưa tham gia liên kết.
Câu 7. Khẳng định đúng là
A. NH3 có độ tan trong nước lớn hơn PH3
B. NH3 có độ tan trong nước thấp hơn PH3
C. NH33 có độ tan trong nước tương tự PH3
D. Cả A, B và C đều sai.
Đáp án: A
NH3 có độ tan trong nước lớn hơn PH3 là đúng vì NH3 có thể tạo liên kết hydrogen với nước còn PH3 thì không. Do đó NH3 tan tốt trong nước.
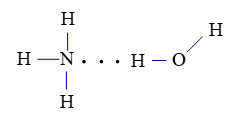
Câu 8. Trong phân tử, khi các electron di chuyển tập trung về một phía bất kì của phân tử sẽ hình thành nên các
A. lưỡng cực tạm thời
B. lưỡng cực cảm ứng
C. lưỡng cực vĩnh viễn
D. một ion âm
Đáp án: A
Trong phân tử, khi các electron di chuyển tập trung về một phía bất kì của phân tử sẽ hình thành nên các lưỡng cực tạm thời.

Câu 9. Tương tác van der Waals là lực tương tác yếu giữa các phân tử, được hình thành do sự xuất hiện của các
A. ion âm và ion dương
B. lưỡng cực tạm thời
C. lưỡng cực cảm ứng
D. Cả B và C.
Đáp án: D
Tương tác van der Waals là lực tương tác yếu giữa các phân tử, được hình thành do sự xuất hiện của các lưỡng cực tạm thời và lưỡng cực cảm ứng.
Câu 10. Tương tác van der Waals làm
A. giảm nhiệt độ nóng chảy và nhiệt độ sôi của các chất
B. giảm nhiệt độ nóng chảy và tăng nhiệt độ sôi của các chất
C. tăng nhiệt độ nóng chảy và giảm nhiệt độ sôi của các chất
D. tăng nhiệt độ nóng chảy và nhiệt độ sôi của các chất
Đáp án: D
Tương tác van der Waals làm tăng nhiệt độ nóng chảy và nhiệt độ sôi của các chất.
Câu 11. Bản chất hình thành liên kết hydrogen và tương tác van der waals đều do
A. sự góp chung electron
B. sự nhường – nhận electron
C. tương tác hút tĩnh điện
D. Cả A, B và C đều sai
Đáp án: C
Bản chất hình thành liên kết hydrogen và tương tác van der waals đều do tương tác hút tĩnh điện.
Câu 12. Khí hiếm nào dưới đây có nhiệt độ sôi thấp nhất?
A. Ne
B. Xe
C. Ar
D. Kr
Đáp án: A
Khối lượng và kích thướng phân tử tăng từ theo thứ tự Ne, Ar, Xe, Kr
Mà tương tác van der Waals tăng khi khối lượng phân tử tăng, kích thước phân tử tăng. Tương tác van der Waals làm tăng nhiệt độ nóng chảy và nhiệt độ sôi của các chất.
Do đó Ne có nhiệt độ sôi thấp nhất.
Câu 13. Tương tác van der Waals tăng khi
A. khối lượng phân tử tăng, kích thước phân tử tăng
B. khối lượng phân tử giảm, kích thước phân tử giảm
C. khối lượng phân tử tăng, kích thước phân tử giảm
D. khối lượng phân tử giảm, kích thước phân tử tăng
Đáp án: A
Tương tác van der Waals tăng khi khối lượng phân tử tăng, kích thước phân tử tăng.
Câu 14. HF có nhiệt độ sôi cao hơn HBr là vì
A. Khối lượng phân tử của HF nhỏ hơn HBr
B. Năng lượng liên kết H – F lớn hơn H – Br
C. Giữa các phân tử HF có liên kết hydrogen còn HBr thì không
D. Cả A, B và C đều sai
Đáp án: C
HF có nhiệt độ sôi cao hơn HBr là vì giữa các phân tử HF có liên kết hydrogen còn HBr thì không.
Để phá vỡ được liên kết hydrogen liên phân tử HF cần cung cấp năng lượng để phá vỡ liên kết và động năng để phân tử chuyển động nhiều hơn so với phân tử HBr. Do đó nhiệt độ sôi của HF cao hơn HBr.
Câu 15. Liên kết hydrogen ảnh hưởng tới tính chất của nước như
A. đặc điểm tập hợp
B. nhiệt độ nóng chảy
C. nhiệt độ sôi
D. Cả A, B và C
Đáp án: D
Liên kết hydrogen ảnh hưởng tới tính chất của nước như: đặc điểm tập hợp, nhiệt độ nóng chảy và nhiệt độ sôi.
Xem thêm các bài giải Trắc nghiệm Hóa lớp 10 Cánh diều hay, chi tiết khác:
Bài 14: Phản ứng hóa học và enthalpy
Bài 15: Ý nghĩa và cách tính biến thiên enthalpy phản ứng hóa học
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.