Với giải Hoá học 11 trang 33 ( Kết nối tri thức ) chi tiết trong Bài 5: Ammonia. Muối ammonium giúp học sinh dễ dàng xem và so sánh lời giải, từ đó biết cách làm bài tập Hoá học 11. Mời các bạn đón xem:
Hoá học 11 trang 33 ( Kết nối tri thức )
Lời giải:
Trong công nghiệp, phản ứng giữa ammonia với acid được dùng để sản xuất phân bón.
Ví dụ:
NH3 + HCl → NH4Cl
NH3 + HNO3 → NH4NO3
2NH3 + H2SO4 → (NH4)2SO4
Trong các phản ứng này ammonia đóng vai trò là base.
Hoạt động 1 trang 33 Hóa học 11: Viết cấu hình electron của các nguyên tử H (Z = 1) và N (Z = 7).
Lời giải:
Cấu hình electron nguyên tử H (Z = 1): 1s1.
Cấu hình electron nguyên tử N (Z = 7): 1s2 2s2 2p3.
Hoạt động 2 trang 33 Hóa học 11: Trình bày các bước lập công thức Lewis của phân tử ammonia.
Lời giải:
Các bước lập công thức Lewis của phân tử ammonia (NH3):
Cách 1: Viết công thức Lewis dựa vào công thức electron
Bước 1: Viết công thức electron:
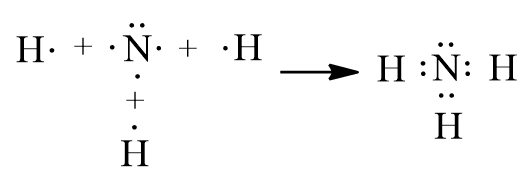
Bước 2: Từ công thức electron, thay 1 cặp electron dùng chung bằng 1 gạch nối giữa hai nguyên tử ta được công thức Lewis:
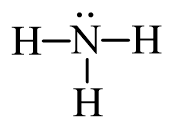
Cách 2: Thực hiện lần lượt theo các bước sau:
Bước 1: Tính tổng số electron hóa trị trong phân tử:
Nitrogen (N) có 5 electron hóa trị, hydrogen có 1 electron hóa trị. Trong phân tử NH3 có 1 nguyên tử N và 3 nguyên tử H. Vậy tổng số electron hóa trị = 5 + 3.1 = 8 electron
Bước 2: Vẽ khung phân tử tạo bởi liên kết đơn giữa các nguyên tử:
Trong phân tử NH3, nguyên tử N cần 3 electron để đạt octet, mỗi nguyên tử H cần 1 electron để đạt octet. Vì vậy, N là nguyên tử trung tâm, còn các nguyên tử H được xếp xung quanh:
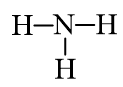 (1)
(1)
Bước 3: Tính số electron hóa trị chưa tham gia liên kết bằng cách lấy tổng số electron trừ số electron tham gia tạo liên kết:
Số electron hóa trị chưa tham gia liên kết trong sơ đồ là: 8 – 2.3 = 2 electron.
Bước 4: Hoàn thiện octet cho các nguyên tử có độ âm điện lớn hơn trong sơ đồ:
Từ công thức (1), nguyên tử H đã đủ octet, hoàn thiện octet cho N. Xung quanh nguyên tử N mới có 6 electron, ta bổ sung 2 electron vào nguyên tử N. Ta được công thức (2) chính là công thức Lewis của NH3:
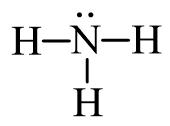 (2)
(2)
Xem thêm các bài giải Hoá học 11 Kết nối tri thức hay, chi tiết khác:
Hoá học 11 trang 34 ( Kết nối tri thức )
Hoá học 11 trang 35 ( Kết nối tri thức )
Hoá học 11 trang 36 ( Kết nối tri thức )
Hoá học 11 trang 37 ( Kết nối tri thức )
Xem thêm các bài giải Hoá học 11 Kết nối tri thức hay, chi tiết khác:
Mở đầu trang 33 Hóa học 11: Từ ammonia, thông qua phản ứng nào có thể sản xuất...
Hoạt động 1 trang 33 Hóa học 11: Viết cấu hình electron của các nguyên tử H (Z = 1) và N (Z = 7).
Hoạt động 2 trang 33 Hóa học 11: Trình bày các bước lập công thức Lewis của phân tử ammonia.
Câu hỏi 1 trang 34 Hóa học 11: Từ đặc điểm cấu tạo của phân tử ammonia, hãy giải thích...
Câu hỏi 2 trang 34 Hóa học 11: Hãy giải thích tại sao ammonia tan tốt trong nước
Hoạt động trang 34 Hóa học 11: Trong công nghiệp, phản ứng giữa ammonia với acid...
Câu hỏi 3 trang 34 Hóa học 11: Trong hai phản ứng oxi hoá ammonia bằng oxygen ở trên, hãy:
Hoạt động trang 35 Hóa học 11: Sưu tầm một số hình ảnh để báo cáo, thuyết trình về...
Hoạt động trang 35 Hóa học 11: Vận dụng kiến thức về cân bằng hoá học,...
Thí nghiệm trang 36 Hóa học 11: Nhận biết ion ammonium trong phân đạm
Câu hỏi 4 trang 37 Hóa học 11: a) So sánh phân tử ammonia và ion ammonium về dạng hình học...
Em có thể trang 37 Hóa học 11: - Vận dụng được kiến thức về cân bằng hoá học, tốc độ phản ứng....
Xem thêm các bài giải Hoá học 11 Kết nối tri thức hay, chi tiết khác:
Hoá học 11 ( Kết nối tri thức ) Bài 3: Ôn tập chương 1
Hoá học 11 (Kết nối tri thức) Bài 4: Nitrogen
Hoá học 11 (Kết nối tri thức) Bài 6: Một số hợp chất của nitrogen với oxygen
Hoá học 11 (Kết nối tri thức) Bài 7: Sulfur và sulfur dioxide
Hoá học 11 (Kết nối tri thức) Bài 8: Sulfuric acid và muối sulfate
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.