Với giải Hoá học 11 trang 19 ( Cánh diều ) chi tiết trong Bài 2: Sự điện li trong dung dịch nước. Thuyết Bronsted – Lowry về acid - base giúp học sinh dễ dàng xem và so sánh lời giải, từ đó biết cách làm bài tập Hoá học 11. Mời các bạn đón xem:
Hoá học 11 trang 19 ( Cánh diều )
Lời giải:
- Dung dịch phèn sắt (NH4Fe(SO4)2.12H2O) có môi trường acid. Do trong nước, phèn sắt bị phân li hoàn toàn theo phương trình:
NH4Fe(SO4)2.12H2O → NH4+ + Fe3+ + 2SO42- + 12H2O
Ion NH4+ và Fe3+ đóng vai trò là acid trong các cân bằng:
NH4+ + H2O ⇌ NH3 + H3O+ (*)
Fe3+ + 3H2O ⇌ Fe(OH)3 + 3H+ (**)
- Người ta có thể dùng phèn sắt để loại bỏ các chất lơ lửng trong nước bởi ion Fe3+ tạo Fe(OH)3 theo (**) ở dạng kết tủa, có khả năng hấp phụ các chất rồi lắng xuống đáy bể.
a) Chất X là chất điện li.
b) Trong dung dịch chất X có các ion dương và ion âm.
c) Chất X ở trạng thái rắn khan cũng dẫn điện.
d) Trong dung dịch chất X có electron tự do.
Lời giải:
Đáp án đúng là: (c); (d)
Phát biểu (c) không đúng do X ở trạng thái rắn, khan không dẫn điện.
Phát biểu (d) không đúng do dung dịch chất X có các ion dương và ion âm.
Lời giải:
Giả sử nồng độ của dung dịch HCl bằng nồng độ của dung dịch CH3COOH và bằng x M.
HCl là acid mạnh, phân li hoàn toàn trong nước:
HCl → H+ + Cl-
x → x x M
CH3COOH là acid yếu, phân li một phần trong nước:
CH3COOH ⇌ CH3COO- + H+
x M
Suy ra [CH3COO-] = [H+] < x M
Vậy dung dịch HCl dẫn điện tốt hơn dung dịch CH3COOH có cùng nồng độ do trong dung dịch HCl (x M) có nhiều phần tử mang điện hơn dung dịch CH3COOH (x M).
Bài 3 trang 19 Hoá học 11: Giải thích vai trò của nước trong sự điện li của HCl và NaOH.
Lời giải:
Nước là dung môi phân cực, đóng vai trò quan trọng trong sự điện li của HCl và NaOH.
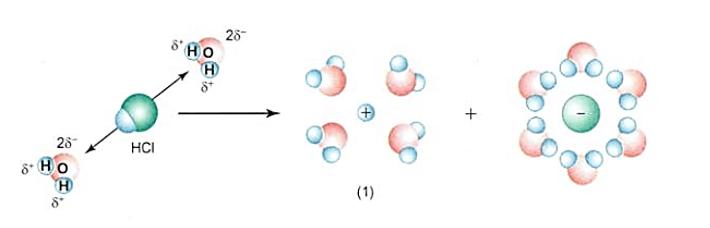
+ Khi tan trong nước, các phân tử HCl hút về chúng những cực ngược dấu của các phân tử nước. Do sự tương tác giữa các phân tử nước và phân tử HCl, kết hợp với sự chuyển động không ngừng của các phân tử nước dẫn đến sự điện li phân tử HCl ra các ion H+ và Cl-.
+ NaOH là hợp chất ion, trong tinh thể có các ion Na+ và OH- liên kết với nhau bằng lực hút tĩnh điện. Nước là dung môi phân cực. Khi cho tinh thể NaOH vào nước, các ion Na+ và OH- trên bề mặt hút các phân tử nước lại gần. Các phân tử nước hướng các đầu âm vào ion Na+, các đầu dương vào ion OH- làm yếu liên kết giữa các cation, anion trong tinh thể và khuếch tán vào nước.
Xem thêm các bài giải Hoá học 11 Cánh diều hay, chi tiết khác:
Hoá học 11 trang 15 ( Cánh diều )
Hoá học 11 trang 16 ( Cánh diều )
Hoá học 11 trang 17 ( Cánh diều )
Hoá học 11 trang 18 ( Cánh diều )
Xem thêm các bài giải Hoá học 11 Cánh diều hay, chi tiết khác:
Mở đầu trang 15 Hoá học 11: Quan sát Hình 2.1, em hãy nêu những sự khác nhau giữa...
Câu hỏi 1 trang 16 Hoá học 11: Trong thí nghiệm trên, đèn sáng hay không sáng chứng...
Luyện tập 1 trang 16 Hoá học 11: Dự đoán trong thí nghiệm trên, cốc thuỷ tinh chứa nước...
Luyện tập 2 trang 16 Hoá học 11: Tìm hiểu và cho biết những chất nào sau đây thuộc...
Câu hỏi 2 trang 17 Hoá học 11: Ở quá trình (3b), nước đóng vai trò là acid hay base? Vì sao?
Luyện tập 3 trang 17 Hoá học 11: Trong cân bằng (4), hãy chỉ ra hai acid và hai base. Giải thích.
Câu hỏi 3 trang 17 Hoá học 11: Dựa vào cân bằng (4) và (5), hãy giải thích vì sao H2O được...
Luyện tập 4 trang 18 Hoá học 11: Cho các phân tử sau: HBr, HI, H2S, KOH. Hãy phân loại...
Câu hỏi 4 trang 18 Hoá học 11: Trong các cân bằng (7), (8a) và (8b), xác định các acid và base.
Vận dụng trang 19 Hoá học 11: Tương tự Ví dụ 5, hãy cho biết dung dịch phèn sắt....
Bài 1 trang 19 Hoá học 11: Nếu dòng điện chạy qua được dung dịch nước của một chất X...
Bài 2 trang 19 Hoá học 11: Giải thích vì sao dung dịch HCl dẫn điện tốt hơn dung dịch....
Bài 3 trang 19 Hoá học 11: Giải thích vai trò của nước trong sự điện li của HCl và NaOH.
Xem thêm các bài giải Hoá học 11 Cánh diều hay, chi tiết khác:
Hoá học 11 (Cánh diều) Bài 1: Mở đầu về cân bằng hoá học
Hoá học 11 (Cánh diều) Bài 3: PH của dung dịch. Chuẩn độ acid – base
Hoá học 11 (Cánh diều) Bài 4: Đơn chất nitrogen
Hoá học 11 (Cánh diều) Bài 5: Một số hợp chất quan trọng của nitrogen
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.