Toptailieu.vn giới thiệu Giải bài tập Hóa học 9 Bài 8: Một số bazơ quan trọng chính xác, chi tiết nhất giúp học sinh dễ dàng làm bài tập Một số bazơ quan trọng lớp 9.
Giải bài tập Hóa học 9 Bài 8: Một số bazơ quan trọng
Bài tập trang 27,30 SGK Hóa học 9
Bài 1 trang 27 SGK Hóa học 9: Có 3 lọ không nhãn, mỗi lọ đựng chất rắn sau: NaOH, Ba(OH)2, NaCl. Hãy trình bày cách nhận biết chất đựng trong mỗi lọ bằng phương pháp hóa học. Viết các phương trình hóa học (nếu có).
Phương pháp giải
Dựa vào tính chất hóa học của các chất và hiện tượng khác nhau quan sát được => chọn chất chỉ thị phân biệt các chất trên
Gợi ý: Hòa tan các mẫu thử trên vào nước, sau đó dùng quỳ tím và dd H2SO4 loãng
Lời giải
Bước 1: Lấy ra 1 lượng ở từng mẫu thử
Bước 2: Hòa tan mẫu thử từng chất vào nước để tạo thành các dung dịch tương ứng.
Bước 3: Cho quỳ tím vào mỗi dung dịch: Nếu quỳ tím chuyển sang màu xanh là NaOH và Ba(OH)2, nếu quỳ tím không đổi màu là NaCl.
=> Nhận biết được NaCl
Bước 4: Dẫn khí CO2 vào hai dung dịch bazơ còn lại. Dung dịch nào có kết tủa xuất hiện là Ba(OH)2 , dung dịch không có kết tủa là NaOH.
Ba(OH)2 + CO2 → BaCO3↓ + H2O
2NaOH + CO2 → Na2CO3 + H2O
Bài 2 trang 27 SGK Hóa học 9: Có những chất sau:.
Hãy chọn chất thích hợp điền vào mỗi sơ đồ phản ứng sau và lập phương trình học:
a) ;
b) ;
c) ;
d) ;
e) .
Lời giải
a) ;
b) ;
c) ;
d) ;
e)
Bài 3 trang 27 SGK Hóa học 9: Dẫn từ từ 1,568 lít khí CO2 (đktc) vào một dung dịch có hòa tan 6,4 gam NaOH, sản phẩm là muối Na2CO3.
a) Chất nào đã lấy dư và dư là bao nhiêu (lít hoặc gam)?
b) Hãy xác định khối lượng muối thu được sau phản ứng.
Phương pháp giải
Đổi số mol CO2 ; mol NaOH
Viết PTHH: 2NaOH + CO2 → Na2CO3 + H2O
Lập tỉ lệ
Tỉ lệ nào nhỏ hơn thì chất đó phản ứng hết. Mọi tính toán theo chất phản ứng hết.
Lời giải
Số mol: nCO2 = = 0,07 mol; nNaOH = = 0,16 mol
Phương trình hóa học:
2NaOH + CO2 → Na2CO3 + H2O
Theo PTHH 2 1 ( mol)
Theo đề bài 0,16 0,07 ( mol)
Ta có: .
Vậy CO2 phản ứng hết. NaOH dư. Mọi tính toán theo số mol của CO2
Theo PTHH: nNaOH pư = 2nCO2 = 2.0,07 = 0,14 (mol)
=> nNaOH dư = 0,16 – 0,14 = 0,02 (mol)
a) Chất còn dư là NaOH và dư: 0,02 x 40 = 0,8 g
b) nNa2CO3 = nCO2 = 0,07 (mol)
Khối lượng muối Na2CO3 tạo thành là: 0,07 x 106 = 7,42 g.
Bài 1 trang 30 SGK Hóa học 9: Viết các phương trình hóa học thực hiện những chuyển đổi hóa học sau:
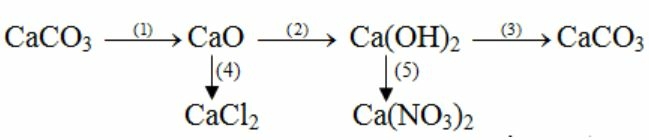
Lời giải
(1) CaCO3 CaO + CO2
(2) CaO + H2O → Ca(OH)2
(3) Ca(OH)2 + CO2 → CaCO3 + H2O
(4) CaO + 2HCl → CaCl2 + H2O
(5) Ca(OH)2 + 2HNO3 → Ca(NO3)2 + 2H2O
Bài 2 trang 30 SGK Hóa học 9: Có ba lọ không nhãn, mỗi lọ đựng một trong ba chất rắn màu trắng sau:CaCO3, CaO, Ca(OH)2 . Hãy nhận biết chất đựng trong mỗi lọ bằng phương pháp hóa học. Viết các phương pháp hóa học.
Phương pháp giải
Gợi ý: Dùng nước
Lời giải
Hòa tan 3 chất rắn trên vào nước:
+ Chất rắn không tan là CaCO3
+ Chất rắn tan đồng thời tỏa nhiều nhiệt là CaO
CaO + H2O → Ca(OH)2
+ Chất chỉ tan một phần tạp chất lỏng màu trắng và có một phần kết tủa lắng dưới đáy : Ca(OH)2
Bài 3 trang 30 SGK Hóa học 9: Hãy viết các phương trình hóa học của phản ứng khi cho dung dịch NaOH tác dụng với dung dịch H2SO4 tạo ra:
a) Muối natri hiđrosunfat.
b) Muối natrisunfat.
Lời giải
a) Muối natri hiđrosunfat:
H2SO4 + NaOH → H2O + NaHSO4
b) Muối natri sunfat:
H2SO4 + 2NaOH → 2H2O + Na2SO4
Bài 4 trang 30 SGK Hóa học 9: Một dung dịch bão hòa khí CO2 trong nước có pH = 4. Hãy giải thích và viết phương trình hóa học của CO2 với nước.
Phương pháp giải
pH là giá trị để đo một dung dịch có môi trường axit, bazo hay trung tính
pH = 7 môi trường trung tính
pH > 7 môi trường bazơ
pH < 7 môi trường axit
Lời giải
Dung dịch bão hòa CO2 có pH = 4, nghĩa là dung dịch có tính axit yếu. Vì khí CO2 tác dụng với nước tạo thành axit cacbonic, là một axit rất yếu:
CO2 + H2O H2CO3
Lý thuyết Một số bazơ quan trọng
A. NATRI HIĐROXIT (NaOH)
I. Tính chất vật lí
- Natri hiđroxit là chất rắn không màu, hút ẩm mạnh, tan nhiều trong nước và tỏa nhiệt.
- Dung dịch NaOH có tính nhờn, làm bục vải giấy và ăn mòn da. Khi sử dụng NaOH phải hết sức cẩn thận.
II. Tính chất hóa học
Natri hiđroxit có đầy đủ tính chất của một bazơ tan (kiềm).
1. Làm đổi màu chất chỉ thị.
- Dung dịch NaOH làm đổi màu qùy tím thành xanh.
- Dung dịch phenolphatalein không màu thành màu đỏ.
2. Tác dụng với axit → muối + nước (phản ứng trung hòa)
Thí dụ:
NaOH + HCl → NaCl + H2O
2NaOH + H2SO4 → Na2SO4 + H2O
3. Tác dụng với oxit axit → muối + nước
Thí dụ:
2NaOH + CO2 → Na2CO3 + H2O
2NaOH + SO2 → Na2SO3 + H2O
(khi NaOH tác dụng với còn có thể tạo ra muối axit NaHCO3, NaHSO3)
4. Tác dụng với dung dịch muối.
Thí dụ:
2NaOH + CuSO4 → Na2SO4 + Cu(OH)2↓
III. Ứng dụng
Natri hiđroxit có nhiều ứng dụng trong đời sống và trong sản xuất. Nó được dùng trong:
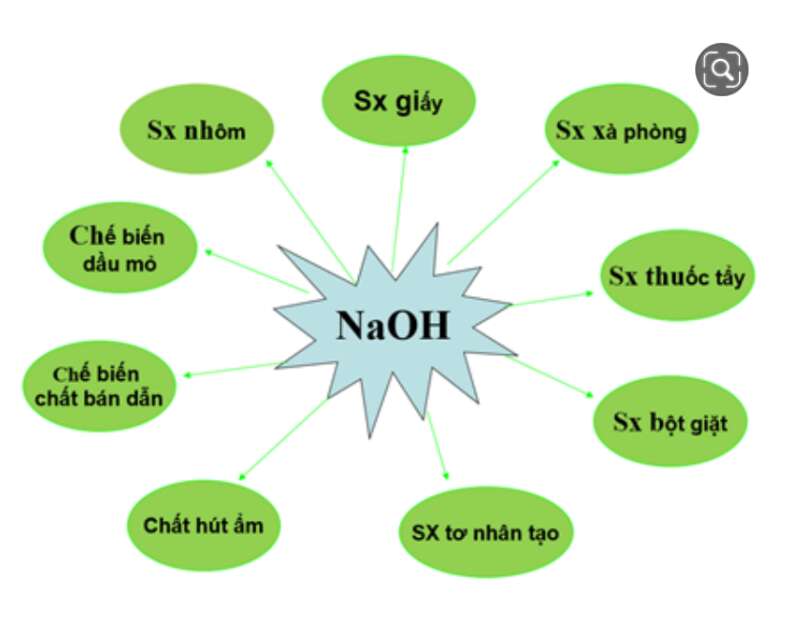
IV. Sản xuất Natri hiđroxit
- Trong công nghiệp, NaOH được điều chế bằng cách điện phân dung dịch NaCl
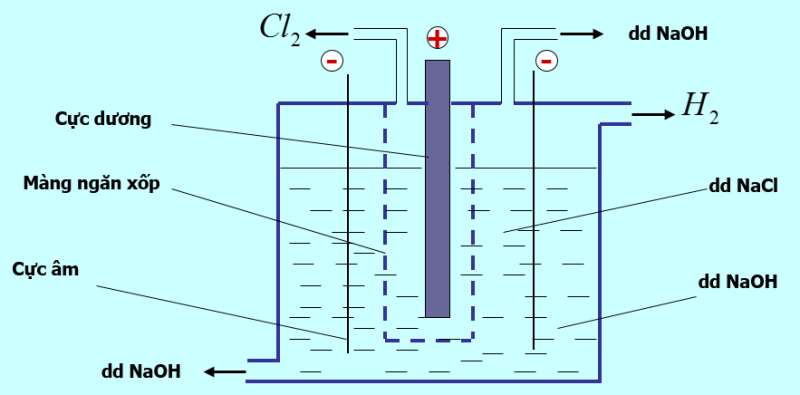
- Phương trình điện phân:
2NaCl + 2H2O 2NaOH + H2 + Cl2
- Tác dụng của màng ngăn xốp: không cho khí clo thoát ra tác dụng với dung dịch NaOH vì xảy ra phản ứng:
Cl2 + 2NaOH → NaCl + NaClO + H2O
B. CANXI HIĐROXIT Ca(OH)2
I. Tính chất hóa học Ca(OH)2
- Ca(OH)2 có tính chất hóa học của một bazơ tan.
1. Làm đổi màu chất chỉ thị
- Làm đổi màu qùy tím thành xanh.
- Dung dịch phenolphatalein không màu thành màu đỏ.
2. Ca(OH)2 + axit → muối + nước (phản ứng trung hòa)
Phương trình hóa học :
Ca(OH)2 + 2HCl → CaCl2 + 2H2O
Ca(OH)2 + H2SO4 → CaSO4 + H2O
3. Dung dịch Ca(OH)2 + oxit axit → muối + nước
Phương trình hóa học
Ca(OH)2 + CO2 → CaCO3↓ + H2O
Ca(OH)2 + SO2 → CaSO3↓ + H2O
4. Ca(OH)2 + dung dịch muối → muối mới + bazo mới
Phương trình hóa học
Ca(OH)2 + FeCl2 → Fe(OH)2↓ + CaCl2
II. Ứng dụng
- Làm vật liệu trong xây dựng.
- Khử chua đất trồng trọt.
- Khử độc các chất thải công nghiệp, diệt trùng chất thải sinh hoạt và xác chết động vật…
III. Thang PH
- pH = 7: Dung dịch là trung tính Thí dụ : nước cất có pH = 7
- pH < 7: Dung dịch có tính axit, pH càng nhỏ độ axit càng lớn.
- pH > 7: Dung dịch có tính bazơ, pH càng lớn độ bazơ càng lớn.
Sơ đồ tư duy: Một số bazo quan trọng
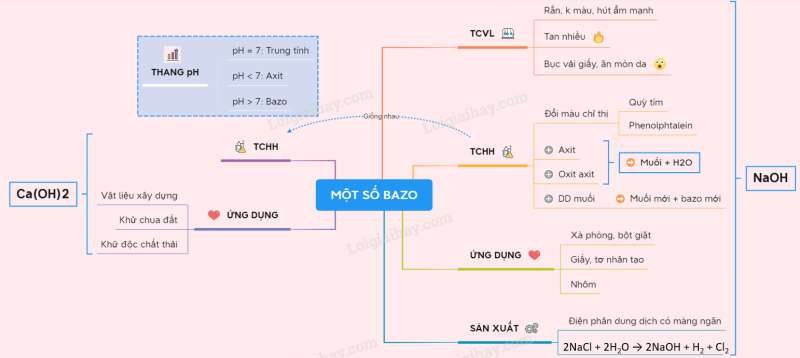
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.